10 प्रकार के रासायनिक बंधन (उदाहरण के साथ समझाया गया)
रासायनिक बंधन हैं बल जो परमाणुओं को एक साथ रखते हैं अणु बनाने के लिए। परमाणुओं के बीच तीन प्रकार के बंधन होते हैं:
- धात्विक बंधन।
- आयोनिक बंध।
- सहसंयोजक बंधन: गैर-ध्रुवीय, ध्रुवीय, सरल, दोहरा, ट्रिपल, मूल।
इन बंधों की बदौलत प्रकृति में मौजूद सभी यौगिक बनते हैं। ऐसे बल भी हैं जो अणुओं को एक साथ रखते हैं, जिन्हें अंतर-आणविक बंधन के रूप में जाना जाता है, जैसे:
- हाइड्रोजन बांड या पुल।
- द्विध्रुवीय-द्विध्रुवीय बल।
इसके बाद, हम इनमें से प्रत्येक लिंक की व्याख्या करते हैं।
| रासायनिक बंधन के प्रकार | विशेषता | उदाहरण | |
|---|---|---|---|
| धातु | धातु आयन गतिमान इलेक्ट्रॉनों के समुद्र में तैरते हैं। | धातु तत्व: सोडियम, बेरियम, चांदी, लोहा, तांबा। | |
| ईओण का | एक परमाणु से दूसरे परमाणु में इलेक्ट्रॉनों का स्थानांतरण। | सोडियम क्लोराइड+क्लोरीन- | |
| सहसंयोजक | गैर ध्रुवीय | इलेक्ट्रॉनों को दो परमाणुओं के बीच समान रूप से साझा करें। | आण्विक हाइड्रोजन एच-एच या एच2 |
| ध्रुवीय | दो परमाणुओं के बीच असमान रूप से इलेक्ट्रॉनों को साझा करें। | जल अणु एच2या | |
| सरल | इलेक्ट्रॉनों की एक जोड़ी साझा करें। | क्लोरीन अणु Cl2 सीएल-क्ली | |
| दोहरा | इलेक्ट्रॉनों के दो जोड़े साझा करें। | ऑक्सीजन अणु O2 ओ = ओ | |
| ट्रिपल | इलेक्ट्रॉनों के तीन जोड़े साझा करें। | नाइट्रोजन अणु N≣N या N2 | |
| संप्रदान कारक | परमाणुओं में से केवल एक ही इलेक्ट्रॉनों को साझा करता है। | यौगिक अमोनिया-बोरॉन ट्राइफ्लोराइड में नाइट्रोजन और बोरॉन के बीच का बंधन। | |
| अंतर आणविक बल | हाइड्रोजन ब्रिज | एक अणु के हाइड्रोजन दूसरे अणु के विद्युत ऋणात्मक परमाणुओं की ओर आकर्षित होते हैं। | एक पानी के अणु में हाइड्रोजन और दूसरे पानी के अणु में ऑक्सीजन के बीच हाइड्रोजन बंधन। |
| द्विध्रुवीय-द्विध्रुवीय | दो विद्युत ध्रुवों वाले अणु अन्य अणुओं के विपरीत ध्रुवों को आकर्षित करते हैं। | मेथनल एच अणुओं के बीच बातचीत2सी = ओ |
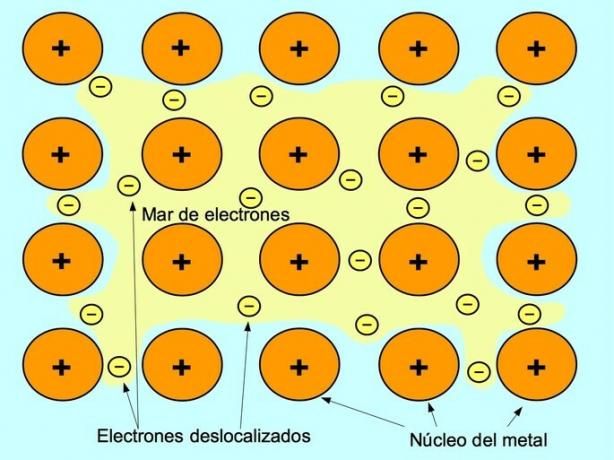
धात्विक बंधन
धात्विक बंधन धात्विक तत्वों के धनात्मक आयनों और आयनों के बीच मुक्त गतिमान ऋणात्मक इलेक्ट्रॉनों के बीच आकर्षण बल है। धातु परमाणुओं को कसकर पैक किया जाता है, इससे इलेक्ट्रॉनों को परमाणुओं की जाली के भीतर स्थानांतरित करने की अनुमति मिलती है।
धातुओं में, वैलेंस इलेक्ट्रॉन अपने मूल परमाणु से मुक्त होते हैं और इलेक्ट्रॉनों का एक "समुद्र" बनाते हैं जो संपूर्ण धातु संरचना के चारों ओर तैरता है। यह धातु के परमाणुओं को सकारात्मक रूप से आवेशित धातु आयनों में बदलने का कारण बनता है जो एक साथ पैक होते हैं।
सोडियम ना, बेरियम बा, कैल्शियम सीए, मैग्नीशियम एमजी, गोल्ड एयू, सिल्वर एजी और एल्युमिनियम अल जैसे धात्विक तत्वों के बीच धात्विक बंधन स्थापित होता है।
आयोनिक बंध
आयनिक बंधन वह बल है जो एक धातु तत्व, जैसे सोडियम या मैग्नीशियम, को गैर-धातु तत्व, जैसे क्लोरीन या सल्फर के साथ जोड़ता है। धातु इलेक्ट्रॉनों को खो देता है और एक सकारात्मक धातु आयन में बदल जाता है जिसे कहा जाता है कटियन. ये इलेक्ट्रॉन अधात्विक तत्व में चले जाते हैं और यह एक ऋणावेशित आयन में बदल जाता है जिसे कहा जाता है ऋणायन.
धनायन और आयन मिलकर एक त्रि-आयामी नेटवर्क बनाते हैं जो विभिन्न आवेशों वाले आयनों के बीच इलेक्ट्रोस्टैटिक आकर्षण की ताकतों द्वारा बनाए रखा जाता है। ये बल आयनिक यौगिक बनाते हैं।
पृथ्वी की पपड़ी मुख्य रूप से आयनिक यौगिकों से बनी है। अधिकांश चट्टानें, खनिज और रत्न आयनिक यौगिक हैं। उदाहरण के लिए:
- सोडियम क्लोराइड NaCl: धात्विक तत्व सोडियम है जो एक इलेक्ट्रॉन को क्लोरीन में स्थानांतरित करता है, जो अधातु तत्व है।
- मैग्नीशियम क्लोराइड MgCl2: मैग्नीशियम Mg दो क्लोरीन परमाणुओं को दो इलेक्ट्रॉन दान करता है, जैसा कि नीचे दिए गए चित्र में दिखाया गया है:
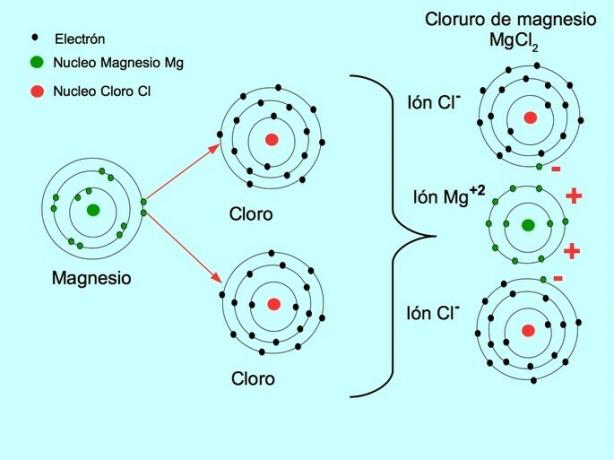
यह सभी देखें धनायनों और आयनों के बीच अंतर.
सहसंयोजक बंधन
सहसंयोजक बंधन तब बनता है जब दो गैर-धातु परमाणु इलेक्ट्रॉनों को साझा करते हैं। परमाणुओं के इलेक्ट्रॉनों के लिए आत्मीयता और साझा किए गए इलेक्ट्रॉनों की मात्रा के आधार पर यह बंधन कई प्रकार का हो सकता है।
गैर-ध्रुवीय सहसंयोजक बंधन
गैर-ध्रुवीय सहसंयोजक बंधन वह बंधन है जो दो परमाणुओं के बीच बनता है जहां इलेक्ट्रॉनों को समान रूप से साझा किया जाता है। यह बंधन सामान्य रूप से सममित अणुओं में होता है, अर्थात दो समान परमाणुओं से बने अणु, जैसे हाइड्रोजन अणु H2 और ऑक्सीजन अणु O2.

ध्रुवीय सहसंयोजक बंधन
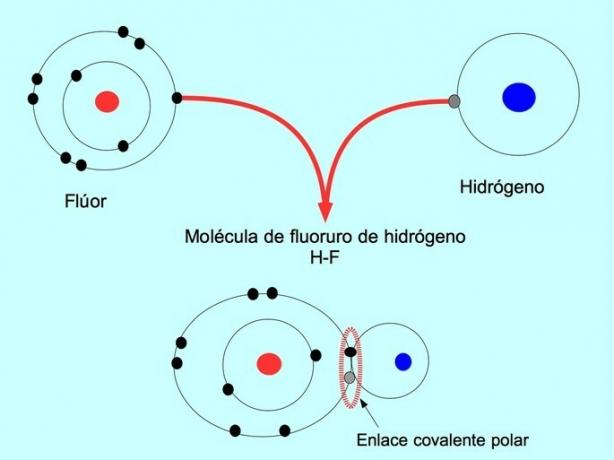
ध्रुवीय सहसंयोजक बंधन तब बनता है जब दो परमाणु इलेक्ट्रॉनों को साझा करते हैं लेकिन उनमें से एक में इलेक्ट्रॉनों के लिए अधिक आकर्षण होता है। इससे अणु में अधिक इलेक्ट्रॉनों के साथ अधिक नकारात्मक "ध्रुव" होता है और विपरीत ध्रुव अधिक सकारात्मक होता है।
इस वितरण या इलेक्ट्रॉनों के असंतुलन वाले अणुओं को ध्रुवीय के रूप में जाना जाता है। उदाहरण के लिए, हाइड्रोजन फ्लोराइड एचएफ में, हाइड्रोजन और फ्लोरीन के बीच एक सहसंयोजक बंधन होता है, लेकिन फ्लोरीन में उच्च विद्युतीयता होती है, इसलिए यह इलेक्ट्रॉनों को अधिक मजबूती से आकर्षित करती है साझा किया।
सरल सहसंयोजक बंधन
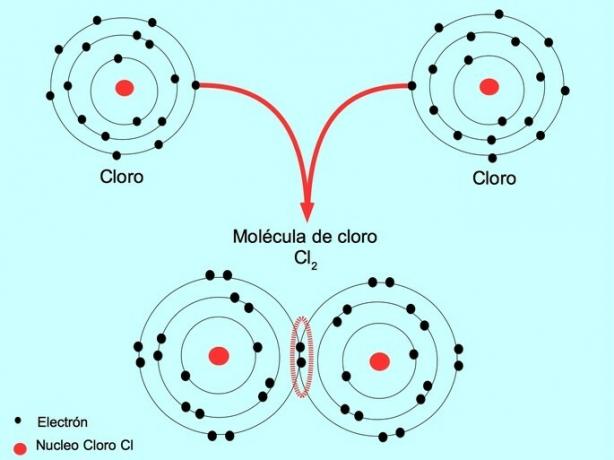
जब दो परमाणु दो इलेक्ट्रॉनों को साझा करते हैं, प्रत्येक से एक, तो बनने वाले सहसंयोजक बंधन को एकल सहसंयोजक बंधन कहा जाता है।
उदाहरण के लिए, क्लोरीन एक परमाणु है जिसके बाहरी कोश में सात वैलेंस इलेक्ट्रॉन होते हैं, जिसे आठ इलेक्ट्रॉनों से भरा जा सकता है। एक क्लोरीन दूसरे क्लोरीन के साथ मिलकर क्लोरीन अणु Cl. बना सकता है2 जो अकेले क्लोरीन से कहीं अधिक स्थिर है।
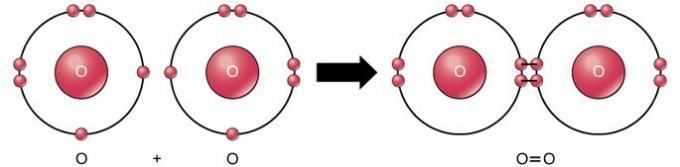
दोहरा सहसंयोजक बंधन
दोहरा सहसंयोजक बंधन वह बंधन है जहां दो परमाणुओं के बीच इलेक्ट्रॉनों के चार इलेक्ट्रॉन (दो जोड़े) साझा किए जाते हैं। उदाहरण के लिए, ऑक्सीजन के अंतिम कोश में 6 इलेक्ट्रॉन होते हैं। जब दो ऑक्सीजन संयुक्त होते हैं, तो दोनों के बीच चार इलेक्ट्रॉन साझा होते हैं, जिससे प्रत्येक के अंतिम कोश में 8 इलेक्ट्रॉन होते हैं।
ट्रिपल सहसंयोजक बंधन
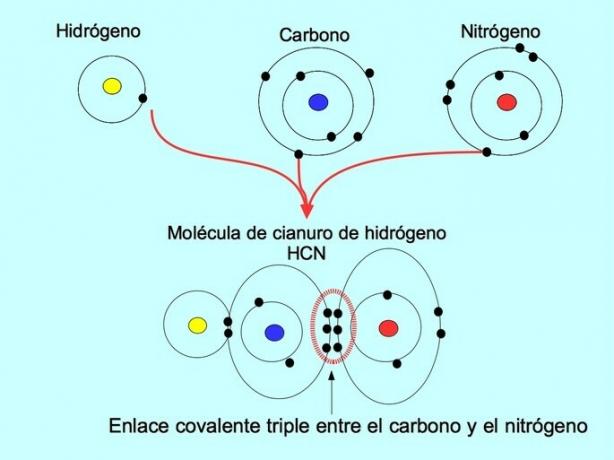
ट्रिपल सहसंयोजक बंधन तब बनता है जब दो परमाणुओं के बीच 6 इलेक्ट्रॉन (या तीन जोड़े) साझा किए जाते हैं। उदाहरण के लिए, हाइड्रोजन साइनाइड अणु एचसीएन में, कार्बन और नाइट्रोजन के बीच एक ट्रिपल बॉन्ड बनता है, जैसा कि नीचे दिए गए चित्र में प्रस्तुत किया गया है:
समन्वय या मूल सहसंयोजक बंधन
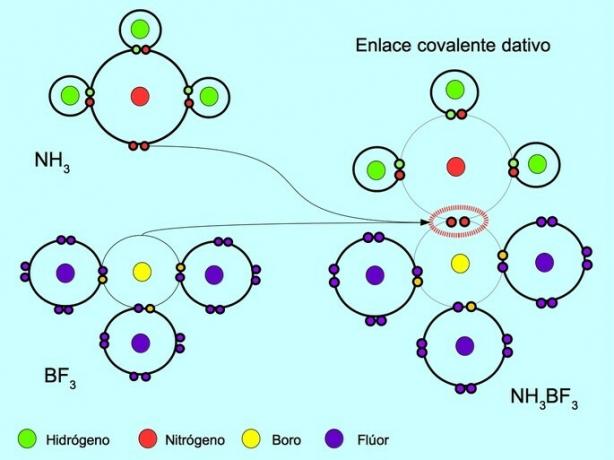
समन्वित या मूल सहसंयोजक बंधन वह बंधन है जो तब बनता है जब बंधन में केवल एक परमाणु एक इलेक्ट्रॉन जोड़ी का योगदान देता है। उदाहरण के लिए, जब अमोनिया NH प्रतिक्रिया करता है3 बोरॉन ट्राइफ्लोराइड BF. के साथ3, नाइट्रोजन दो इलेक्ट्रॉनों के साथ सीधे बोरॉन से बंध जाता है, जिसमें साझा करने के लिए कोई इलेक्ट्रॉन उपलब्ध नहीं होता है। इस प्रकार, नाइट्रोजन और बोरॉन दोनों के संयोजकता कोश में 8 इलेक्ट्रॉन रह जाते हैं।
यह सभी देखें कार्बनिक और अकार्बनिक यौगिक.
इंटरमॉलिक्युलर लिंक
अणु उन बलों के माध्यम से जुड़ते हैं जो तरल या ठोस अवस्था में पदार्थ बनाना संभव बनाते हैं।
द्विध्रुवीय-द्विध्रुवीय बंध या बल
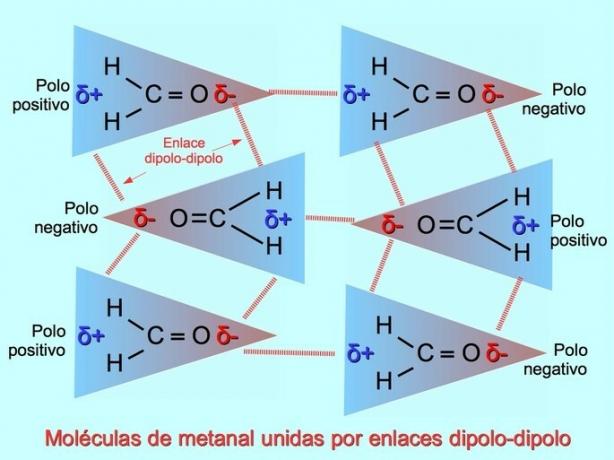
जब नकारात्मक ध्रुव सकारात्मक ध्रुवों की ओर आकर्षित होते हैं और इसके विपरीत ध्रुवीय अणुओं के बीच कमजोर अंतर-आणविक बंधन स्थापित किए जा सकते हैं। उदाहरण के लिए, मेथनल एच2सी = ओ एक ध्रुवीय अणु है, जिसमें ऑक्सीजन पर आंशिक नकारात्मक चार्ज और हाइड्रोजन पर आंशिक सकारात्मक चार्ज होता है। एक मेथैनल अणु का सकारात्मक पक्ष दूसरे मेथैनल अणु के नकारात्मक पक्ष को आकर्षित करता है।
हाइड्रोजन बांड या बांड
हाइड्रोजन बांड या हाइड्रोजन बांड एक बंधन है जो अणुओं के बीच स्थापित होता है। यह तब होता है जब अणु में हाइड्रोजन एक ऑक्सीजन, नाइट्रोजन या फ्लोरीन से सहसंयोजक रूप से बंधा होता है। ऑक्सीजन, नाइट्रोजन और फ्लोरीन उच्च वैद्युतीयऋणात्मकता वाले परमाणु हैं, इसलिए वे इलेक्ट्रॉनों को अधिक मजबूती से आकर्षित करते हैं जब वे उन्हें एक और कम विद्युतीय परमाणु के साथ साझा करते हैं।
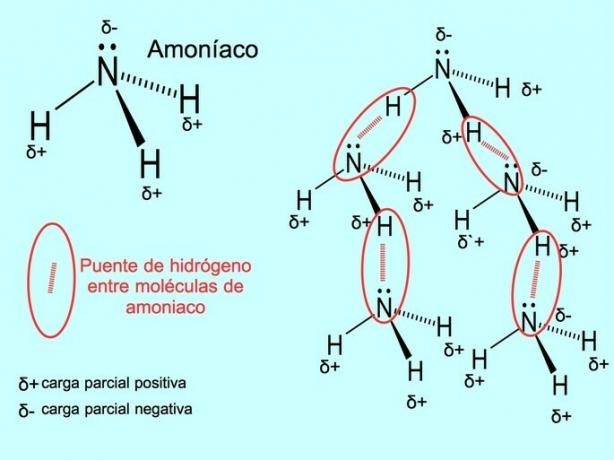
पानी के अणुओं के बीच हाइड्रोजन बांड होते हैं H2हे और अमोनिया NH3 जैसा कि चित्र दिखाता है:
आपको देखने में रुचि हो सकती है:
- परमाणु और अणु.
- कार्बनिक और अकार्बनिक यौगिकों के उदाहरण.
- धातु और अधातु
संदर्भ
जुमदहल, एस.एस., जुमदहल, एस.ए. (2014) रसायन विज्ञान। नौवां संस्करण। ब्रूक्स / कोल। बेलमोंट।
कॉमन्स, सी।, कॉमन्स, पी। (२०१६) हेनमैन केमिस्ट्री १। 5 वां संस्करण। पियर्सन ऑस्ट्रेलिया। मेलबर्न।


