आइसोटोप की मुख्य विशेषताएं Main

छवि: ग्रह
हमारे ग्रह को बनाने वाले सभी पदार्थ परमाणुओं से बने हैं। लेकिन सभी परमाणु समान नहीं होते हैं, विभिन्न तत्वों के परमाणुओं में प्रोटॉन, न्यूट्रॉन और इलेक्ट्रॉनों की संख्या अलग-अलग होती है। कभी-कभी इनकी संख्या उपपरमाण्विक कण समान नहीं हैं, संतुलित नहीं हैं, और प्रजातियां जैसे आइसोटोप. समस्थानिक एक ही तत्व के परमाणु होते हैं (उदाहरण के लिए, हाइड्रोजन) लेकिन उनमें न्यूट्रॉन की संख्या समान नहीं होती है। यह "असंतुलन" का कारण बनता है आइसोटोप की विशेषताएं एक ही तत्व के बराबर नहीं हैं। एक शिक्षक के इस पाठ में हम इन सभी विशेषताओं को विस्तार से देखेंगे। हमने शुरू किया!
सूची
- एक आइसोटोप क्या है?
- समस्थानिकों की परमाणु विशेषताएं
- समस्थानिकों का एक जिज्ञासु अनुप्रयोग: समस्थानिक अंकन
- एक ही तत्व के समस्थानिकों के लक्षण
एक आइसोटोप क्या है?
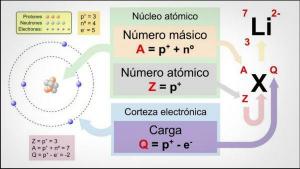
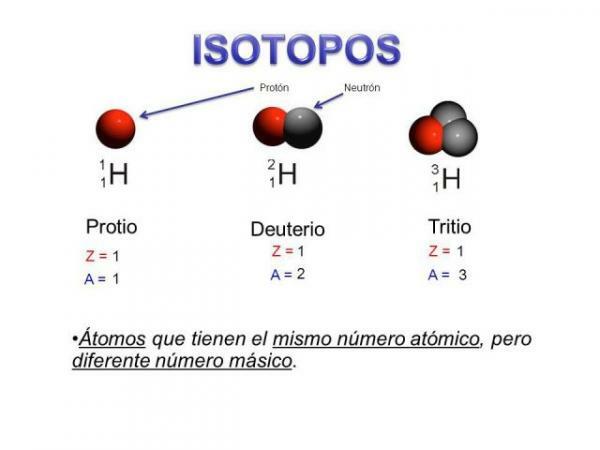
आइसोटोप की विशेषताओं के बारे में बात करने से पहले, यह समझना महत्वपूर्ण है कि इसमें क्या शामिल है। उप - परमाणविक कण. हम कह सकते हैं कि आइसोटोप क्या हैं परमाणुओं के "उपसमूह" हैं: वो हैं परमाणुओं एक ही तत्व का लेकिन वह कुछ चीजों में भिन्न होता है।
आइसोटोप हैं प्रोटॉन की समान संख्या वाले दो परमाणु (समान परमाणु क्रमांक), परंतु न्यूट्रॉन की विभिन्न संख्या (विभिन्न परमाणु द्रव्यमान)। एक ही तत्व के समस्थानिकों को आमतौर पर उस तत्व के नाम के साथ नाम दिया जाता है जिसके बाद उसका परमाणु द्रव्यमान होता है। यह सर्वविदित है औरएल कार्बन चौदह (C14), जिसका उपयोग जीवाश्मों की आयु निर्धारित करने के लिए किया जाता है लेकिन कार्बन के अन्य समस्थानिक होते हैं जैसे कार्बन 12 और कार्बन 13, जो कार्बन के अन्य समस्थानिकों जैसे कार्बन 8 या कार्बन की तुलना में अधिक स्थिर हैं कार्बन 22.
हमारे मामले में, ये सभी परमाणु कार्बन परमाणु हैं, इसलिए इनकी परमाणु संख्या 6 (Z = 6) है लेकिन कार्बन 12. है ("सामान्य" कार्बन) का परमाणु भार 12 बनाम कार्बन 14 का परमाणु भार 14 या 8 कार्बन का परमाणु भार होता है सी8.
विभिन्न समस्थानिकों के बीच ये अंतर परमाणुओं को अलग-अलग विशेषताओं, अन्य तत्वों के परमाणुओं के साथ व्यवहार, अर्ध-जीवन आदि का कारण बन सकते हैं।
छवि: आपके कार्य
समस्थानिकों की परमाणु विशेषताएं।
- परमाणु स्तर पर समस्थानिकों की पहली विशेषता यह है कि सभी समस्थानिक हैं एक ही तत्व के परमाणु.
- यह मुख्य विशेषता हमें दूसरी विशेषता की ओर ले जाती है: एक ही तत्व के सभी समस्थानिकों में समान परमाणु क्रमांक, यानी प्रोटॉन की समान संख्या।
- किसी तत्व के सभी समस्थानिकों में होता है प्रोटॉन की समान संख्या.
- एक ही तत्व के समस्थानिकों में अलग-अलग संख्या में न्यूट्रॉन होते हैं, अर्थात्, भिन्न द्रव्यमान संख्या या परमाणु द्रव्यमान.

छवि: ईएचयू
समस्थानिकों का एक जिज्ञासु अनुप्रयोग: समस्थानिक अंकन।
आइसोटोपिक लेबलिंग एक ऐसी तकनीक है जो आइसोटोप की दो बहुत ही महत्वपूर्ण विशेषताओं का उपयोग करती है: कि सभी आइसोटोप एक ही तरह से प्रतिक्रिया करते हैं रसायनिक प्रतिक्रिया और उनमें से कुछ के पास है रेडियोधर्मिता.
रासायनिक अभिक्रिया के दौरान दो या दो से अधिक पदार्थ, अभिकर्मक कहलाते हैं, वे विभिन्न संयोजनों, तथाकथित उत्पादों के परिणामस्वरूप अन्य विभिन्न पदार्थों को बनाने के लिए अपने परमाणुओं को मिलाते हैं। समस्थानिक अंकन एक तकनीक है जिसके द्वारा हम एक अभिकर्मक के रेडियोधर्मी समस्थानिक को प्रतिक्रिया में पेश कर सकते हैं, ताकि यह सामान्य तरीके से प्रतिक्रिया करेगा और हम इसे किसी भी समय रेडियोधर्मिता के लिए धन्यवाद कर सकते हैं कि उत्सर्जन
इस तकनीक के अन्य प्रकार हमें अभिकर्मक के विभिन्न समस्थानिकों की पहचान करने की अनुमति देते हैं मास स्पेक्ट्रोमेट्री या अवरक्त स्पेक्ट्रोस्कोपी।

छवि: स्लाइडप्लेयर
एक ही तत्व के समस्थानिकों के लक्षण।
पिछले खंड में देखी गई परमाणु विशेषताओं के परिणामस्वरूप, उसी तत्व के समस्थानिकों में अन्य प्रकार की विशेषताएं हो सकती हैं, जिनका वर्णन हम नीचे करेंगे।
- एक ही तत्व के समस्थानिक होते हैं अलग द्रव्यमान। भौतिक गुण जैसे घनत्व, जो एक ही तत्व के विभिन्न समस्थानिकों के लिए भिन्न होगा।
- कुछ रासायनिक गुण वे उस तत्व के प्रकार पर निर्भर करते हैं जो वह है, और इसलिए वे एक तत्व के विभिन्न समस्थानिकों के लिए भिन्न नहीं होंगे। एक उदाहरण है घुलनशीलता, क्या होगा लगातार एक तत्व के सभी समस्थानिकों के लिए।
- रासायनिक गुणों में उनकी समानता से निकटता से संबंधित समस्थानिकों की निम्नलिखित विशेषता है: एक ही तत्व के समस्थानिक रासायनिक प्रतिक्रियाओं में उसी तरह प्रतिक्रिया करते हैं. इसका मतलब यह है कि यदि कार्बन 12 परमाणु (सबसे सामान्य या "सामान्य" परमाणु) दो ऑक्सीजन परमाणुओं के साथ प्रतिक्रिया करता है कार्बन डाइऑक्साइड अणु बनाने के लिए, हम जानते हैं कि कार्बन के अन्य समस्थानिक भी हैं वे करेंगे। यह आइसोटोप और रेडियोआइसोटोप के कई व्यावहारिक अनुप्रयोगों के लिए एक बहुत ही महत्वपूर्ण संपत्ति है।
- किसी तत्व के समस्थानिक हो सकते हैं प्राकृतिक या कृत्रिम मूल. यदि विचाराधीन समस्थानिक प्रकृति में पाया जा सकता है, इसके निर्माण में मनुष्य के हाथ के हस्तक्षेप के बिना, हम एक समस्थानिक का सामना कर रहे हैं प्राकृतिक जबकि यदि इसे परमाणु रिएक्टरों, कण त्वरक या रेडियोआइसोटोप जनरेटर में बनाया गया है तो हम कहते हैं कि यह है कृत्रिम। एक ही तत्व में प्राकृतिक और कृत्रिम समस्थानिक हो सकते हैं।
- आइसोटोप हो सकते हैं रेडियोधर्मी या गैर-रेडियोधर्मी. रेडियोधर्मी समस्थानिक वे होते हैं जिनमें ऊर्जा की अधिकता होती है, जिसे परमाणु अस्थिर अवस्था से अधिक स्थिरता में जाने के लिए समाप्त कर देता है।
- पिछली विशेषताओं के संबंध में हम कह सकते हैं कि समस्थानिक रेडियोधर्मी उनके पास एक परिवर्तनशील जीवन काल. जीवनकाल वह समय है जो आइसोटोप को विघटित होने में लगता है, अर्थात उस अतिरिक्त ऊर्जा को रोकने के लिए जो इसे अस्थिर बनाती है। ऐसे रेडियोधर्मी समस्थानिक हैं जो बहुत अस्थिर होते हैं और उनका जीवनकाल सेकंड का होता है जबकि अन्य को विघटित होने और अधिक स्थिर समस्थानिक बनने में घंटों या साल भी लगते हैं। आम तौर पर, कृत्रिम रूप से बनाए गए परमाणुओं में प्राकृतिक की तुलना में बहुत कम जीवन या क्षय का समय होता है।
अगर आप इसी तरह के और आर्टिकल पढ़ना चाहते हैं आइसोटोप के लक्षण, हम अनुशंसा करते हैं कि आप हमारी श्रेणी दर्ज करें परमाणु.
ग्रन्थसूची
- ब्रिसेनो वी, जी। (एस.एफ) आइसोटोप।
- बेलमोंटे, ए. (15 मई 2019)। परमाणु के गुण।
- विकिपीडिया (22 अक्टूबर 2019)। आइसोटोप।