प्रबल और दुर्बल अम्ल और क्षार के बीच अंतर (उदाहरण के साथ)
रसायन विज्ञान में अम्लों और क्षारों का वर्गीकरण जलीय माध्यम में इन पदार्थों के आयनीकरण बल पर निर्भर करता है। ए) हाँ:
- ए अम्ल और क्षार प्रबल होते हैं जब वे पूरी तरह से आयनित हो जाते हैं, यानी आयनीकरण प्रक्रिया में वे पूरी तरह से धनायनों या सकारात्मक आयनों में और आयनों या नकारात्मक आयनों में बदल जाते हैं।
- दूसरी ओर, अम्ल और क्षार दुर्बल होते हैं जब वे पानी में आंशिक रूप से आयनित होते हैं, अर्थात, समाधान में धनायनों का अनुपात, आयनों का एक और अनुपात और असंबद्ध अणुओं का एक अन्य अनुपात होगा।
| प्रबल अम्ल और क्षार | कमजोर अम्ल और क्षार | |
|---|---|---|
| परिभाषा | वे पदार्थ जो विलयन में पूर्णतः आयनित हो जाते हैं। | वे पदार्थ जो विलयन में आंशिक रूप से आयनित होते हैं। |
| आयनीकरण | पूर्ण | आंशिक |
| जलीय घोल में तत्व | समान सांद्रता में धनायन और आयन। | विभिन्न अनुपातों में धनायन, आयन और अणु। |
| आयनीकरण स्थिरांक | ऊपर उठाया | थोड़ा |
| उदाहरण |
|
|
प्रबल अम्ल और क्षार
ए अम्ल या क्षार तब प्रबल होते हैं जब जलीय माध्यम में वे पूर्णतः वियोजित हो जाते हैंदूसरे शब्दों में, आयनीकरण प्रक्रिया पूरी हो गई है और समाधान में आयनों और धनायनों की समान सांद्रता होगी।
आप अम्ल और प्रबल क्षारक को कैसे आयनित करते हैं?
एक प्रबल अम्ल, जैसे हाइड्रोक्लोरिक अम्ल HCl, निम्न प्रकार से आयनित होता है:
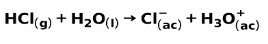
एक मजबूत आधार, जैसे सोडियम हाइड्रॉक्साइड NaOH, निम्नलिखित तरीकों से आयनित होता है:
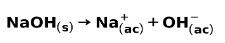
प्रबल अम्लों के उदाहरण और उनके सूत्र
| मजबूत अम्ल | सूत्र |
|---|---|
| हाइड्रोक्लोरिक एसिड | एचसीएल |
| सल्फ्यूरिक एसिड | एच2दप4 |
| नाइट्रिक एसिड | एचएनओ3 |
| हाइड्रोब्रोमिक एसिड | एचबीआर |
| परक्लोरिक तेजाब | एचसीएलओ4 |
| क्रोमिक एसिड | एच2सीआरओ4 |
| टेट्राफ्लोरोबोरिक एसिड | एचबीएफ4 |
मजबूत आधारों और उनके सूत्रों के उदाहरण
| मजबूत आधार | सूत्र |
|---|---|
| सोडियम हाइड्रॉक्साइड | NaOH |
| लिथियम हाइड्रॉक्साइड | LiOH |
| पोटेशियम हाइड्रोक्साइड | कोह |
| रुबिडियम हाइड्रॉक्साइड | आरबीओएच |
| सीज़ियम हाइड्रॉक्साइड | सीएसओएच |
| कैल्शियम हाइड्रॉक्साइड | सीए (ओएच)2 |
| बेरियम हाइड्रॉक्साइड | बा (ओएच)2 |
| स्ट्रोंटियम हाइड्रॉक्साइड | सीनियर (ओएच)2 |
| एल्युमिनियम हाइड्रॉक्साइड | अल (ओएच)3 |
आपको और देखने में रुचि हो सकती है अम्ल और क्षार के उदाहरण.
कमजोर अम्ल और क्षार
ए जलीय घोल में आंशिक रूप से आयनित होने पर अम्ल या क्षार कमजोर होता हैयानी विलयन में आयन और अआयनीकृत अणु होते हैं।
आप अम्ल और दुर्बल क्षारक को कैसे आयनित करते हैं?
एक कमजोर अम्ल, जैसे एसिटिक अम्ल CH3COOH, निम्न प्रकार से आयनित होता है:
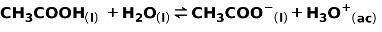
इस प्रतिक्रिया का संतुलन दो तीरों द्वारा विपरीत दिशाओं में व्यक्त किया जाता है।
जब एक कमजोर एसिड अलग हो जाता है या आयनित हो जाता है, तो समाधान में मौजूद प्रजातियों के बीच एक संतुलन स्थापित हो जाता है; इसे a. द्वारा व्यक्त किया जा सकता है आयनीकरण स्थिरांकखट्टा:
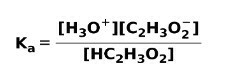
आयनीकरण स्थिरांक अभिकारकों की सांद्रता के गुणन पर उत्पादों की सांद्रता के गुणन के बीच के अनुपात से अधिक कुछ नहीं है।
एक कमजोर आधार, जैसे NH अमोनिया3, निम्न प्रकार से आयनित होता है:
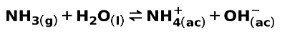
जब एक कमजोर आधार अलग हो जाता है या आयनित हो जाता है, तो समाधान में मौजूद प्रजातियों के बीच एक संतुलन स्थापित हो जाता है; इसे a. द्वारा व्यक्त किया जा सकता है आधार आयनीकरण स्थिरांक:
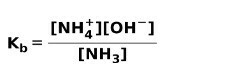
आप के बीच अंतर जानने में रुचि हो सकती है अम्ल और क्षार.
कमजोर अम्लों के उदाहरण उनके सूत्र और अम्ल आयनीकरण स्थिरांक K. के साथसेवा मेरे
| कमजोर अम्ल | सूत्र | आयनीकरण स्थिरांक |
|---|---|---|
| फॉर्मिक एसिड | एच2सीओ2 | 1.77 x 10-4 |
| सिरका अम्ल | एच3सीसीओएच | 1.75 x 10-5 |
| हाइड्रोसायनिक एसिड | HOCN | 3.30 x 10-4 |
| हाइड्रोजन साइनाइड | एचसीएन | 6.20 x 10-10 |
| हाइपोक्लोरस तेजाब | एचओसीएल | 3.50 x 10-8 |
| नाइट्रस तेजाब | एचएनओ2 | 4.00 x 10-4 |
| दुग्धाम्ल | कोर्ट3एच5या3 | 1.40 x 10-4 |
| कार्बोनिक एसिड | एच2सीओ3 |
4.30 x 10-7 5.60 x 10-11 |
| बोरिक एसिड | एच3बो3 |
5.80 x 10-10 1.80 x 10-13 3.00 x 10-14 |
कमजोर आधारों के उदाहरण उनके सूत्र और मूल आयनीकरण स्थिरांक K. के साथख
| कमजोर आधार | सूत्र | आयनीकरण स्थिरांक |
|---|---|---|
| अमोनिया | राष्ट्रीय राजमार्ग3 | 1.75 x 10-5 |
| मिथाइलमाइन | चौधरी3राष्ट्रीय राजमार्ग2 | 4.38 x 10-4 |
| ethylamine | सी2एच5राष्ट्रीय राजमार्ग2 | 5.60 x 10-4 |
| रंगों का रासायनिक आधार | सी6एच5राष्ट्रीय राजमार्ग2 | 3.80 x 10-10 |
| पिरिडीन | सी5एच5नहीं | 1.70 x 10-9 |
| बेंजाइलमाइन | सी7एच9नहीं | 2.20 x 10-5 |
| सोडियम बाइकार्बोनेट | नाहको | 2.00 x 10-4 |
आपको इसके बारे में और जानने में रुचि हो सकती है अम्ल और क्षार के लक्षण