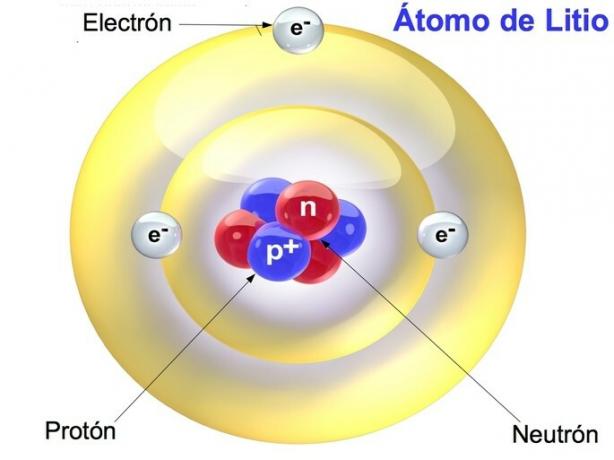
प्रोटॉन, न्यूट्रॉन और इलेक्ट्रॉन
प्रोटॉन, न्यूट्रॉन और इलेक्ट्रॉन ऐसे कण हैं जो परमाणु बनाते हैं, जो तत्व का सबसे छोटा हिस्सा है। ये कण रासायनिक तत्वों की विशेषताओं और गुणों को निर्धारित करते हैं।
प्रोटॉन और न्यूट्रॉन परमाणु नाभिक में केंद्रित होते हैं, जबकि इलेक्ट्रॉनों को क्रस्ट या परमाणु की परिधि में वितरित किया जाता है। एक परमाणु में इलेक्ट्रॉनों और प्रोटॉन की संख्या समान होती है, जबकि न्यूट्रॉन की संख्या परिवर्तनशील होती है।
इसके बाद, हम प्रोटॉन, न्यूट्रॉन और इलेक्ट्रॉनों के बीच एक तुलनात्मक तालिका प्रस्तुत करते हैं।
| प्रोटोन | न्यूट्रॉन | इलेक्ट्रॉन | |
|---|---|---|---|
| परिभाषा | धनात्मक आवेश का उपपरमाण्विक कण | उपपरमाण्विक तटस्थ आवेश कण | ऋणात्मक रूप से आवेशित उपपरमाण्विक कण |
| भार | सकारात्मक +1 |
तटस्थ 0 |
नकारात्मक -1 |
| प्रतीक | पी+ | नहीं0 | तथा- |
| परमाणु में स्थान | कोर | कोर | परिधीय कक्षक |
| मास (किलो) | 1,673 x 10--27किलोग्राम | 1,675 x 10--27किलोग्राम | 9,109 x 10--31किलोग्राम |
| प्रोटॉन की तुलना में द्रव्यमान (amu) | 1 | 1 | 0,0005 |
| मौलिक कण | 3 क्वार्क: 2 यू और 1 डी | 3 क्वार्क: 2 डी और 1 यू | 1 लेप्टन |
| खोजकर्ता (वर्ष) | तथा। रदरफोर्ड (1911) | जे। चैडविक (1931) | जे जे थॉमसन (1897) |
एक प्रोटॉन क्या है?
प्रोटॉन एक परमाणु के नाभिक में पाए जाने वाले धनात्मक आवेशित कण होते हैं। किसी तत्व के प्रत्येक परमाणु में प्रोटॉन की एक निश्चित संख्या होती है, जो इसकी परमाणु संख्या या Z निर्धारित करती है। इस प्रकार, हाइड्रोजन में एक प्रोटॉन होता है और Z बराबर 1 होता है।
प्रोटॉन का द्रव्यमान 1.673 x 10. है-27 किलो, जो 1 परमाणु द्रव्यमान इकाई या एमू का प्रतिनिधित्व करता है (अंग्रेजी में इसके परिवर्णी शब्द के लिए परमाण्विक भार इकाई).
1911 में, अर्नेस्ट रदरफोर्ड ने पाया कि एक परमाणु का नाभिक छोटा और धनावेशित होता है, इसलिए प्रोटॉन की अवधारणा।
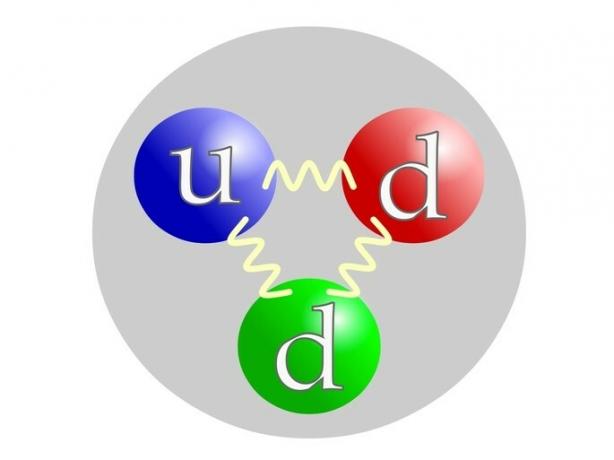
प्रोटॉन प्राथमिक कणों से बना होता है जिन्हें क्वार्क कहा जाता है क्वार्क: 2 क्वार्क यू (प्रति .) यूपी= ऊपर) और 1 क्वार्टक d (by .) नीचे= नीचे)।

परमाणु के प्रोटॉन की गणना कैसे करें?
एक परमाणु में प्रोटॉन की संख्या उसके परमाणु क्रमांक से निर्धारित की जा सकती है, जो कि आवर्त सारणी में स्थिति संख्या है।
उदाहरण के लिए, गोल्ड एयू की परमाणु संख्या = 79 है, जिसका अर्थ है कि सोने के नाभिक में 79 प्रोटॉन होते हैं।
न्यूट्रॉन क्या है?
न्यूट्रॉन एक परमाणु के नाभिक में प्रोटॉन के साथ पाए जाने वाले कण होते हैं। उन्हें पत्र द्वारा निरूपित किया जाता है नहीं और वे न्यूट्रल चार्ज हैं। एकमात्र तत्व जिसमें न्यूट्रॉन नहीं है वह हाइड्रोजन है।
न्यूट्रॉन का द्रव्यमान प्रोटॉन के समान होता है, इसलिए प्रोटॉन और न्यूट्रॉन के द्रव्यमान का योग किसी तत्व के परमाणु द्रव्यमान को निर्धारित करता है।
वे परमाणु जिनकी परमाणु संख्या समान होती है, लेकिन न्यूट्रॉन की संख्या भिन्न होती है, समस्थानिक कहलाते हैं। उदाहरण के लिए, ड्यूटेरियम हाइड्रोजन का एक समस्थानिक है, जिसके नाभिक में एक न्यूट्रॉन और एक प्रोटॉन होता है।
अंग्रेजी भौतिक विज्ञानी जेम्स चैडविक ने 1931 में इस उप-परमाणु कण की खोज की, जिसका द्रव्यमान प्रोटॉन के करीब था, लेकिन एक तटस्थ विद्युत आवेश के साथ, यही कारण है कि इसे न्यूट्रॉन कहा जाता था।
न्यूट्रॉन क्वार्क द्वारा प्रोटॉन की तरह बना होता है: 1 क्वार्क u (by .) यूपी= ऊपर) और 2 क्वार्टक d (by .) नीचे= नीचे)।
परमाणु के न्यूट्रॉन की गणना कैसे करें?
हम एक परमाणु में न्यूट्रॉन की संख्या की गणना कर सकते हैं यदि हम इसका परमाणु द्रव्यमान और इसकी परमाणु संख्या Z जानते हैं। हम पहले से ही जानते हैं कि परमाणु संख्या Z प्रोटॉन की संख्या है और परमाणु द्रव्यमान प्रोटॉन और न्यूट्रॉन का योग है जो एक परमाणु के पास होता है।
उदाहरण के लिए, ऑक्सीजन का परमाणु द्रव्यमान 16 है और Z 8 है। ऑक्सीजन में प्रोटॉन की संख्या परमाणु द्रव्यमान शून्य से Z के बराबर होती है:
16 - 8 = 8 न्यूट्रॉन
एक इलेक्ट्रॉन क्या है?
इलेक्ट्रॉन परमाणु के कण होते हैं जो नाभिक के चारों ओर बादल में होते हैं। जबकि प्रोटॉन और न्यूट्रॉन नाभिक में केंद्रित होते हैं, इलेक्ट्रॉनों को बाहर की परतों में वितरित किया जाता है।
एक परमाणु के सबसे बाहरी कोश में मौजूद इलेक्ट्रॉन एक परमाणु से दूसरे परमाणु में कूद सकते हैं। यह परमाणु को एक अलग विद्युत आवेश देता है; उदाहरण के लिए, यदि कोई परमाणु एक इलेक्ट्रॉन प्राप्त करता है, तो उसका आवेश ऋणात्मक होगा, जबकि यदि वह एक इलेक्ट्रॉन खोता है, तो आवेश धनात्मक होगा।
आयनों में ऐसा होता है, यानी एक परमाणु जो एक या अधिक इलेक्ट्रॉनों को प्राप्त करता है या खो देता है। उदाहरण के लिए, क्लोरीन में 17 इलेक्ट्रॉन होते हैं, लेकिन यह Cl क्लोराइड आयन बनने के लिए एक इलेक्ट्रॉन प्राप्त कर सकता है।-, 18 इलेक्ट्रॉनों और एक नकारात्मक चार्ज के साथ।
इलेक्ट्रॉन की खोज 1897 में जे.जे. थॉमसन, "किशमिश का हलवा" के परमाणु मॉडल के समान।
इलेक्ट्रॉन एक प्राथमिक कण से बना है जो लेप्टन है।
एक इलेक्ट्रॉन का द्रव्यमान प्रोटॉन और न्यूट्रॉन के द्रव्यमान से लगभग 2000 गुना छोटा होता है। मान लीजिए कि एक प्रोटॉन या न्यूट्रॉन 10 पाउंड की बॉलिंग बॉल के आकार का होता है, तो इलेक्ट्रॉन एक छोटे संगमरमर के आकार का होगा।
इसलिए, परमाणु द्रव्यमान की गणना करते समय एक परमाणु में इलेक्ट्रॉनों का द्रव्यमान नगण्य होता है।
परमाणु के इलेक्ट्रॉनों की गणना कैसे करें?
एक तटस्थ परमाणु में इलेक्ट्रॉनों की संख्या उस परमाणु में प्रोटॉन की संख्या के बराबर होती है। उदाहरण के लिए, Au सोने में 79 प्रोटॉन होते हैं, इसलिए इसमें 79 इलेक्ट्रॉन होंगे।
आपको यह देखने में भी रुचि हो सकती है:
- धनायन और ऋणायन
- परमाणु और अणु.
संदर्भ
मायर्स, आर.एल. (2005) भौतिकी की मूल बातें। ग्रीनवुड।
पीक, बी.एम. (1989) इलेक्ट्रॉन, प्रोटॉन और न्यूट्रॉन की खोज। जे. रासायनिक शिक्षा 66: 738। डीओआई: १०.१०२१ / एड०६६पी७३८