A PERIODIKUS TÁBLÁZAT csoportjainak jellemzői
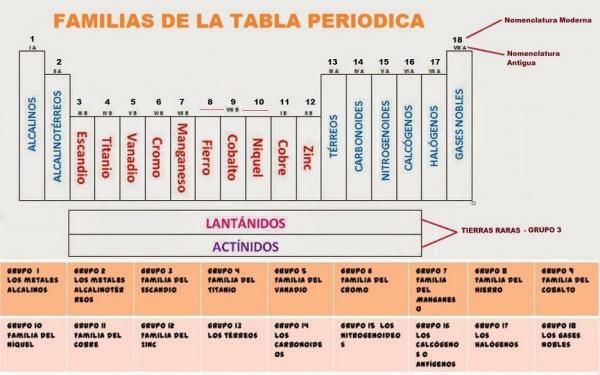
Kép: Természettudományok
A periódusos rendszer rendeljen mindent kémiai elemek eddig ismert. Bár másképp tűnhet, ezek az elemek gondosan érvényes szabályok szerint vannak elrendezve méretétől a reaktivitásáig más tulajdonságokon, például az utolsó héjon lévő elektronok számán keresztül haladva atom.
A periódusos rendszer lényegében egy sorokból és oszlopokból álló táblázat. A sorok, amelyek formában vannak elrendezve vízszintes, az ún időszakok amíg a oszlopokfüggőlegesen a csoportok. De mi határozza meg, hogy két elem ugyanabban a csoportban vagy más csoportban van? Ebben a TANÁR leckében látni fogjuk a a periódusos rendszer csoportjainak jellemzői.
Index
- Melyek a periódusos rendszer csoportjai? Hány csoport van a periódusos rendszerben?
- Az 1. csoport jellemzői (IA)
- 2. csoport (IIA) jellemzői
- A 3–12. Csoport (B) jellemzői
- A 13. csoport jellemzői (IIIA)
- A 14. csoport jellemzői (HÉA)
- A 15. csoport jellemzői (VA)
- A 16. csoport jellemzői (VIA)
- A 17. csoport jellemzői (VIIA)
- A 18. csoport jellemzői (VIIIA)
Melyek a periódusos rendszer csoportjai? Hány csoport van a periódusos rendszerben?
Mielőtt elkezdenénk beszélni a csoportok jellemzőiről a periódusos rendszerben, tudnunk kell, miből áll ez a rendszer. Az eddig felfedezett kémiai elemek tanulmányozásához Mendelejev ezt a mintát a táblázatban találta ki: periódusos rendszer. Vízszintes sorok és függőleges oszlopok jelennek meg a periódusos rendszerben. A periódusos rendszer oszlopait csoportoknak és ugyanazon csoport elemeinek nevezzük (ugyanabban a csoportban) oszlop) ugyanazokkal a vegyértékekkel és hasonló kémiai tulajdonságokkal bír, mint amelyeket a következőkben láthatunk szakaszok.
Jelenleg a periódusos rendszer 18 csoportból áll. Mindegyik csoporthoz van hozzárendelve egy kód és bizonyos esetekben egy közös név.
A 18 periódusos csoport Ők:
- 1. csoport, IA vagy alkálifémek. Lítiumból (Li), nátriumból (Na), káliumból (K), rubídiumból (Rb), céziumból (Cs) és franciumból (Fr)
- 2., II A csoport vagy alkáliföldfémek. Berilliumból (Be), magnéziumból (Mg), kalciumból (Ca), stronciumból (Sr), báriumból (Ba) és rádiumból (Ra) áll.
- 3. csoport, IIIB vagy Escandio család. Összetétele: Scandium (Sc), ittrium (Y), Lutetium (Lu), Lawrencio (Lr), Lanthanum (La), Actinium (Ac).
- 4., IV B vagy Titán család. A következő elemekből áll: titán (Ti), cirkónium (Zr), hafnium (Hf) és rutherfordium (Rf)
- 5. csoport, VB vagy Vanadium család. Ezt a csoportot az elemek alkotják: vanádium (V), nióbium (Nb), tantál (Ta) és dubnium (Db).
- 6. csoport, VIB vagy krómcsalád. A 6. csoportba tartoznak: króm (Cr), molibdén (Mo), Wolfram vagy Tungsten (W) és Seaborgium (Sg).
- 7., VIIB. Csoport vagy mangáncsalád. A 7. csoportot a következők alkotják: mangán (Mn), technécium (Tc), rénium (Re) és Bohrio (Bh).
- 8., VIIIB. Csoport vagy vascsalád. A 8. csoportba tartoznak: vas (Fe), ruténium (Ru), ozmium (Os) és Hassium (Hs).
- 9. csoport, IXB vagy kobalt család. A 9. csoport a következőkből áll: kobalt (Co), ródium (Rh), irídium (Ir) és Meitnerium (Mt).
- 10. csoport, XB vagy nikkel család. Ez a csoport a következőkből áll: nikkel (Ni), Palladium (Pd), Platinum (Pt) és Darmstadium (Ds) (korábban Ununnilio (Uun).
- 11. csoport, XIB, réz vagy fémverő család. Ebbe a csoportba tartoznak: Réz (Cu), Ezüst (Ag), Arany (Au) és Roentgenium (Rg).
- 12. csoport, XIIB vagy cink család. A 12. csoportot a következők alkotják: cink (Zn), kadmium (Cd), higany (Hg) és Copernicium (Cn).
- 13. csoport, IIIA vagy Boron család. Bór (B), alumínium (Al), gallium (Ga), indium (In), tallium (Tl) és nihónium (Nh) alkotta.
- 14. csoport, IVA, szén vagy karbon család. A 14. csoportot az elemek alkotják: szén (C), szilícium (Si), germánium (Ge), ón (Sn), ólom (Pb) és phlerovium (Fl).
- 15. csoport, V5, a pnicógenos vagy a nitrogén-oxid család. A következőkből áll: nitrogén (N), foszfor (P), arzén (As), antimon (Sb), bizmut (Bi) és muscovio (Mc).
- 16. csoport, VIA, amfogének, kalkogének vagy az oxigéncsalád. A következőkből áll: oxigén (O), kén (S), szelén (Se), Tellúr (Te), polónium (Po) és Livermorio (Lv).
- 17. csoport, VIIA vagy halogének. Ez a csoport a következőkből áll: fluor (F), klór (Cl), bróm (Br), jód (I), asztát (At) és tenesz (Ts).
- 18. csoport, VIIIA vagy nemesgázok. Csoport alkotta: hélium (He), neon (Ne), argon (Ar), kripton (Kr), xenon (Xe), radon (Rn) és oganesson (Og).
A kémiai elemek második osztályozása
A kémiai elemeken belül megtalálhatjuk a periódusos rendszer csoportjainak második osztályozását.
- Az 1., 2., 13., 14., 15., 16., 17. és 18. csoport a fő elemek vagy csoportok A csoportjába tartozik
- Míg a 3., 4., 5., 6., 7., 8., 9., 10., 11. és 12. csoport a B vagy átmeneti fémek csoportjába tartozik.
Ezen kémiai elemek többsége megtalálható a természetben, akár tisztán, akár más vegyületekkel vagy elemekkel keverve. Másrészről, némelyikük, például a Muszkovik, mesterséges elemek, amelyeket az ember laboratóriumokban hozott létre, és amelyeket soha nem láttak a természetben. Itt részletesebben felfedezünk hogyan szerveződik a periódusos rendszer.
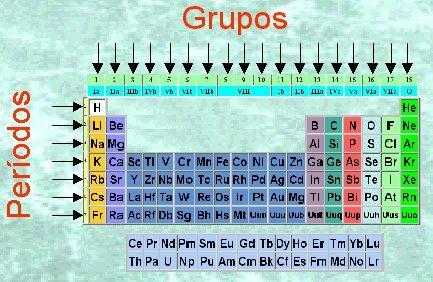
Kép: Periódusos rendszer
Az 1. csoport jellemzői (IA)
A periódusos rendszerben szereplő csoportok jellemzőinek elemzésével kezdjük, a következőkről beszélünk 1. csoport elemei amelyek a következők jellemzők:
- Oxidációs szám +1. Ezért nagyon elektropozitívak és alacsony az ionizációs energiájuk, mivel könnyen elveszítik ezt az elektront.
- Az elektronikus konfiguráció ns1
- Ezek a kémiailag leginkább reaktív kémiai elemek, ezért természetükben nem elszigeteltek, hanem sók formájában.
- Lágy, kis sűrűségű fémek, alacsony olvadásponttal. Vágásuk vagy megolvasztásukkor ezüst színük és fémes fényük figyelhető meg.
- Hajlékony, alakítható és jó hő- és villamosenergia-vezetők.
- Vízzel reagálva hidroxidokat képeznek

Kép: Slideshare
2. csoport (IIA) jellemzői.
A 2. csoport elemei a következő jellemzőkkel rendelkeznek:
- Oxidációs szám +2
- Az elektronikus konfiguráció ns2
- Alacsony ionizációs energia, amely egyre kevesebb lesz, amikor az ember leereszkedik a csoportba. Ezért a berillium kivételével mindegyik egyértelműen ionos vegyületeket képez.
- Könnyen reagálnak a halogénnel és ionos sókat képeznek.
- Alacsony sűrűségűek, színesek és puhák
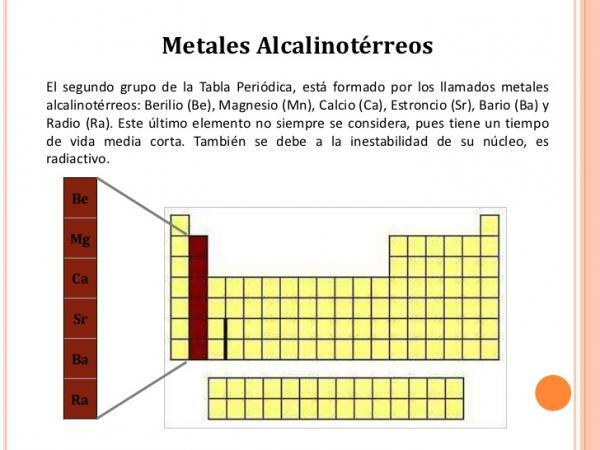
Kép: Slideshare
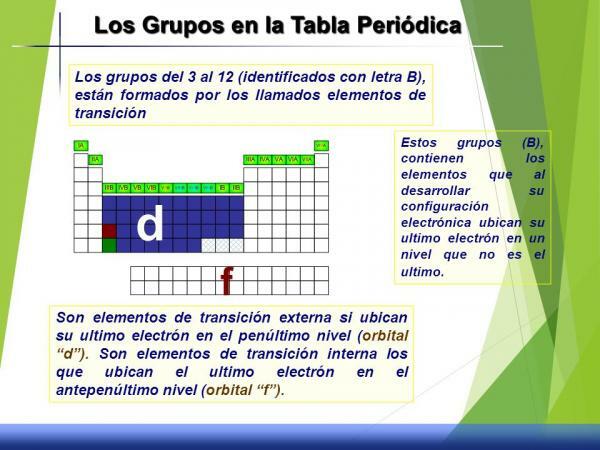
A 3–12. Csoport (B) jellemzői.
Ezt a csoportkészletet hívjuk átmenetifémek vagy blokk d mivel ha elektronikus konfigurációját nézzük, akkor a d pálya részben tele van elektronokkal.
Közepes magatartásuk van, vagyis anélkül, hogy nagyon reaktívak lennének, nem túl tehetetlenek (kevés reaktánsok), nincsenek jellemző oxidációs állapotuk, állapotuk, sűrűségük vagy tulajdonságaik egyértelműen meghatározott.
Kép: Slideplayer
A 13. csoport jellemzői (IIIA)
13. csoportAnnak ellenére, hogy jellemzői tekintetében is meglehetősen közbenső, azt látjuk, hogy valamivel jobban definiált, mint az előzőek. A 13. csoport elemei:
- Oxidációs állapotuk +3, és bizonyos elemekben +1 is
- Általában nagyon magas olvadáspontú metalloidok
- Hajlamosak jellegzetes nemfémes tulajdonságokra

Kép: Slideshare
A 14. csoport jellemzői (HÉA)
A karbid elemek Emellett meglehetősen változatosak és nagyon különleges tulajdonságokkal rendelkeznek: Ahogy megyünk lefelé a csoportban, az elemek több fémes tulajdonságokkal rendelkeznek; a szén nemfém, a szilícium és a germánium félmetál, és a csoporton belül az ón és az ólom fémek.

Kép: Slideserve
A 15. csoport jellemzői (VA)
A periódusos rendszer csoportjainak jellemzőivel folytatva most a csoport 15 elem:
- Magas hőmérsékleten nagyon reaktívak. Klasszikus példa a nitrogén reakciója oxigénnel és hidrogénnel, amely csak magas hőmérsékleten vagy nyomáson fordul elő.
- 5 vegyértékű elektronjuk van.
- A kovalens kötések általában N és P, az ionos kötések az Sb és Bi és más elemek között jönnek létre.

Kép: Slideplayer
A 16. csoport jellemzői (VIA)
A. Jellemzői csoport 16 elem Ők:
- Hat vegyérték elektronjuk van (az utolsó héj s2o4)
- Tulajdonságai nem fémetől fémesig változnak, mivel atomszáma növekszik.
- Atomi térfogata, sűrűsége, az anion sugara, valamint az olvadás- és forráspontok nőnek, ahogy haladunk a csoportban.
- Fajlagos hője és a hidrid képződésének hője csökken, ahogy a csoportban lefelé haladunk.

Kép: Slideplayer
A 17. csoport jellemzői (VIIA)
A. Jellemzői 17. csoport vagy halogének a következő:
- Egyértékű elemek, vagyis csak egy vegyérték számuk van. Halogénekben a vegyérték értéke -1.
- Általában fémekkel kombinálva halogenideket, halogenideket vagy hidrideket képeznek.
- Kevés affinitásuk van az oxigénhez, ezért nem oxidokat képeznek, hanem nagyon magas hőmérsékleten.

Kép: Slideplayer
A 18. csoport jellemzői (VIIIA)
Ezt a leckét a periódusos rendszer csoportjainak jellemzőiről úgy fejezzük be, hogy a következőkről beszélünk nemesgázok vagy a 18. csoport elemei amelyek a következő jellemzőkkel rendelkeznek:
- Bemutatják a gáz állapotát a természetben.
- Elektronikus rétegük vagy utolsó valens rétegük teljes, ezért nem túl reaktívak.
- Nagyon bőséges természetűek. A hidrogén után a hélium a legelterjedtebb elem az ismert univerzumban.
- Alacsony olvadás- és forráspontjuk van
- Negatív elektronikus affinitást mutatnak
- Néhányuk radioaktív, ami gazdasági szempontból nagyon fontos.

Kép: Slideplayer
Ha további hasonló cikkeket szeretne olvasni A periódusos rendszer csoportjainak jellemzői, javasoljuk, hogy adja meg a Az atom.
Bibliográfia
- Quimicas.net (2015. július) Vegyi elemek csoportjai. Felépült https://www.quimicas.net/2015/07/grupos-de-elementos-quimicos.html
- Pacheco, A (s.f) A periódusos rendszer csoportjai, azok leírása és jellemzői Felépült http://www.universidadcultural.com.mx/online/claroline/work/user_work.php? cmd = exDownload & authId = 7750 & assigId = 3 & workId = 131 & cidReset = true & cidReq = CIIS1_002
- Tudományterület (s.f) Periódusos rendszercsoportok helyreállítva https://www.areaciencias.com/quimica/familias-de-la-tabla-periodica.html