Különbség az endoterm reakciók és az exoterm reakciók között
A endoterm reakció hatalmat igényel, míg a exoterm reakció energiát szabadít fel. A kémiai reakciók ezen osztályozása figyelembe veszi az energia részvételét akár reagensként, akár termékként.
Az energia a munkavégzés vagy a hőtermelés képessége. Ne feledje, hogy a kémiai reakciók az atomok átrendeződését jelentik az anyagok között, megszakadva vagy kémiai kötéseket képezve. Általában ez a kémiai kötések kialakulása vagy megszakadása a rendszer energiájának változásával jár.
| Endoterm reakció | Exoterm reakció | |
|---|---|---|
| Meghatározás | Kémiai reakció, ahol az energia elnyelődik. | Kémiai reakció, ahol az energia hő formájában szabadul fel. |
| Az energia eredete | A környezetből | A rendszerről |
| Helyzeti energia | A reagensekben alacsonyabb, mint a termékekben. | Magasabb a reagensekben, mint a termékekben. |
| Termelés | Nem spontán | Spontán |
| Belső energiaváltozás | ΔE> 0; a belső energiaváltozás nagyobb, mint nulla. | AE <0; a belső energia változása nulla alatt van. |
| Hőfok | Csökken | Növeli |
| Példák | A fotoszintézis és általában a szintézis reakciói. | Égő gyufa, égési reakciók. |
Mi az endoterm reakció?
A kémiai reakció endoterm, amikor elnyeli az energiát a környezetből. Ebben az esetben a hőt a rendszer kívülről továbbítja a belső oldalra. Ha hőmérőt helyezünk, miközben az endoterm reakció zajlik, a hőmérséklet csökken.
Az "endoterm" szó a görögből származik endon ami "belül" és therme ami "hőt" jelent. Az endoterm reakciók nem spontán mennek végbe.
Honnan származik az energia az endoterm reakciókban?
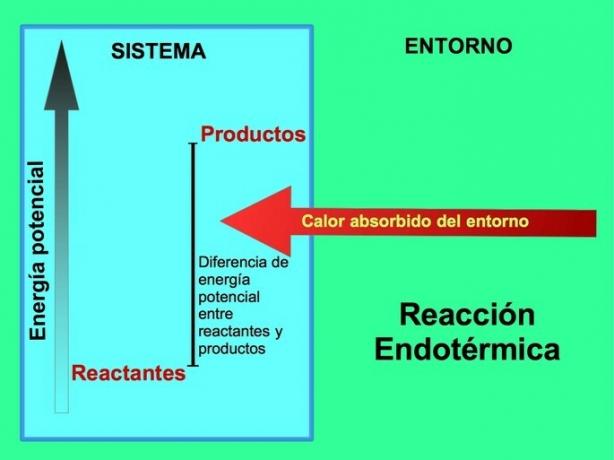
Az endoterm reakciók során az energia a rendszeren kívüli környezetből származik. A termékek potenciális energiájának mennyisége nagyobb, mint a reagensek potenciális energiája. Ezért a reakció lefolytatásához energiát kell adni a reagensekhez. Ez az energia a környezet hőjéből származik.
Például, a fotoszintézis endoterm folyamat, ahol a növények megfogják a napenergiát, hogy szén-dioxidból és oxigénből glükózt termeljenek:

A fotoszintézis reakció termékei, a glükóz és az oxigén, nagyobb mennyiségű potenciális energiát tartalmaznak a reagensek, a szén-dioxid és a víz vonatkozásában. További példák az endoterm kémiai reakciókra a felhasznált energia mennyiségével:

Példák az endoterm reakcióra
Nem csak a kémiai laboratóriumban fordulnak elő reakciók. Napról napra olyan helyzeteket is találunk, ahol endoterm reakciók lépnek fel.
Ételt főzni
Bár nem tűnhet annak, az ételek főzésének folyamata endoterm. Bizonyos ételek fogyasztásához hőt kell biztosítanunk.
Azonnali hidegzsák
A dudorok vagy rándulások kezelésére használt hideg csomagokat vízzel töltik fel, de rázáskor vagy kopogáskor ammónium-nitrátot tartalmazó kapszula törik be. Az ammónium-nitrát vízzel való keverése endoterm reakció, amely a tasak lehűlését okozza.
Érdekes lehet a Különbség a hő és a hőmérséklet között.
Mi az exoterm reakció?
A az exoterm reakció az, ahol az energia kifolyik a rendszerből. Ez az energia hő formájában szabadul fel, ezért hőmérőt helyezve a reakciórendszerbe, megnő a hőmérséklet.
Az "exoterm" szót az alkotja exo ami "kifelé" és termoszok, ami "hőt" jelent. Az exoterm reakciók spontán fordulhatnak elő, és egyes esetekben robbanásveszélyesek lehetnek, például alkálifémek és víz kombinációja.
Honnan származik az energia az exoterm reakciókban?
Kémiai reakcióban a reagensek azok a vegyületek, amelyek átalakulnak és termékeket képeznek. Például, amikor a nátrium-Na reagál klór-kloriddal, ezek a reagensek és a termék nátrium-klorid-NaCl:

A reaktánsok és a termékek is tárolják a potenciális energiát. A l-ből tudjukenergiatakarékosság ey hogy az energia nem vész el és nem nyerhető el, ezért a reagensek energiájának meg kell egyeznie a termékekével.
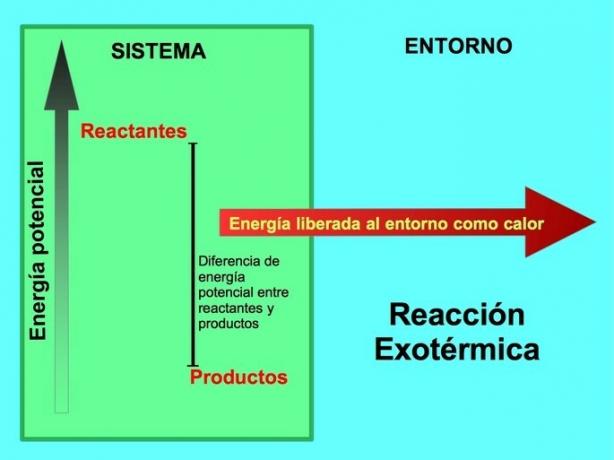
Exoterm reakcióban la reagensek több potenciális energiával rendelkeznek a termékekhez képest, így a felesleges energia hőként szabadul fel. Ebben az esetben az energiát is a termékek részének tekintik:

Bármely exoterm folyamatban a kémiai kötésekben tárolt potenciális energia egy része hő révén hőenergiává alakul.
Példák exoterm reakcióra
Mosószer
Amikor feloldunk egy kis mosóport vízzel a kezünkben, enyhe melegítést érezhetünk.
Háztartási gázégetés
A háztartási használatra szánt gázok, például a metán vagy a bután elégetése oxigénnel történő kémiai reakcióval jár együtt szén-dioxid és víz képződésével, valamint energia felszabadulásával. Ez egy tipikus exoterm reakció a mindennapi használat során:
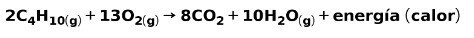
Az égési folyamat során felszabaduló energiát az ételek főzésére fordítják.
Az is érdekelheti, hogy mik azok Nyílt rendszer, zárt rendszer és elszigetelt rendszer.