Temukan bagaimana TABEL PERIODIK diatur dengan cara yang MUDAH dan PRAKTIS

Gambar: ptable.com
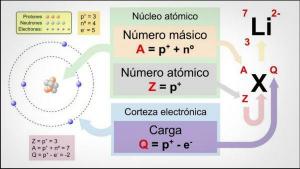
Pada tahun 1869, ahli kimia Rusia Dimitri Ivanovich Mendeleev menemukan cara untuk mengklasifikasikan semua unsur kimia yang muncul di alam. Metode klasifikasi ini adalah tabel periodik dan banyak yang menggambarkannya sebagai "jantung kimia". Tabel periodik lahir dengan hanya 63 unsur kimia, tetapi ketika ditemukan, banyak unsur kimia ditambahkan ke dalam urutannya.
Dalam pelajaran ini dari seorang GURU kita akan mengulas bagaimana tabel periodik diatur, melihat kriteria apa yang diikuti saat meletakkan elemen yang berbeda di kotak tabel ini.
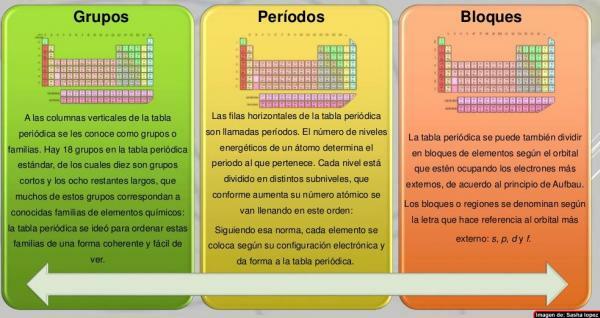
Di kolom tabel periodik mereka disebut kelompok. Saat ini, dalam tabel periodik yang biasa digunakan, yaitu yang standar, terdapat 18 golongan yang diberi nomor dari kiri ke kanan dari 1 sampai 18. Cara penamaan ini grup-grup (nomenklatur) dapat bervariasi: kadang-kadang digunakan nomenklatur campuran angka dan huruf Romawi, pada kesempatan lain kelompok memiliki nama umum (logam alkali, halogen, gas mulia, dll.) dan dalam istilah lain mereka disebut sebagai "kelompok ..." dan nama anggota pertamanya (misalnya, "kelompok skandium" untuk kelompok 3).
Elemen dari grup yang sama dapat memiliki pola sifat yang berbeda:
- Jari-jari atom meningkat, dari atas ke bawah dalam satu grup. Saat kita turun dalam tabel periodik, jumlah elektron meningkat dan oleh karena itu jumlah kulit yang terisi dengannya. Oleh karena itu, elektron pada kulit terakhir (kulit valensi) semakin jauh dari inti dan atom semakin besar, yaitu memiliki jari-jari yang lebih besar.
- Dari atas, setiap elemen memiliki energi ionisasi lebih rendah. Karena ada lebih banyak elektron, elektron yang ditemukan di kulit valensi lebih jauh dari nukleus dan oleh karena itu Ini menarik mereka dengan kekuatan yang lebih kecil, membuatnya lebih mudah untuk melepaskan elektron saat kita turun ke bawah. berkala.
- Akhirnya, kami juga mengamati penurunan keelektronegatifan dalam kelompok yang sama. Sekali lagi, karena jarak antara elektron valensi dan nukleus meningkat, elektron dari atom lain adalah lebih jauh dari gaya tarik inti dan oleh karena itu menariknya dengan gaya yang lebih kecil daripada atom yang lebih kecil (gugus). lebih tinggi).
Keteraturan ini adalah tren, yaitu, ada pengecualian tertentu seperti apa yang terjadi pada golongan 11, di mana keelektronegatifan meningkat lebih jauh ke bawah golongan. Selanjutnya, di beberapa bagian tabel periodik seperti blok d dan f, kesamaan horizontal antara unsur-unsur dari golongan yang sama tidak begitu mencolok.

Gambar: Perpustakaan Penelitian
Tujuh baris horizontal tabel periodik disebut periode. Jumlah tingkat energi suatu atom menentukan periode yang dimilikinya. Setiap tingkat dibagi ke dalam kategori yang berbeda yang disebut kulit atau orbital elektronik yang dapat bertipe s, p, d dan f.
Seperti yang terjadi di grup, item dari periode yang sama memiliki pola yang sama similar jari-jari atom, energi ionisasi, afinitas elektron, dan keelektronegatifan:
- Dalam suatu periode, jari-jari atom biasanya turun jika kita bergerak ke kanan pada tabel periodik. Saat kita berpindah dari satu elemen ke elemen berikutnya, proton dan elektron ditambahkan, menyebabkan mereka elektron ditarik ke dalam nukleus (ingat bahwa elektron terlalu ringan untuk gaya tarik-menarik inti).
- Penurunan jari-jari atom dalam periode yang sama membuat energi ionisasi dan keelektronegatifan meningkat dari kiri ke kanan, karena gaya tarik yang diberikan inti pada elektron meningkat.
- Itu Afinitas elektronik itu juga menunjukkan pola selama periode tersebut, meskipun lebih ringan. Logam, yang berada di sebelah kiri tabel periodik, umumnya memiliki afinitas lebih rendah daripada nonlogam, yang berada di sebelah kanan periode. Ini adalah hal yang umum dan tidak berlaku untuk gas mulia, yang lapisan terakhirnya (lapisan valensi) terisi dan oleh karena itu sangat sedikit reaktif.
Gambar: SlidePlayer
Unsur-unsur tabel periodik dapat dibagi dalam blok menurut urutan penyelesaian kulit elektron unsur. Setiap blok diberi nama sesuai dengan terbaruorbital di mana, secara teori, adalah elektron terakhir (s, p, d atau f):
- blok s Itu terdiri dari dua kelompok pertama, hidrogen dan helium.
- blok p Itu terdiri dari enam kelompok terakhir (kelompok 13 hingga 18).
- Blok d Golongan 3 sampai 12 (biasa disebut logam transisi) terbentuk.
- blok f, yang biasanya ditempatkan secara terpisah, di bawah sisa tabel periodik, tidak memiliki nomor golongan dan terdiri dari lantanida dan aktinida.
Tabel periodik unsur telah bertahan selama bertahun-tahun karena merupakan sistem yang telah terbukti sangat berguna dan terutama karena dapat diperbarui. Secara teori, mungkin ada lebih banyak elemen yang akan mengisi orbital lain, tetapi ini belum disintesis atau belum ditemukan. Dalam kasus di mana unsur-unsur atom baru ditemukan, para peneliti akan melanjutkan dengan urutan abjad untuk memberi nama blok yang berbeda (blok g, blok h, dll).
Gambar: Educando, portal Pendidikan Dominika