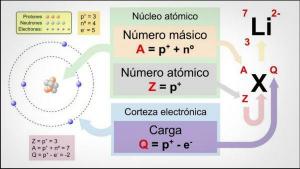
Scopri come è organizzata la TAVOLA PERIODICA in modo FACILE e PRATICO

Immagine: ptable.com
Nel 1869, il chimico russo Dimitri Ivanovich Mendeleev escogitò un modo per classifica tutti gli elementi chimici chemical che appaiono in natura. Questo metodo di classificazione è la tavola periodica e molti la descrivono come il "cuore della chimica". La tavola periodica è nata con solo 63 elementi chimici ma, man mano che sono stati scoperti, alle sue righe sono stati aggiunti numerosi elementi chimici.
In questa lezione di un INSEGNANTE esamineremo come è organizzata la tavola periodica, vedendo quali criteri vengono seguiti quando si inseriscono i diversi elementi nelle caselle di questa tabella.
A colonne della tavola periodica sono stati chiamati gruppi. Attualmente, nella tavola periodica normalmente utilizzata, cioè quella standard, sono presenti 18 gruppi, numerati da sinistra a destra da 1 a 18. Questo modo di nominare i gruppi (nomenclatura) può variare: a volte si usa una nomenclatura mista di numeri romani e lettere, in altre occasioni i gruppi hanno nomi comuni (metalli alcali, alogeni, gas nobili, ecc.) e in altri sono nominati come "il gruppo di ..." e il nome del suo primo membro (ad esempio, "il gruppo di scandio" per il gruppo 3).
Elementi dello stesso gruppo possono avere modelli di proprietà diverse:
- Aumento del raggio atomico, dall'alto verso il basso in un gruppo. Man mano che scendiamo nella tavola periodica, il numero di elettroni aumenta e quindi il numero di gusci pieni di essi. Pertanto, gli elettroni nell'ultimo guscio (guscio di valenza) sono più lontani dal nucleo e gli atomi diventano sempre più grandi, cioè hanno un raggio maggiore.
- Dall'alto, ogni elemento ha un minore energia di ionizzazione. Poiché ci sono più elettroni, quelli che si trovano nel guscio di valenza sono più lontani dal nucleo e quindi Questo li attrae con meno forza, rendendo più facile rimuovere gli elettroni mentre scendiamo nel tavolo. periodico.
- Infine, osserviamo anche a diminuzione dell'elettronegatività all'interno dello stesso gruppo. Di nuovo, all'aumentare della distanza tra gli elettroni di valenza e il nucleo, gli elettroni di altri atomi sono più lontano dalla forza attrattiva del nucleo e quindi li attrae meno fortemente degli atomi più piccoli (gruppi più alto).
Queste regolarità sono tendenze, cioè ci sono alcune eccezioni come ciò che accade nel gruppo 11, dove l'elettronegatività aumenta più in basso nel gruppo. Inoltre, in alcune parti della tavola periodica come i blocchi d e f, le somiglianze orizzontali tra elementi dello stesso gruppo non sono così marcate.

Immagine: Biblioteca di ricerca
Le sette righe orizzontali della tavola periodica sono chiamate periodi. Il numero di livelli energetici di un atomo determina il periodo a cui appartiene. Ogni livello è suddiviso in diverse categorie chiamate conchiglie o orbitali elettronici che possono essere di tipo s, p, d ed f.
Come è successo nei gruppi, gli articoli dello stesso periodo hanno modelli simili raggio atomico, energia di ionizzazione, affinità elettronica ed elettronegatività:
- In un periodo, il raggio atomico normalmente scende se ci spostiamo a destra sulla tavola periodica. Mentre ci spostiamo da un elemento all'altro, vengono aggiunti protoni ed elettroni, facendo sì che gli elementi gli elettroni vengono attirati nel nucleo (ricordate che gli elettroni sono troppo leggeri per la forza attrattiva nucleo).
- La diminuzione del raggio atomico nello stesso periodo fa sì che il energia di ionizzazione ed elettronegatività aumenta da sinistra a destra, poiché l'attrazione che il nucleo esercita sugli elettroni è in aumento.
- Il Affinità elettronica mostra anche un andamento nel periodo, anche se più mite. I metalli, che si trovano a sinistra della tavola periodica, hanno generalmente un'affinità inferiore rispetto ai non metalli, che si trovano a destra del periodo. Questa è una generalità e non vale per i gas nobili, che hanno il loro ultimo strato (strato di valenza) riempito e quindi sono molto poco reattivi.
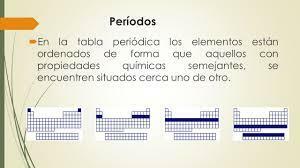
Immagine: SlidePlayer
Gli elementi della tavola periodica possono essere divisi in blocchi secondo l'ordine in cui i gusci elettronici degli elementi sono completati. Ogni blocco è denominato in base al ultimoorbitale in cui, in teoria, è l'ultimo elettrone (s, p, d o f):
- Il blocco s È costituito dai primi due gruppi, idrogeno ed elio.
- Il blocco p È composto dagli ultimi sei gruppi (gruppi dal 13 al 18).
- Blocco d Si formano i gruppi da 3 a 12 (comunemente chiamati metalli di transizione).
- Il blocco f, che normalmente è posto separatamente, al di sotto del resto della tavola periodica, non ha numeri di gruppo ed è composto da lantanidi e attinidi.
La tavola periodica degli elementi è sopravvissuta per tanti anni perché è un sistema che si è dimostrato molto utile e soprattutto perché può essere aggiornato. In teoria potrebbero esserci più elementi che riempirebbero altri orbitali, ma questi non sono ancora stati sintetizzati o non sono stati scoperti. Nel caso in cui venissero scoperti nuovi elementi atomici, i ricercatori continuerebbero con l'ordine alfabetico per denominare i diversi blocchi (blocco g, blocco h, ecc.).
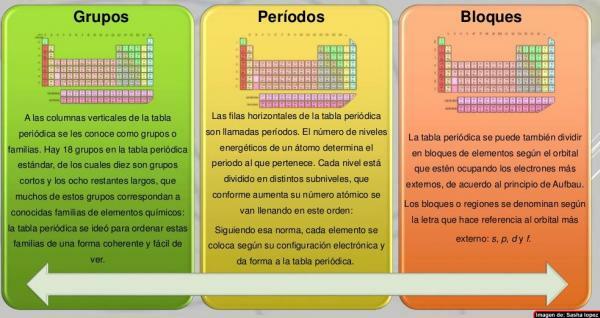
Immagine: Educando, il portale dell'educazione dominicana