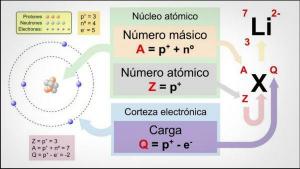
CARATTERISTICHE PRINCIPALI DEGLI ISOTOPI

Immagine: Pianeti
Tutta la materia che compone il nostro pianeta è costituita da atomi. Ma non tutti gli atomi sono uguali, gli atomi di elementi diversi hanno un numero diverso di protoni, neutroni ed elettroni. A volte il numero di questi le particelle subatomiche non sono le stesse, non sono equilibrati, e specie come il isotopi. Gli isotopi sono atomi dello stesso elemento (ad esempio idrogeno) ma non hanno lo stesso numero di neutroni. Questo "squilibrio" provoca il caratteristiche degli isotopi dello stesso elemento non sono uguali. In questa lezione di un INSEGNANTE esamineremo in dettaglio tutte queste caratteristiche. Abbiamo iniziato!
Indice
- Che cos'è un isotopo?
- Caratteristiche atomiche degli isotopi
- Una curiosa applicazione degli isotopi: marcatura isotopica
- Caratteristiche degli isotopi dello stesso elemento
Che cos'è un isotopo?
Prima di parlare delle caratteristiche degli isotopi, è importante conoscere meglio in cosa consistono.
particella subatomica. Potremmo dire quali sono gli isotopi sono "sottogruppi" di atomi: Sono atomi dello stesso elemento ma che differiscono in certe cose.Gli isotopi sono due atomi con lo stesso numero di protoni (lo stesso numero atomico), ma diverso numero di neutroni (diversa massa atomica). Gli isotopi dello stesso elemento sono solitamente denominati con il nome dell'elemento seguito dalla sua massa atomica. È ben noto el carbonio quattordici (C14), che viene utilizzato per determinare l'età dei fossili, ma il carbonio ha altri isotopi come carbonio 12 e carbonio 13, che sono più stabili di altri isotopi di carbonio come carbonio 8 o carbonio carbonio 22.
Nel nostro caso, tutti questi atomi sono atomi di carbonio quindi hanno numero atomico 6 (Z = 6) ma carbonio 12 (carbonio “normale”) ha un peso atomico di 12 contro il peso atomico di 14 di carbonio 14 o il peso atomico di 8 di carbonio C8.
Queste differenze tra i diversi isotopi possono far sì che gli atomi abbiano caratteristiche diverse, comportamenti con atomi di altri elementi, emivite, ecc.
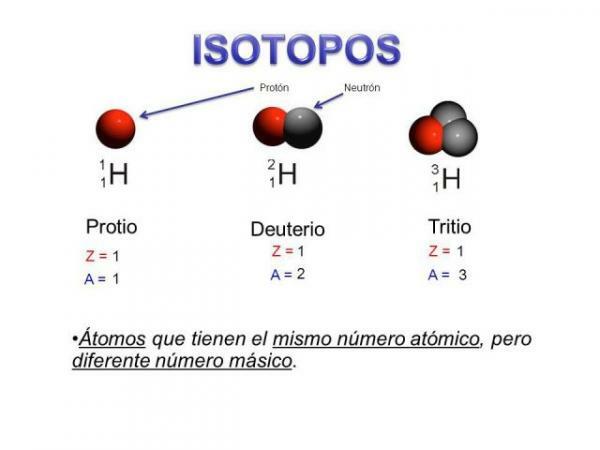
Immagine: i tuoi compiti
Caratteristiche atomiche degli isotopi.
- La prima caratteristica degli isotopi a livello atomico è che tutti gli isotopi sono atomi dello stesso elemento.
- Questa caratteristica principale ci porta a una seconda caratteristica: tutti gli isotopi di uno stesso elemento hanno la stesso numero atomico, cioè lo stesso numero di protoni.
- Tutti gli isotopi di un elemento hanno il stesso numero di protoni.
- Gli isotopi di uno stesso elemento hanno un diverso numero di neutroni, cioè diverso numero di massa o massa atomica.

Immagine: EHU
Una curiosa applicazione degli isotopi: la marcatura isotopica.
L'etichettatura isotopica è una tecnica che utilizza due caratteristiche molto importanti degli isotopi: che tutti gli isotopi reagiscono allo stesso modo in reazioni chimiche e che alcuni di loro hanno radioattività.
Durante una reazione chimica, due o più sostanze, chiamati reagenti, uniscono i loro atomi per formare altre sostanze diverse risultanti da diverse combinazioni, i cosiddetti prodotti. Il marcatura isotopica è una tecnica mediante la quale possiamo introdurre l'isotopo radioattivo di un reagente nella reazione, in modo che Questo reagirà in modo normale e possiamo localizzarlo in qualsiasi momento grazie alla radioattività che emettere.
Altre varianti di questa tecnica consentono di identificare diversi isotopi di un reagente mediante spettrometria di massa o spettroscopia infrarossa.

Immagine: Slideplayer
Caratteristiche degli isotopi di uno stesso elemento.
In conseguenza delle caratteristiche atomiche viste nella sezione precedente, gli isotopi dello stesso elemento possono avere altri tipi di caratteristiche, che descriveremo di seguito.
- Gli isotopi dello stesso elemento hanno massa diversa. Proprietà fisiche come densità, che sarà diverso per i diversi isotopi dello stesso elemento.
- Certo proprietà chimiche dipendono dal tipo di elemento che è, e quindi non saranno differenti per i diversi isotopi di un elemento. Un esempio è il solubilità, cosa sarà costante per tutti gli isotopi di un elemento.
- Strettamente correlata alla loro uguaglianza nelle proprietà chimiche è la seguente caratteristica degli isotopi: gli isotopi dello stesso elemento reagiscono allo stesso modo nelle reazioni chimiche. Ciò significa che se l'atomo di carbonio 12 (l'atomo più comune o "normale") reagisce con due atomi di ossigeno Per formare la molecola di anidride carbonica, sappiamo che anche quelli degli altri isotopi del carbonio sono lo faranno. Questa è una proprietà molto importante per molte applicazioni pratiche di isotopi e radioisotopi.
- Gli isotopi di un elemento possono essere of origine naturale o artificiale. Se l'isotopo in questione si trova in natura, senza che la mano dell'uomo sia intervenuta nella sua creazione, siamo di fronte ad un isotopo naturale mentre se è stato creato in reattori nucleari, acceleratori di particelle o generatori di radioisotopi diciamo che lo è artificiale. lo stesso elemento può avere isotopi naturali e artificiali.
- Gli isotopi possono essere radioattivo o non radioattivo. Gli isotopi radioattivi sono quelli in cui vi è un eccesso di energia, che l'atomo tende ad eliminare per passare da uno stato instabile ad uno di maggiore stabilità.
- In relazione alle caratteristiche precedenti possiamo dire che gli isotopi radioattivo loro hanno un tempo di vita variabile. La vita è il tempo che impiega l'isotopo a disintegrarsi, cioè a smettere di avere quell'energia in eccesso che lo rende instabile. Ci sono isotopi radioattivi che sono molto instabili e hanno una durata di pochi secondi mentre altri impiegano ore o addirittura anni per disintegrarsi e diventare isotopi più stabili. Normalmente gli atomi creati artificialmente hanno una vita o un tempo di decadimento molto più breve di quelli naturali.
Se vuoi leggere più articoli simili a Caratteristiche degli isotopi, ti consigliamo di entrare nella nostra categoria di l'atomo.
Bibliografia
- Briceno V, G. (s.f) Isotopi.
- Belmonte, A. (15 maggio 2019). Proprietà dell'atomo.
- Wikipedia (22 ottobre 2019). Isotopo.