סיווג מתכות מהטבלה המחזורית

ה מתכות הם ה אלמנטים שופעים יותר על טבלה מחזורית. הם מאופיינים ב: להיות מוליכים טובים של חום וחשמל, להיות מוצקים בטמפרטורת החדר (עם למעט כספית אשר נוזלית) ובעלת יכולת להחזיר אור, ולכן הם מציגים ברק מאפיין.
אך מערכת האלמנטים הגדולה הזו מוצגת מסודרת בתוך הטבלה המחזורית בקבוצות או במשפחות שונות המשקפות את הדמיון וההבדל ביניהן. בשיעור זה של מורה נראה מה ה סיווג מתכות ומה המאפיינים והתכונות של הקבוצות השונות המוגדרות בסיווג זה.
כפי שכבר הזכרנו, מתכות הן מרכיבי הרוב של טבלה מחזורית. הם מופצים ב שני חבר'ה נהדרים הכוללים, בכל מקרה, תת-סוגים שונים המקובצים למשפחות של הגושים השונים בטבלה המחזורית.
להלן נציג מתאר קצר של סיווג זה, אותו נפתח ביתר פירוט בסעיפים הבאים.
- 1. מתכות מייצגות: חסום את הטבלה המחזורית.
- 1.1. משפחה של מתכות אלקליות
- 1.2. משפחה של מתכות אלקליות
- 2. מתכות מעבר: חסום ד 'של הטבלה המחזורית.
- 3. מתכות מעבר פנימיות: חסום f בטבלה המחזורית.
- 3.1. לנתנידים: אלמנטים מהתקופה השישית בטבלה.
- 3.2. אקטינידים: אלמנטים של תקופת 7 בטבלה.
- 4. מתכות לאחר מעבר: גוש של הטבלה המחזורית.
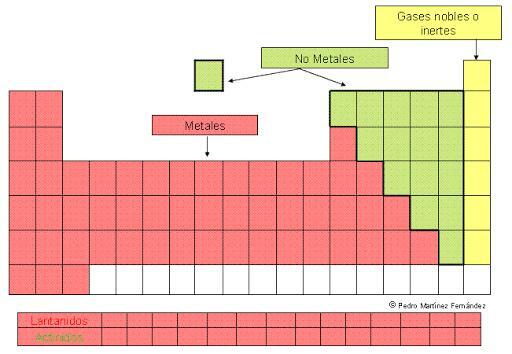
תמונה: Educamix
האלמנטים הייצוגיים או האלמנטים העיקריים הם אותם אלמנטים שהם
שופע יותר בטבע. בין האלמנטים המתכתיים, אלמנטים מייצגים הם המתכות של חסום שכלומר, היסודות האלקליין (משפחה 1 של הטבלה המחזורית) ואלמנטים האדמה הבסיסית (משפחה 2 של הטבלה המחזורית).בשתי קבוצות אלו אנו מוצאים אלמנטים ריאקטיביים מאוד, בעלי נטייה חזקה להתחמצן (לאבד את האלקטרונים שלהם מקליפת הערכיות) ולכן הם מפחיתים עוצמה של יסודות אחרים. בטבע הם נמצאים בצורה של מלחים יוניים מסיסים מאוד במים, תחמוצות או הידרוקסידים (בסיסים חזקים).
מתכות אלקליות (קבוצה 1 בטבלה המחזורית)
- מתכות אלקליות מייצגות 5% מקרום כדור הארץ. נתרן (Na) ואשלגן (K) הם הנפוצים ביותר.
- הם אלמנטים מבריקים כסוף למראה, צפיפות נמוכה, מתכות רכות, ותגובות מאוד. בשל תגובתיותם הגבוהה, הם אינם נמצאים במצבם הטהור בטבע. נקודות הרתיחה או האידוי של מתכות אלקליות נמוכות יחסית והן מוליכות טובות של חום וחשמל.
- מנקודת המבט של תצורתם האלקטרונית, הם אלמנטים המציגים א אלקטרון יחיד כובש את מסלול מעטפת הערכיות שלו. יש להם כוח משלב של 1 (ערכיות) ומספר חמצון +1. הם מראים נטייה רבה לאבד את האלקטרון מהקליפה החיצונית ביותר ליצירת קטיונים.
- כאלמנטים ביולוגיים, מתכות אלקליות מתפתחות א תפקיד חשוב ביצורים חיים, במיוחד נתרן ואשלגן, הממלאים תפקיד מהותי בהעברת עצבים ובמקרה של אשלגן בוויסות פעילות האנזים.
- למתכות האלה יש שימושים מרובים בתעשייה. לדוגמא, ליתיום (Li) משמש לייצור סגסוגות אלומיניום בעלות חוזק גבוה, בייצור קרמיקה, או כרכיבי סוללה. יש לו גם שימושים רפואיים שכן הוא מהווה מרכיב במערכת העצבים וחסרונו גורם למחלות פסיכיאטריות.
הערה: קבוצה 1 בטבלה המחזורית כוללת גם מימן, שאינו מתכת.
מתכות אדמה אלקליין (קבוצה 2 בטבלה המחזורית):
- מתכות אדמה אלקליין מייצגות 4% מהרכב קרום האדמה. הם שופעים במיוחד סידן (Ca) ומגנזיום (Mg).
- כמו המתכות האלקליות, מתכות אלה הם מאוד מגיבים כך שהם לא נמצאים בצורה חופשית בטבע.
- למרות שיש להם מאפיינים פיזיקוכימיים דומים למתכות האלקליות, הם נוטים להיות קשים ופחות תגוביים מהמתכות האלקליות. יש להם צפיפות נמוכה וקשיות ונקודות התכה גבוהות מאלה של מתכות אלקליות.
- מנקודת מבט של תצורת אלקטרונים, הם מאופיינים להציג את מסלולו של מעטפת הערכיות הממולאת (כלומר, תפוס על ידי זוג אלקטרונים). לכן, יש להם כוח משלב של 2 (ערכיות) ומספר חמצון של +2. הם מגיבים בקלות עם הלוגנים (קבוצה 17 בטבלה המחזורית), ויוצרים מלחים יוניים.
- התפקיד שלך בתור המרכיבים של אורגניזמים חיים זה חשוב במיוחד במקרה של סידן (Ca) ומגנזיום (Mg). יונים של מגנזיום וסידן הם היונים הנפוצים ביותר במי ים יחד עם יון הכלוריד (Cl-).
- 99% מהסידן בגופנו נמצא בשלד, אך בצורתו היונית יש לו תפקיד מהותי בהעברת עצבים, בתפקוד עצבי-שרירי ובוויסות אנזימטית.
- מגנזיום, בצורתו היונית, מבצע תפקידים ביולוגיים חשובים באורגניזמים חיים, כולל הבולט ביותר, תפקידו הבסיסי בפוטוסינתזה של צמחים כמרכיב כלורופיל.
- השימושים התעשייתיים במתכות אדמה אלקליין מגוונים. הרלוונטיים ביותר הם השימוש בסידן כמרכיב במלט, השימוש במגנזיום לפיתוח שריפות מלאכותי, כציפוי של מבני ברזל למניעת התחמצנותם או כמרכיב של סגסוגות ופלדות אוֹר.
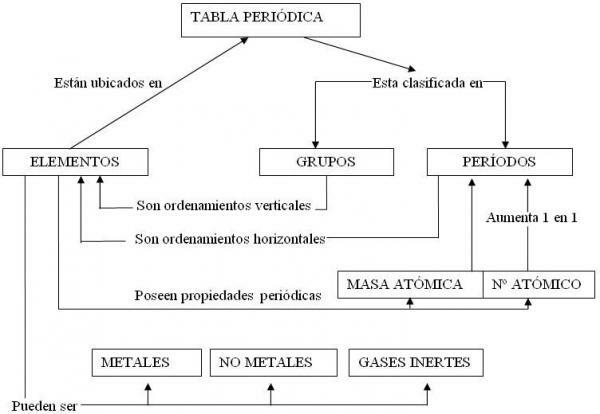
תמונה: אתרי גוגל
במסגרת סיווג המתכות עלינו לדבר על מתכות מעבר או מתכות של חסום ד, הם קבוצת המתכות הנפוצה ביותר ומקובצות ב- סך הכל 10 קבוצות או משפחות של הטבלה המחזורית.
- לרוב מתכות המעבר יש מאפיינים הדומים למתכות מייצגות: הן טובות מוליכים של חום וחשמל ומחזירים אור.
- הם מראים שונות רבה מבחינת הקשיות ונקודות הרתיחה וההיתוך, אך באופן כללי הם כן קשה יותר ובעל נקודות התכה ורתיחה גבוהות יותר ממתכות אלקליות ו אדמות אלקליין.
- מ ה נקודת מבט כימית הם מאופיינים ב: בעלי מספר קואורדינציה מרובה (ערכיות) או מצבי חמצון, הם בדרך כלל זרזים טובים (יכולת להגדיל או להקטין את קצב התגובות הכימיות) וליצור תרכובות בעלות צבע ובעלות יכולת יוצרים קומפלקסים של תיאום (תרכובות כימיות עם יון מתכתי במרכז, מחוברים לסדרה של ליגנדים המסודרים בתוכם סְבִיב). מסיבה זו, מתכות מעבר יוצרות קטיונים של מטענים שונים.
- צפיפות משתנה מאוד בגוש יסודות זה, מסטרונציום עם צפיפות נמוכה ועד אוסמיום (Os), שהוא היסוד בעל הצפיפות הגבוהה ביותר בטבלה המחזורית.
- אם נסתכל על התצורה האלקטרונית של מתכות מעבר, הן מאופיינות בהצגה אורביטלים מלאים חלקית. מילוי האורביטלים בגוש זה של הטבלה המחזורית מציג סדרת אי סדרים אשר באים לידי ביטוי במספרי החמצון המרובים שנרכשו על ידי המתכות בבלוק זה של הטבלה תְקוּפָתִי.
ברזל (Fe) וטיטניום (Ti): מתכות מעבר רבות יותר
- ברזל הוא הנפוץ ביותר ומייצג כ -5% ממשקל קרום כדור הארץ. נדיר למצוא אותו בצורתו האלמנטרית בטבע, שם הוא נמצא בדרך כלל ויוצר תחמוצות ופחמתי.
- לברזל טהור מעט שימושים, אך לסגסוגות שלה עם חומרים אחרים שימושים מרובים. הצורות השימושיות של סגסוגות ברזל הן ברזל יצוק (זהו סגסוגת ברזל המאופיינת בתכולת הפחמן הנמוכה ובתכולת הברזל הגבוהה שלה). יש לו את המאפיין שהוא יכול להיות יצוק לוהט ומתקשה בקירור מהיר), ברזל יצוק (הידוע גם בשם שמו של ברזל יצוק אפור או ברזל יצוק, זהו סגסוגת של ברזל, סיליקון ופחמן המכילה כמויות קטנות של מנגן, זרחן ו גוֹפרִית; בהם פחמן הוא בצורת גרפיט) ופלדה (סגסוגת מטוהרת של ברזל ופחמן).
- מתכות מעבר אחרות שנמצאות בשימוש נרחב בתעשייה הן נחושת וכסף. בנוסף, מתכות מעבר רבות משמשות בתעשייה כזרזים לתגובות כימיות.
- ברמה הביולוגית, לברזל בצורתו היונית יש תפקיד מהותי ב הובלת חמצן, מכיוון שהוא חלק מהמרכז הפעיל של המוגלובין ומיוגלובין.
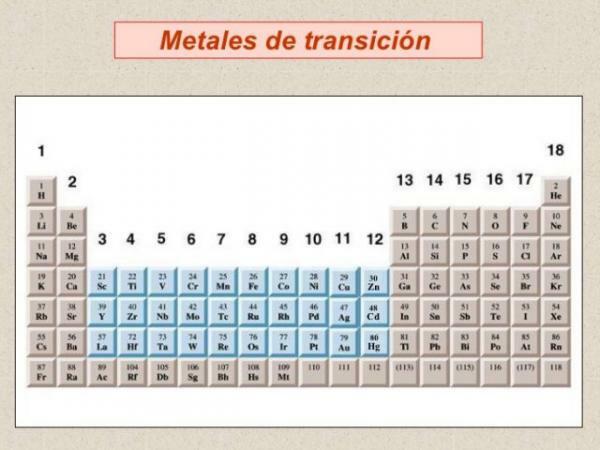
תמונה: אתר 100cia
מתכות המעבר הפנימיות או המתכות של חסום והם נקראים גם אדמות נדירות. הם מקובצים לשתי משפחות של אלמנטים: לנתנידים וה אקטינידים. הם אותם יסודות מתכתיים בהם נמצאים אלקטרונים התופסים את המסלולים. האלמנטים של קבוצת הלנטנידים כבשו חלקית את האורביטליות של רמה 4 ואת האקטינידים של רמה 5.
לנתנידים או לנתנואידים
- הם 15 האלמנטים של מעבר פנימי שהם חלק מה- תקופה 6 של הטבלה המחזורית של האלמנטים.
- לקבוצת אלמנטים זו תכונות אופייניות משותפות. הוא בערך מתכות רכות ומבריקות כסף מוליכות החום והחשמל שלו נמוכה יחסית למתכות אחרות. הן מתכות בעלות צפיפות נמוכה יותר ממתכות מעבר.
- בטבע הם נמצאים בפרופורציות נמוכות, המהווים חלק מרבים מינרלים. לנטנידים בעלי יכולת גבוהה למגנטציה או מגנטיזציה ומאופיינים גם בזוהר הקטיונים שלהם.
- לנתנידים יש שימושים מרובים בתעשייה בייצור מגנטים קבועים חזקים, סוללות נטענות וייצור חומרים מוליכים-על. יש להם מספר יישומים באופטיקה (ייצור צינורות פלורסנט ומנורות, תצוגות גביש נוזלי ולייזרים). הם משמשים גם כזרזים לתגובות כימיות או כפיגמנטים.
אקטינידים או אקטינואידים
- הם 15 האלמנטים המרכיבים את תקופה 7 של הטבלה המחזורית.
- רבים מהם סונתזו באופן מלאכותי, אך הם נמצאים גם בטבע בפרופורציות קטנות מאוד.
- הם מראים התנהגות דומה לזו של מתכות המעבר (גוש ד) ושונה מאלה של הלנתנידים. כמו במקרה של מתכות רבות, יש להן ברק כסוף אופייני.
- כקבוצה, חשיבותם נעוצה בעובדה שכולם יסודות רדיואקטיביים. כלומר, מדובר באלמנטים שהגרעינים שלהם אינם יציבים מתפרקים, ומשחררים אנרגיה (אנרגיה גרעינית) ומולידים יסודות כימיים אחרים בעלי גרעין יציב יותר. כל האיזוטופים של היסודות בקבוצה זו הם רדיואקטיביים ובעלי מחצית חיים קצרים. האקטינידים הנפוצים ביותר בטבע הם אורניום (U) ותוריום (Th).
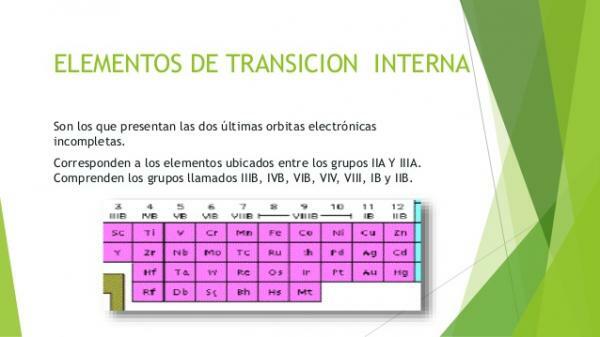
תמונה: מצגת שקופיות

