Moeller図:それが何であるか、それが化学でどのように使用されるか、そして例
化学は特に複雑になる可能性があるため、化学を紹介された人の学習を容易にするツールはどれでも歓迎します。
マデルングの法則と原子の電子配置に精通するための最も一般的な方法の1つは次のとおりです。 Moellerダイアグラムは、どの軌道でどの軌道にあるかを非常に簡単に確認できるグラフィカルなニーモニックルールです。 電子。
次 Moeller図が何で構成されているかを発見します、それがマデルングの法則とどのように関連しているか、いくつかの解決された例によってどのように適用されているか、そしてどの化学元素がこの戦略に従わないか。
- 関連記事: 「5種類の化学結合:これが物質の構成方法です」
Moeller図とは何ですか?
雨の方法または対角線の法則としても知られているMoeller図は次のとおりです。 マデルングの法則を学習するためのグラフィックおよびニーモニック法、化学元素の電子配置を知り、書くための技術.
この図は、軌道の列を上から下へ、右から左へと対角線を描くことを特徴としています。 Moellerダイアグラムを介して、軌道の充填の順序が定義されます。これは、n、l、およびmlの3つの量子数によって定義されます。
Moellerダイアグラムは、次のように機能します。

各列は、原子の電子が循環する異なる軌道、負の電荷を持つ亜原子粒子に対応します。 問題の軌道は次のとおりです。s、p、d、f、それぞれが電子を収容するための特定の空間を持っているため、エネルギーレベルが異なります。.
前述の意味で対角線または矢印を描くと、最初の軌道は1sになります。 2番目の矢印は2s軌道で始まります。 3番目の矢印は2pと3sを横切っています。 4番目の対角線は3pと4sです。 5番目の対角線は3d、4p、5sなどです。 Moellerダイアグラムは、化学の周期表の元素の電子配置を研究し始めた人のための入門的な手法です。
- あなたは興味があるかもしれません: 「自然科学の6つの主要な分野」
マデルングの法則
Moeller図以来 マデルングの法則をグラフで表したものです (一部の国ではクレチコフスキーの規則としても知られています)最初にそれが何であるかを知る必要があります。 この規則によれば、原子の軌道の充填は、次の2つの規則に従う必要があります。
マデルングの最初のルール
n + lの最小値を持つ軌道が最初に埋められ、nが主量子数、lが軌道角運動量です。.
たとえば、3d軌道はn = 3およびl = 2に対応します。 したがって、n + l = 3 + 2 = 5です。 代わりに、4s軌道はn = 4およびl = 0に対応するため、n + l = 4 + 0 = 4になります。 このことから、4s = 4で3d = 5であるため、電子は3d軌道の前に最初に4s軌道を満たすことが確立されます。
- 関連記事: 「11種類の化学反応」
マデルングの2番目のルール
2つの軌道のn + lの値が同じである場合、電子は最初にnの値が小さい方の軌道を占有します。.
たとえば、3d軌道の値はn + l = 5で、4p軌道の値(4 + 1 = 5)と同じですが、3d軌道のnの値が最も低いため、最初に充填されます。 4p軌道。
これらすべての観察と規則から、原子軌道を埋めるには次の順序に達することができます:1s 2s 2p 3s 3p 4s 3d4p。 この順序は固定されていますが、それを心から覚えるのは複雑です。そのため、その順序をグラフィカルに表すMoeller図があります。
- あなたは興味があるかもしれません: 「ダルトンの原子理論の9つの仮説」
Moeller図を使用するときに従うべき手順
前のセクションでコメントしたように、Madelungのルールは式n + lを使用して何を確立します 軌道は、要素の電子配置が何であるかを決定する前後に満たされます 決定。 ただし、Moellerダイアグラムはすでにこれをグラフィカルかつ簡単に表しているため、 同じ図の列と対角線を描いて、それぞれの軌道がどのような順序であるかを調べます エレメント。
原子の電子配置とその電子が配置されている軌道を発見するには、まずその原子番号Zを知る必要があります。. 数Zは、この原子が中性である限り、または同じである限り、原子内の電子の数に対応します。つまり、それはイオンではなく、正(陽イオン)でも負(陰イオン)でもありません。
したがって、中性原子のZがわかれば、その元素の中性原子が通常持っている電子の数はすでにわかっています。 これを念頭に置いて、Moeller図に対角線を描き始めます。 軌道の種類ごとに電子を収容する能力が異なることを考慮に入れる必要があります、これは:
- s = 2電子
- p = 6電子
- d = 10電子
- f = 14電子
Zによって与えられた最後の電子が占有された軌道で停止します。
Moeller図の例
Moellerダイアグラムがどのように機能するかをよりよく理解するために、以下に、さまざまな元素の電子配置を設定するいくつかの実用的な例を示します。
ベリリウム
中性ベリリウム(Be)原子の電子配置を確立するには、最初に周期表でそれを探す必要があります。 表の2列目と2行目にあるアルカリ土類. その原子番号は4であるため、Z = 4であり、4つの電子もあります。
これらすべてを考慮して、Moellerダイアグラムを使用して、この元素の4つの電子がどのように配置されているかを確認します。 まず、前述の意味で、上から下、右から左に対角線を作成します。
軌道を埋めるとき、 それぞれに見つかった電子の数を上付き文字として入力することをお勧めします. 1sは最初の軌道であり、2つの電子を占有するため、次のように記述します。

私たちはまだ自由電子を持っているので、軌道を埋め続けます。 次は2s軌道で、1sと同様に、2つの電子を占有します。したがって、2s2。 Beの中性原子の軌道にすべての電子がすでに配置されているので、この元素の電子配置は次のようになります。

上付き文字を追加することで、うまくいったことを確認します:2 + 2 = 4
- あなたは興味があるかもしれません: 「分子運動論:物質の3つの状態」
マッチ
元素リン(P)は、周期表の3行16列にある非金属です。、Z = 15の場合、軌道を占有する必要のある合計15個の電子があります。
前の例を見て、少し前に進み、その電子の4つを見つけることができます ベリリウムが4つの電子に対して持っているのと同じ軌道で、9つの電子が欠落しています プラス。

2s軌道の後、次の対角線は2p軌道に入り、3s軌道で終了します。 2p軌道は6個の電子を占有でき、3sの場合は2個しか占有できません。 したがって、次のようになります。
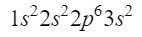
現時点では、12個の電子が適切に配置されていますが、まだ3個残っています。 別の対角線を作成し、今度はMoeller図に従って3p軌道、つまり6つの電子のためのスペースを持つ軌道から入ります。、ただし、電子が3つしか残っていないため、この軌道は完全には占有されず、上付き文字として3を使用します。 したがって、リンを終わらせるために、その電子配置は次のようになります。

上付き文字を追加することで、うまくいったことを確認します:2 + 2 + 6 + 2 + 3 = 15
ジルコニウム
元素ジルコニウム(Zr)は、列4と行5にある遷移金属であり、Z = 40です。. 前の例を利用してパスを短くすると、最初の18個の電子を見つけることができます。
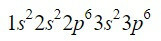
3p軌道の後、Moellerダイアグラムで私たちを導く次の軌道は、それぞれ2、10、6、および2電子の容量を持つ4s、3d、4p、および5s軌道です。

図の最初の9つの軌道を完了すると、合計20個の電子が追加されます。 次の軌道である4dに格納されている残りの2つの電子を残します. したがって、中性元素であるジルコニウムの電子配置は次のとおりです。
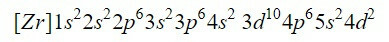
上付き文字を追加することで、うまくいったことを確認します:2 + 2 + 6 + 2 + 6 + 2 + 10 + 6 + 2 + 2 = 40
空気
ここに、酸素(O)というもう少し複雑な例があります。. このガスは周期表の16列目と2行目にあり、非金属で原子番号は8です。
これまでのところ、他の例を見ると、そのZ = 8と思いますが、このガスは特殊な性質であり、ほとんどの場合、-2の電荷を持つイオンの形であるため、それほど単純ではありません。
つまり、中性酸素原子には、原子番号で示されているように8つの電子がありますが、 確かに、自然界では10個(8個の電子+ 2個の電子、または必要に応じて-8個の電荷)があります。 電気-2)。
したがって、この場合、 軌道上に配置しなければならない電子の数は8ではなく10の電子です、Z = 10の化学元素ネオンの電子を探しているかのように。
これを理解すると、イオン(陰イオン)を使用していることを考慮に入れて、前のケースで行っていたのと同じことを行うだけで済みます。
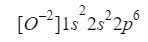
上付き文字を追加することで、うまくいったことを確認します:2 + 2 + 6 = 10
カルシウム
カルシウム(Ca)にも酸素に似たことが起こりますが、この場合のみ、陽イオン、つまり正電荷を持つイオンについて話します。.
この元素は、原子番号20の周期表の列2行4にありますが、 自然は通常、正電荷が+2のイオンの形で表されます。これは、その電荷が18(- 20 + 2 = 18; 20電子-2電子= 18電子)。
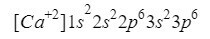
上付き文字を追加することで、うまくいったことを確認します:2 + 2 + 6 + 2 + 6 = 18
Moeller図とMadelungの規則の例外
Moellerの図は、Madelungの法則を理解し、さまざまな化学元素の電子がどのように配置されているかを知るのに非常に役立ちますが、真実は間違いありません。 組成が私たちが説明したことに従わない特定の物質があります。
それらの電子配置は、量子的な理由からマデルングの法則によって予測されたものと実験的に異なります。. 私たちが持っている基準に従わないこれらの元素の中には、クロム(Cr、Z = 24)、銅(Cu、Z = 29)、銀(Ag、Z = 47)、ロジウム(Rh、Z = 45)、セリウム( Ce、Z = 58)、ニオブ(Nb; Z = 41)、とりわけ。
d軌道とf軌道を埋めるとき、例外が非常に頻繁に発生します。 たとえば、Moellerの図とMadelungの法則によれば、4s ^ 2 3d ^ 4で終わる原子価配置を持つはずのクロムの場合、実際には4s ^ 1 3d ^ 5の原子価配置になります。 もう1つの奇妙な例は、銀の例です。これは、最後の例として5s ^ 2 4d ^ 9ではなく、5s ^ 1 4d ^ 10です。

