주기율표는 무엇을 위한 것입니까?
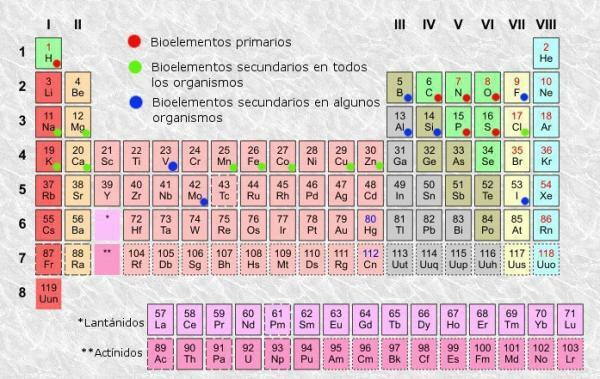
주기율표는 러시아 화학자가 1869년에 발명한 원자 원소의 분류 체계입니다. Dmitri Mendeleev 및 나중에 다른 화학자들에 의해 그의 모습에 도달할 때까지 재구성 및 업데이트됨 흐름. 역사 전반에 걸쳐 유용함이 입증된 도구임에도 불구하고(그래서 계속 사용 및 업데이트됨) 배우고 이해하기가 너무 지루하기 때문에 우리 모두는 "테이블은 무엇을위한 것입니까? 주기적? ".
알고 싶다면 주기율표는 무엇입니까 속성을 이해하는 것이 왜 중요한지, 교사로부터 이 수업을 계속 읽으십시오.
인덱스
- 주기율표의 분류
- 주기율표로 원소의 이름이나 기호 찾기
- 원소의 원자량을 안다
- 원소의 원자번호를 안다
- 원소의 원자 반경 예측
- 두 원소의 이온화 에너지 비교
- 화학 원소의 전기 음성도 찾기
- 두 원소의 전자 친화력 비교
주기율표의 분류.
모든 테이블에서와 마찬가지로 주기율표 열(세로)과 행(가로)을 구분할 수 있습니다. 주기율표에는 18개의 열 또는 그룹과 7개의 행 또는 기간이 있습니다.
또한 일반적으로 표의 각 상자 내에서 최소한 다음 정보가 나타나는지 확인할 수 있습니다.
- 화학 원소 기호: 요소를 식별하는 데 사용되는 약어 또는 기호. 일반적으로 하나 또는 두 개의 문자로 구성되며 첫 번째 문자는 항상 대문자입니다.
- 화학 원소 이름: 상위 약어에 해당하는 화학 원소의 이름. 일반적으로 기호 아래에 있습니다.
- 원자 번호: 해당 원소의 각 원자가 가지고 있는 양성자의 총 수. 일반적으로 항목 상자의 왼쪽 상단(또는 더 완전한 테이블의 오른쪽 상단)에 나타납니다.
- 원자 질량: 원자의 질량은 일반적으로 단일 원자에 있는 양성자와 중성자의 총 질량으로 간주할 수 있습니다. 가장 단순한 표에서는 요소 이름 아래에 표시되지만 다른 표에서는 요소 상자의 오른쪽 상단에 나타날 수 있습니다.
다음과 같은 더 복잡하고 구체적인 정보를 포함하는 주기율표가 있습니다. 산화 상태 (예를 들어, 화합물을 공식화할 때 유용함), 이온화 에너지, 전기 음성도 등, 그러나 기본 주기율표는 일반적으로 충분한 정보를 제공하고 일반적으로 일반 사용자에게 충분합니다. 사용자는 아래에서 우리가 말하는 것과 같은 정보를 찾을 수 있습니다.

주기율표로 원소의 이름이나 기호를 찾으십시오.
때때로 우리는 알고 있습니다. 화학 원소 기호 그러나 우리는 그의 이름을 모릅니다. 다른 시간에는 우리가 알고 있습니다. 화학 원소 이름, 그러나 그 약어나 기호는 아닙니다. 사실, 수업 중에 이런 일이 일어난 것은 매우 쉽습니다.
이런 경우 복잡한 주기율표를 사용할 필요 없이 주기율표를 사용하여 누락된 데이터를 빠르고 정확하게 조회할 수 있습니다.
원소의 원자량을 알 수 있습니다.
때때로 우리는 우리가 다루고 있는 화학 원소를 알고 있지만 그 원소를 알아야 합니다. 원자 질량, 즉 해당 원소의 원자 무게가 얼마인지입니다.
이 정보는 예를 들어 다음 작업을 수행할 때 유용합니다.
- 물질의 특정 양을 계산합니다.
- 테스트 또는 실험에서 얻은 결과를 분석합니다.
- 질량의 백분율을 계산하십시오.
- 복잡한 분자의 정확한 몰 질량을 이해합니다.
원소의 원자번호를 안다.
원자 번호는 원소의 원자가 가지고 있는 총 양성자 수. 양이온이 아닌 전기적으로 중성인 원자에서(양전하를 띠며 정상 상태보다 하나의 전자가 작음) 또는 음이온(음전하를 띠고 정상 상태보다 하나의 전자가 더 많음)인 경우 양성자의 수는 다음과 같습니다. 전자.
전자나 중성자의 수는 원소의 종류를 바꾸지 않기 때문에 양성자의 수는 한 원소를 다른 원소와 구별할 때 결정적인 요소입니다.

원소의 원자 반경을 예측합니다.
원자 반경은 서로 거의 접촉하지 않는 동일한 원소의 두 원자 중심 사이 거리의 절반입니다. 이 경우 알아두세요. 주기율표에서 화학 원소의 위치 대략적인 원자 반경을 찾거나 다른 요소와 비교하는 데 도움이 될 수 있습니다. 이를 위해 우리는 그것을 알아야합니다 원자 반경:
- 주기율표의 상단에서 하단으로 이동함에 따라 증가합니다.
- 주기율표를 따라 왼쪽에서 오른쪽으로 이동할 때 하강합니다.
이런 식으로 칼슘은 루비듐보다 작지만 철보다 큽니다.
에 대해 자세히 알아보기 원자 반경은 무엇입니까 교사의 다른 비디오 수업과 함께.
두 원소의 이온화 에너지를 비교하십시오.
그만큼 이온화 에너지 이다 원소의 원자에서 전자를 제거하는 데 필요한 에너지. 이 경우 주기율표에서 두 원소의 위치를 알면 전자를 "제거"하는 것이 더 쉬운 원소를 알 수 있습니다. 다음 사항만 고려하면 됩니다.
- 이온화 에너지는 주기율표를 위아래로 움직일 때 감소합니다.
- 이온화 에너지는 주기율표의 왼쪽에서 오른쪽으로 이동할 때 증가합니다.
베릴륨과 산소 사이에서 산소는 더 많은 이온화 에너지를 갖습니다. 같은 족에 속하지만 다음 주기에 있는 산소와 황을 비교하면, 산소도 주기율표에서 더 높기 때문에 더 높은 이온화 에너지를 가집니다.
화학 원소의 전기 음성도를 찾으십시오.
전기 음성도 이다 전자를 끌어당기는 원자의 능력. 실제로 이것은 화학 결합을 형성하는 능력으로 해석됩니다. 화학 원소가 화학 결합을 형성할 수 있는 큰 능력을 가지고 있는지 여부를 알기 위해서는 주기율표에서 다음과 같은 패턴만 고려하면 됩니다.
- 위아래로 움직이면서 내려옵니다.
- 왼쪽에서 오른쪽으로 이동함에 따라 증가합니다.
앞의 경우와 마찬가지로 산소는 첫 번째보다 오른쪽에 있고 황보다 높기 때문에 베릴륨 및 황보다 전기 음성도가 높습니다.

두 원소의 전자 친화력을 비교하십시오.
그만큼 전자 친화성 그는 중성 원자가 전자를 끌어당길 때 받는 에너지 변화 음이온이 됩니다. 이 경우 전자 친화도는 이전의 경우처럼 정확하게 변하지 않지만 일반적으로 전자 친화도는 다음과 같습니다.
- 같은 기간에 왼쪽에서 오른쪽으로 상승합니다.
- 같은 그룹에서 아래에서 위로 올라갑니다.
비슷한 기사를 더 읽고 싶다면 주기율표는 무엇을 위한 것입니까?, 다음 카테고리를 입력하는 것이 좋습니다. 원자.
참고문헌
주기율표 사용에 대한 의견이나 의견이 있습니까? 댓글 섹션에 자유롭게 남겨주세요! 이 기사가 마음에 드셨나요? 아래에 평가를 남길 수도 있습니다!