화학 공식 및 예의 종류

화합물은 모든 물체에 존재합니다 그리고 우리 행성의 생명체. 이러한 화합물을 알아보려고 할 때 일반적으로 다소 복잡할 수 있고 다소간의 정보를 제공할 수 있는 화학식이 사용되며 이를 화학식이라고 합니다. 오늘의 기사에서 교사 우리는 다른 것에 대해 이야기 할 것입니다 화학식의 종류 그리고 그 예. 그들에 대해 더 알고 싶다면 여기에서 알려드립니다!
그만큼 화학식 ~이다 요소의 그래픽 표현 존재하는 화합물을 형성하게 됩니다. 이 공식은 분자의 일부인 다른 원자의 양과 비율을 나타내며 일부 유형의 공식은 또한 다른 유형을 연결하는 화학 결합 유형을 나타냅니다. 집단. 알려진 분자 또는 화합물 각각에 해당합니다. 화학 명명법 사용된 공식 유형에 따라 IUPAC(순수 및 응용 화학 국제 연합)에서 설정했습니다.
존재하는 다양한 유형의 화학식 특정 유형의 정보 제공 일반적으로 그것들은 모두 그것을 형성하는 물질의 화학적 성질을 이해하고 무엇을 표현하는지에 기여합니다. 때때로 일부 원소나 화합물이 다음으로 변형될 수 있기 때문에 특정 화학 반응 중에 발생 다른 사람. 이러한 이유로 화학식은 다음과 같습니다. 원소와 분자의 대표 체계 전문 기술 언어에 의해 결정됩니다.
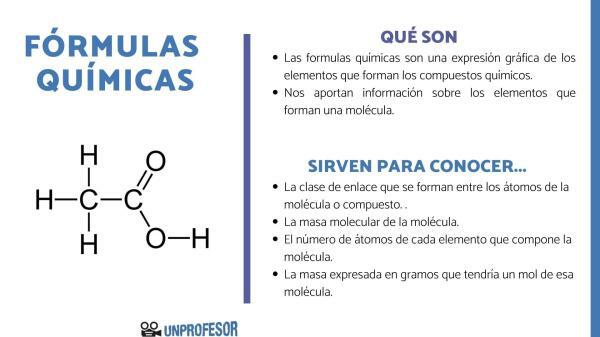
일반적으로 화학식의 종류에 관계없이 이러한 화학식은 약 글자 모양의 화학 기호 대표하는 원자의 종류 에 따라 분자를 형성하는 원소 주기율표 및 분자 내 상대적인 양을 나타내는 화학 기호 옆에 첨자 형태의 일부 숫자.
일부 화학 분야(특히 유기 화학)에는 다음과 같은 화학 그룹이 있습니다. 분자의 구조적 및 기능적 재발, 이를 통해 분자 또는 화합물의 특정 단편을 식별할 수 있습니다. 이러한 분자 조각을 화학 라디칼(짝이 없는 전자가 있는 경우) 또는 화학 그룹이라고 합니다. 기능적(화합물이 특정 방식으로 반응하거나 행동하게 하는 원자 또는 단위인 경우) 방법).
일부 화학적 라디칼의 예 그들은 메틸 라디칼(CH3), 브롬 라디칼(Br-) 또는 염소 라디칼(Cl-)입니다. 작용기의 예는 카르보닐기(CO), 히드록실기(OH) 또는 카르복실기(COOH)이다.

존재하는 다양한 유형의 화학식은 구성 요소의 화학 기호와 이들 사이에 설정되는 논리적 비율을 사용하며 다음과 같이 표현됩니다. 수학 기호. 명명법에 사용된 다른 화학식은 다음과 같습니다.
분자식
분자식은 가장 기본적인 공식이다. 존재하는 원자의 종류와 화합물에 존재하는 각 원자의 수를 나타냅니다. 공식은 작성 및 해석이 매우 간단하며 화학 원소의 기호와 그 숫자를 선형 시퀀스의 형태로 아래 첨자 형태로 표시합니다. 예를 들어, 다음 공식이 있습니다.
- 염기성 산화물: Na2O(산화나트륨), K2O(산화칼륨), MgO(산화마그네슘).
- 수산화물: NaOH(수산화나트륨) KOH(수산화칼륨), Ca(OH)2(수산화칼슘), Mg(OH)2(수산화마그네슘)
- 산: HCl(염산), H3PO4(인산), H2SO3(황산), H2SO4(황산)
- 염: NaCl(염화나트륨), Na2SO3(아황산나트륨), Na2SO4(황산나트륨)
반개발 공식
반 진화식은 분자식과 유사하며 화합물을 구성하는 원자를 표현하고, 선 형태의 화학 결합과 화합물의 원자를 연결하는 결합 유형(단순, 이중 또는 삼중). 그러나 이러한 유형의 공식에서는 탄소-수소 결합이 표시되지 않습니다. 이러한 유형의 공식은 유기 화학 명명법에 널리 사용됩니다. 이러한 수식 유형의 예는 다음과 같습니다.
- 유기화학의 반개발 공식: CH3-CH3(에탄), CH3-CH2-OH(에탄올)
- 무기 화학에서 반 개발 공식: 드물게 PO(OH)3(인산), (OH)2P(O)OP(O)(OH)2(피로인산)
개발된 공식
이것은 화학식의 또 다른 유형입니다. 반개발보다 조금 더 복잡합니다. 이 유형의 공식에서는 결합과 분자 내 원자의 위치가 표시되어 데카르트 평면에서 화합물의 구조를 나타냅니다.
구조식
이러한 유형의 화학식은 매우 복잡하지만 분자에 대한 많은 정보를 제공합니다. 구조 및 조직에 추가하여 공간 형태를 이중 또는 입체적.
루이스 공식
그들은 또한 루이스 다이어그램 또는 루이스 구조이며 개발된 공식과 유사하지만 이 경우에도 원자 사이의 각 결합에서 공유되는 전자는 다음과 같이 표시됩니다. 링크의 선에 연결된 점으로 표시됩니다. 공유되지 않은 전자는 또한 원자에 점으로 표시됩니다. 이 공식은 매우 기술적이고 매우 특정한 분야에서 사용됩니다.



![화학 공식이란 무엇이며 [요약 + 비디오]](/f/d107af781e6392bdf80e01f34e449116.jpg?width=300&height=200)