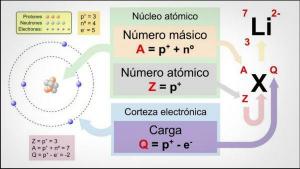
Kā iegūt MASIKAS NUMURU?

Atomi ir daļa no visa materiāla, kas veido Visumu. Matērija ir ļoti dažāda, jo to veido dažāda veida atomi, ar atšķirīgām īpašībām un īpašībām. Dažādu atomu īpašības dod daļiņas, kas tos veido: protoni, elektroni un neitroni. Atšķirīgās proporcijas starp vienu un otru ir noteiktas ķīmijā ar dažādiem nosaukumiem (masas numurs, atomu skaitlis utt.). Masas numurs dod mums galīgo vai kopējo daļiņu skaitu kodolā vai tas pats, kas tas ir veido summu starp protoniem un neitroniem, un to izmanto ķīmijā, lai diferencētu elementa izotopus ķīmiskais.
Šajā skolotāja stundā mēs to redzēsim masas numurs, kā to iegūt, kas tas īsti ir un kādam nolūkam to lieto.
Indekss
- Kāds ir masas numurs?
- Masas numurs un izotopi
- Kā aprēķināt masas skaitli? - Formula
Kāds ir masas numurs?
The masas numurs tas nav nekas vairāk kā protonu un neitronu summa, tas ir, visas daļiņas, kas atrodas kodolā (atcerieties, ka elektroni riņķo ap kodolu, veidojot garozu).
Masas numuru raksta ar burts a
un tas ir norādīts augšējā indeksā, vienmēr pa kreisi no simbola, kas norāda elementu, ar kuru mēs strādājam, tas ir tas ir, mēs to atradīsim kā nelielu skaitli, kas tiek novietots pa kreisi no elementa simbola augšpusē šo. Tas attēlo atoma masu, kas izmērīta u.m.a (atoma masas vienība), jo elektronu masa ir patiešām maza, tā ir tik maza, ka to var neņemt vērā vai atstāt novārtā.Atomu masu skaits parasti tiek izmantots diferencēt izotopus ķīmiskā elementa.

Attēls: Slideshare
Masas numurs un izotopi.
Izotopi ir tā paša ķīmiskā elementa varianti, kuriem ir atšķirīgs neitronu daudzums atšķiras pēc masas skaita. Izotopi dabā var būt dabiski (dabiskie izotopi) vai pilnībā cilvēku radīti (mākslīgie izotopi). Izotopu piemēri dabā ir oglekļa izotopi:
Ogleklis rodas kā trīs izotopu maisījums ar masas numuriem 12, 13 un 14: 12C, 13C un 14C.
Izotopiem ir daudz pielietojumu: tos izmanto vēža ārstēšanai, nosakot indes parādīšanos audos, piemēram, arsēnu, ķīmisko reakciju marķierus utt.
Katram no ķīmiskā elementa izotopiem var būt dažādas īpašības. Viena no pazīstamākajām un visbiežāk izmantotajām īpašībām ir pastāvīgs pussabrukšanas perioda pusperiods vai Pus dzīve. Izotopa pussabrukšanas periods ir laiks, kas nepieciešams radioizotopu sākotnējā parauga pusei kodolu sadalīšanās. Praksē izotopi mēdz sadalīties, pārejot no mazāk stabilām formām uz stabilākām formām. stabils, tāpēc to var saprast arī kā laiku, kas nepieciešams, lai pārveidotu vai pārveidotu puse atomi radioaktīvs no parauga. Oglekļa-14, kas kļūst par oglekļa-12, pussabrukšanas periods ir ļoti ilgs, un to izmanto, lai datētu senās organiskās atliekas, piemēram, fosilijas. Turpretī citu izotopu, piemēram, skābekļa-15, pussabrukšanas periods ir tikai sekundes (precīzāk - 122 sekundes).
Ūdeņraža gadījumā tā dabiskie izotopi tiem ir ļoti atšķirīgas īpašības un īpašības, tāpēc tiem ir trīs dažādi nosaukumi: parastais ūdeņradis vai protium 1H, deitērijs 2H (D) un tritijs 3H (T). Ūdeņradim ir citas mākslīgie izotopi (ūdeņradis-4, ūdeņradis-5 utt.).

Attēls: Slideshare
Kā aprēķināt masas skaitli? - Formula.
Lai aprēķiniet atoma vai jona masas numuru mums būs jāpievieno atomu skaitlis (protonu skaits atomā vai jonā, ko parasti attēlo kā "Z") un elektronu skaits.
Masas numurs (A) = atomu skaitlis (Z) + neitronu skaits (N)
TO = Z + N
Atomu skaits ir atrodams elementu periodiskajā tabulā, katra elementa augšējā kreisajā stūrī. Arī periodiskās tabulas zem elementa parādīsies masas numurs vai atomu masa.
Tāpēc, atņemot atomu skaitli no masas skaita, mēs varam zināt arī protonu skaitu.
Neitronu skaits (N) = masas numurs (A) - atomu skaitlis (Z)
N = A - Z
Piemēram, apskatot periodisko tabulu, redzēsiet, ka dzelzs masas numurs ir 55,84, tas ir, A = 56 noapaļots līdz tuvākajai vienībai; Tās atomu skaitlis (Z) ir 26, tāpēc tā neitronu skaits būs:
N = A - Z = 56-26 = 30
Ja vēlaties lasīt vairāk līdzīgus rakstus Kā iegūt masas numuru?, iesakām ievadīt mūsu kategoriju Atoms.