Moellera diagramma: kas tas ir, kā to izmanto ķīmijā un piemēri
Ķīmija var būt īpaši sarežģīta, tāpēc laipni gaidīts ir jebkurš instruments, kas atvieglo mācīšanos tiem, kuri ar to ir iepazīstināti.
Viena no populārākajām metodēm, kā iepazīt Madelunga likumu un atomu elektronu konfigurāciju, ir Moellera diagramma, grafisks mnemonisks noteikums, kas ļauj ļoti viegli redzēt, kurās orbitālēs elektroni.
Nākamais mēs atklāsim, no kā sastāv Moellera diagramma, kā tas ir saistīts ar Madelunga likumu, kā tas tiek piemērots, izmantojot dažus atrisinātus piemērus, un kuri ķīmiskie elementi neatbilst šai stratēģijai.
- Saistīts raksts: "5 ķīmisko saišu veidi: šādi veidojas matērija"
Kas ir Moellera diagramma?
Moellera diagramma, kas pazīstama arī kā lietus metode vai diagonāļu likums, ir grafiskā un mnemoniskā metode Madelunga likuma apguvei, paņēmiens ķīmisko elementu elektroniskās konfigurācijas izzināšanai un rakstīšanai.
Šo diagrammu raksturo diagonāļu zīmēšana caur orbitāļu kolonnām no augšas uz leju no labās uz kreiso pusi. Izmantojot Moellera diagrammu, tiek noteikta orbitāļu piepildījuma secība, kas tiks definēta ar trim kvantu skaitļiem: n, l un ml.
Moellera diagramma darbojas saskaņā ar sekojošo:

Katra kolonna atbilst citai orbitālei, caur kuru cirkulē atoma elektroni, subatomiskās daļiņas, kurām ir negatīvs lādiņš. Attiecīgās orbitāles ir: s, p, d un f, katrai no tām ir noteikta telpa elektronu izvietošanai un līdz ar to dažādi enerģijas līmeņi..
Ja mēs zīmējam diagonāles vai bultiņas iepriekš minētajā nozīmē, mēs iegūstam, ka pirmā orbitāle ir 1s. Otrā bultiņa sākas ar 2s orbitāli. Trešā bultiņa šķērso 2p un 3s. Ceturtā diagonāle ir 3p un 4s. Piektā diagonāle ir 3d, 4p un 5s un tā tālāk. Moellera diagramma ir ievada metode tiem, kas sāk pētīt periodiskās tabulas elementu elektroniskās konfigurācijas ķīmijā.
- Jūs varētu interesēt: "6 galvenās dabaszinātņu nozares"
Madelunga likums
Kopš Moellera diagrammas ir Madelunga noteikuma grafiskais attēlojums (dažās valstīs zināma arī kā Klečkovska valdīšana) vispirms ir jāzina, par ko ir runa. Saskaņā ar šo noteikumu atoma orbitāļu piepildīšanai ir jāievēro šādi divi noteikumi:
Madelunga pirmais noteikums
Vispirms tiek aizpildītas orbitāles ar viszemākajām vērtībām n + l, kur n ir galvenais kvantu skaitlis, bet l ir orbītas leņķiskais impulss..
Piemēram, 3d orbitāle atbilst n = 3 un l = 2. Tāpēc n + l = 3 + 2 = 5. Tā vietā 4s orbitāle atbilst n = 4 un l = 0, tāpēc n + l = 4 + 0 = 4. No tā tiek noteikts, ka elektroni vispirms aizpilda 4s orbitāli pirms 3d, jo 4s = 4, bet 3d = 5.
- Saistīts raksts: "11 ķīmisko reakciju veidi"
Madelunga otrais noteikums
Ja divām orbitālēm ir vienāda vērtība n + l, elektroni vispirms aizņems to, kuras vērtība ir mazāka.
Piemēram, 3d orbitāles vērtība ir n + l = 5, kas ir identiska 4p orbitāles vērtībai (4 + 1 = 5), bet, tā kā 3d orbitālei ir viszemākā n vērtība, tā tiks aizpildīta vispirms nekā 4p orbitāle.
No visiem šiem novērojumiem un noteikumiem var iegūt šādu secību atomu orbitāļu aizpildīšanā: 1s 2s 2p 3s 3p 4s 3d 4p. Lai gan šī secība ir fiksēta, atcerēties to no galvas ir sarežģīti, tāpēc ir Moellera diagramma, kas grafiski attēlo tās secību.
- Jūs varētu interesēt: "9 Daltona atomu teorijas postulāti"
Darbības, kas jāievēro, izmantojot Moellera diagrammu
Kā mēs komentējām iepriekšējā sadaļā, Madelunga noteikums izmanto formulu n + l, lai noteiktu, ko orbitāles tiek aizpildītas pirms un no tā nosaka, kāda ir elementa elektroniskā konfigurācija noteikts. Tomēr Moellera diagramma to jau attēlo grafiski un vienkārši, tāpēc pietiek sekot līdzi vienas diagrammas kolonnas un uzzīmējiet diagonāles, lai noskaidrotu, kādā secībā katras orbitāles elements.
Lai atklātu atoma elektronisko konfigurāciju un to, kurās orbitālēs atrodas tā elektroni, mums vispirms jāzina tā atomskaitlis Z. Skaitlis Z atbilst elektronu skaitam atomā, ja vien šis atoms ir neitrāls vai tas pats, ka tas nav jons, ne pozitīvs (katjons), ne negatīvs (anjons).
Tādējādi, zinot neitrāla atoma Z, mēs jau zinām, cik elektronu parasti ir šī elementa neitrālajam atomam. Paturot to prātā, mēs sāksim zīmēt Moellera diagrammas diagonāles. Jāņem vērā, ka katram orbitāla veidam ir atšķirīga spēja izvietot elektronus, kuri ir:
- s = 2 elektroni
- p = 6 elektroni
- d = 10 elektroni
- f = 14 elektroni
Tas apstājas pie orbitāles, kur ir aizņemts pēdējais elektrons, ko dod Z.
Moellera diagrammu piemēri
Lai labāk izprastu, kā darbojas Moellera diagramma, tālāk mēs redzēsim dažus praktiskus piemērus dažādu elementu elektronu konfigurācijas iestatīšanai.
Berilijs
Lai noteiktu neitrāla berilija (Be) atoma elektronisko konfigurāciju, vispirms tas ir jāmeklē periodiskajā tabulā, sārmzeme, kas atrodas tabulas otrajā kolonnā un otrajā rindā. Tā atomskaitlis ir 4, tāpēc Z = 4 un tajā ir arī 4 elektroni.
Ņemot to visu vērā, mēs izmantosim Moellera diagrammu, lai redzētu, kā atrodas šī elementa 4 elektroni. Mēs sākam, veidojot diagonāles iepriekš minētajā nozīmē, no augšas uz leju un no labās uz kreiso pusi.
Kad mēs piepildām orbitāles, Katrā no tiem atrasto elektronu skaitu ieteicams likt augšindeksā. Tā kā 1s ir pirmā orbitāle un tā aizņem divus elektronus, mēs to rakstīsim:

Tā kā mums joprojām ir brīvi elektroni, mēs turpinām aizpildīt orbitāles. Nākamā ir 2s orbitāle un, tāpat kā ar 1s, tā aizņem 2 elektronus, tāpēc 2s2. Tā kā mums jau ir visi elektroni, kas labi atrodas Be neitrālā atoma orbitālēs, mēs varam teikt, ka šī elementa elektroniskā konfigurācija ir:

Mēs pārliecināmies, ka esam labi pastrādājuši, pievienojot augšējos indeksus: 2 + 2 = 4
- Jūs varētu interesēt: "Molekulārā kinētiskā teorija: 3 matērijas stāvokļi"
Match
Elements fosfors (P) ir nemetāls, kas atrodams periodiskās tabulas trešajā rindā un 16. ailē., ar Z = 15, tāpēc tajā kopā ir 15 elektroni, kuriem jāieņem orbitāles.
Redzot iepriekšējo piemēru, mēs varam virzīties mazliet uz priekšu un atrast 4 tā elektronus tajās pašās orbitālēs, kas ir berilija 4 elektroniem, trūkst 9 elektronu plus.

Pēc 2s orbitāles nākamā diagonāle ieiet 2p orbitālē un beidzas pie 3s orbitāles. 2p orbitāle var aizņemt 6 elektronus, bet 3s gadījumā tikai 2. Tādējādi mums būtu:
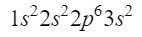
Šobrīd mums ir labi izvietoti 12 elektroni, bet mums vēl ir priekšā vēl 3. Mēs izveidojam vēl vienu diagonāli un šoreiz ieejam caur 3p orbitāli saskaņā ar Moellera diagrammu, orbitāli, kurā ir vieta 6 elektroniem, bet tā kā mums ir palikuši tikai 3 elektroni, šī orbitāle nebūs pilnībā aizņemta, liekot 3 kā augšējo indeksu. Tādējādi, lai izbeigtu fosforu, tā elektroniskā konfigurācija ir šāda:

Mēs pārliecināmies, ka esam pastrādājuši labi, pievienojot augšējos indeksus: 2 + 2 + 6 + 2 + 3 = 15
Cirkonijs
Elements cirkonijs (Zr) ir pārejas metāls, kas atrodams 4. ailē un 5. rindā, un tā Z = 40. Saīsinot ceļu, izmantojot iepriekšējā piemēra priekšrocības, mēs varam atrast pirmos 18 elektronus.
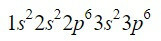
Pēc 3p orbitāles nākamās, kas jāaizpilda, vadoties pēc Moellera diagrammas, ir 4s, 3d, 4p un 5s orbitāles ar attiecīgi 2, 10, 6 un 2 elektronu ietilpību.

Pabeidzot pirmās deviņas orbitāles diagrammā, kopā tiek pievienoti 20 elektroni, atstājot 2 atlikušos elektronus, kas atrodas nākamajā orbitālē, 4d. Tādējādi neitrālā elementa cirkonija elektronu konfigurācija ir:
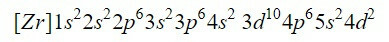
Mēs pārliecināmies, ka esam strādājuši labi, pievienojot augšējos indeksus: 2 + 2 + 6 + 2 + 6 + 2 + 10 + 6 + 2 + 2 = 40
Skābeklis
Šeit mēs redzam nedaudz sarežģītāku piemēru, kas ir skābeklis (O). Šī gāze ir atrodama periodiskās tabulas 16. ailē un 2. rindā, tā ir nemetāla, un tās atomskaitlis ir 8.
Līdz šim, aplūkojot citus piemērus, mēs varētu domāt, ka tā Z = 8, taču tas nav tik vienkārši, jo šai gāzei ir īpašs raksturs, gandrīz vienmēr tā ir jona formā ar lādiņu -2.
Tas nozīmē, ka, lai gan neitrālajam skābekļa atomam ir 8 elektroni, kā norāda tā atomskaitlis, tam ir Taisnība, ka dabā tam ir vairāk, savā gadījumā 10 (8 elektroni + 2 elektroni vai, ja vēlaties, -8 lādiņi elektriskā -2).
Tātad šajā gadījumā elektronu skaits, kas mums jāatrod orbitālēs, ir nevis 8, bet 10 elektroni, it kā mēs atrastu ķīmiskā elementa neona elektronus, kuriem ir Z = 10.
To saprotot, mums tikai jādara tas pats, ko mēs darījām iepriekšējos gadījumos, tikai ņemot vērā to, ka mēs strādājam ar jonu (anjonu):
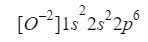
Mēs pārliecināmies, ka esam pastrādājuši labi, pievienojot augšējos indeksus: 2 + 2 + 6 = 10
Kalcijs
Ar kalciju (Ca) notiek kaut kas līdzīgs skābeklim, tikai šajā gadījumā mēs runājam par katjonu, tas ir, jonu ar pozitīvu lādiņu.
Šis elements ir atrodams periodiskās tabulas 2. ailē 4. rindā ar atomskaitli 20, tomēr Daba parasti tiek pasniegta jona formā ar pozitīvu lādiņu +2, kas nozīmē, ka tā elektroniskais lādiņš ir 18 (- 20 + 2 = 18; 20 elektroni - 2 elektroni = 18 elektroni).
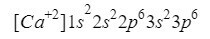
Mēs pārliecināmies, ka esam pastrādājuši labi, pievienojot augšējos indeksus: 2 + 2 + 6 + 2 + 6 = 18
Izņēmumi no Moellera diagrammas un Madelunga noteikuma
Lai gan Moellera diagramma ir ļoti noderīga, lai izprastu Madelunga likumu un zinātu, kā atrodas dažādu ķīmisko elementu elektroni, patiesība ir tāda, ka tā nav nekļūdīga. Ir noteiktas vielas, kuru sastāvs neatbilst mūsu skaidrotajam.
Viņu elektronu konfigurācijas eksperimentāli atšķiras no Madelunga noteikuma prognozētajām kvantu iemeslu dēļ.. Starp šiem elementiem, kas neatbilst standartiem, mums ir: hroms (Cr, Z = 24), varš (Cu, Z = 29), sudrabs (Ag, Z = 47), rodijs (Rh, Z = 45), cērijs ( Ce, Z = 58), niobijs (Nb; Z = 41), cita starpā.
Izņēmumi ir ļoti bieži, aizpildot d un f orbitāļus. Piemēram, hroma gadījumā, kura valences konfigurācijai jābūt 4s ^ 2 3d ^ 4 saskaņā ar Moellera diagrammu un Madelunga likumu, tā valences konfigurācija faktiski ir 4s ^ 1 3d ^ 5. Vēl viens dīvains piemērs ir sudraba piemērs, kuram tā vietā, lai 5s ^ 2 4d ^ 9 būtu pēdējais, ir 5s ^ 1 4d ^ 10.
