Estrutura e características do átomo

Imagem: SlidePlayer
Os átomos fazem parte do nosso mundo. Toda matéria é feita de átomos, por isso é importante entender melhor em que consistem e quais são suas funções. Nesta lição de um PROFESSOR, vamos dizer a você o que estrutura de um átomo e características. Se você quiser saber mais sobre as partículas que constituem toda a matéria, continue lendo este artigo.
Índice
- O que são átomos?
- Estrutura do átomo
- Principais características do átomo
- O que são isótopos?
- Como os átomos são encontrados na natureza?
O que são átomos?
O átomo isso é a menor unidade em que a matéria pode ser dividida sem perder suas propriedades químicas, ou seja, suas propriedades como elemento químico. O átomo é a origem de tudo que pode ser visto ou tocado, desde as estrelas até o café da manhã.
Se deixarmos de lado a perda de suas propriedades químicas, podemos dizer que o átomo é composto por diferentes partículas, chamadas de partículas subatômicas. Existem três tipos de partículas subatômicas -prótons, nêutrons e elétrons- com características diferentes.
Essas partículas são agrupadas em números diferentes para formar os elementos químicos (oxigênio, carbono, etc.), mas sempre serão distribuídas seguindo uma estrutura fixa.

Imagem: Google Sites
Estrutura do átomo.
A estrutura do átomo é fixa, isto é, podemos ter diferentes tipos de átomos (o átomo de hidrogênio, o átomo de oxigênio, etc.), mas suas partículas subatômicas são sempre organizadas de maneira semelhante a um sistema planetário.
Você certamente se lembrará de como o sistema solar está organizado: o Sol está no centro e ao redor a partir disso, os planetas giram descrevendo diferentes órbitas, algumas mais próximas e outras mais distantes do Sol. No caso dos átomos, no centro está o testemunho, com uma forma semelhante a uma amora-preta e é composta por nêutrons e os prótons.
Em torno do núcleo está o Córtex que é a área através da qual o elétrons. Anteriormente, pensava-se que os elétrons descreviam certas órbitas, semelhantes a como os planetas fazem, embora agora seja sabe que essas órbitas não são tão bem definidas e são mais como áreas em que é mais provável que nos encontremos elétrons.
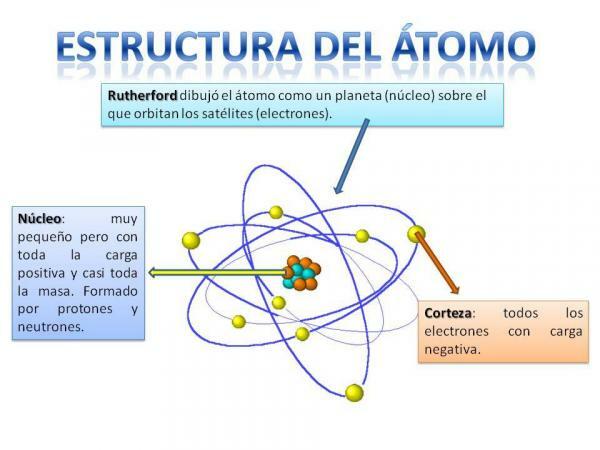
Imagem: REA - Plano Ceibal
Principais características do átomo.
Para continuar com esta lição sobre a estrutura e as características do átomo, é importante enfocar os elementos que fazem um átomo ser considerado como tal.
E para isso temos que responder a esta pergunta: por que todos os átomos decidem se ordenar daquela maneira? A resposta é simples: é devido a forças atrativas elétricas. O núcleo do átomo é formado por nêutrons, que não possuem carga elétrica, e prótons, que possuem carga elétrica positiva. e os elétrons têm carga elétrica negativa, então há uma força atrativa semelhante entre o núcleo e os elétrons produzido entre os dois pólos de um ímã, mas não é forte o suficiente para que os elétrons "caiam" para o testemunho.
Isso é melhor compreendido se levarmos em consideração o tamanho do núcleo: se o átomo tivesse, por exemplo, a dimensão de um estádio de futebol, o núcleo teria a dimensão da bola no centro do campo Quanta força de atração a bola de futebol teria de fazer para que as arquibancadas do estádio caíssem sobre ela!
A função dos nêutrons
Agora você deve estar se perguntando: qual é o papel dos nêutrons? Apesar de não terem carga elétrica, os nêutrons desempenham um grande papel dentro do átomo: contribuem com 99% da massa. Se te ajudar a lembrar, podemos dizer que um átomo é como uma gangue de três amigos: os pesados nêutron, o próton positivo e o elétron negativo, que gira e gira o nêutron e elétron.
O movimento dos elétrons
Neste ponto, quero que voltemos a algo que deixamos no tinteiro: as órbitas que os elétrons descrevem em torno do núcleo. Nós tínhamos dito isso elétrons giram em torno do núcleo Como os planetas ao redor do Sol, alguns mais próximos do que outros, por que eles fazem isso? Os elétrons giram em uma camada ou outra de acordo com a energia que têm para se afastar do núcleo, ou seja, aqueles elétrons que estão mais próximos do núcleo não têm a força suficiente para se mover para longe do núcleo, enquanto aqueles nas camadas mais externas (orbitais) da crosta têm mais energia e foram capazes de se mover para longe do núcleo. testemunho. Além disso, em cada um dos orbitais, há uma capacidade máxima de 8 elétrons (regra do octeto).
As partículas de um átomo
Vamos voltar a outra abordagem que fizemos anteriormente, mas não explicamos: os átomos são feitos de nêutrons, prótons e elétrons, que sempre se combinam seguindo a mesma estrutura de núcleo e crosta, mas o fazem em números diferentes para formar os diferentes elementos químicos. Como podemos obter tantos elementos combinando apenas 3 tipos de partículas? Os elementos químicos, que você já viu representados na tabela periódica, são caracterizados por terem um certo número atômico.
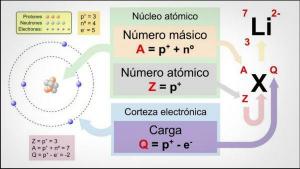
O número atômico (Z) Indica o número de prótons no núcleo desse tipo de átomo, que é igual ao número de elétrons em condições normais. Assim, por exemplo, todos os átomos que têm 6 prótons (Z = 6) serão átomos de carbono e terão as mesmas propriedades químicas; os átomos com 5 prótons (Z = 5) serão átomos de boro, com as mesmas propriedades químicas entre si e diferentes das dos átomos de carbono. Você não tem que confundir número atômico com peso atômico ou número de massa (A), que é a soma do peso dos nêutrons e prótons (o peso dos elétrons é desprezível em relação ao peso do núcleo total).

Imagem: SlidePlayer
O que são isótopos?
Na natureza, podemos encontrar diferentes "subtipos" de elementos, o isótopos. Tenho certeza de que em algum momento você ouviu falar do carbono 14, um isótopo radioativo do carbono usado para determinar, entre outras coisas, a idade dos fósseis. Isótopos são dois átomos com o mesmo número de prótons (o mesmo número atômico), mas número diferente de nêutrons, (massa atômica diferente). Os isótopos do mesmo elemento são geralmente nomeados com o nome do elemento seguido de sua massa atômica.
Em nosso exemplo, ambos os isótopos são de carbono, então eles têm um número atômico de 6 (Z = 6), mas o carbono 12 (carbono “normal”) tem um peso atômico de 12 versus o peso atômico do carbono 14 14. Os isótopos do mesmo elemento têm propriedades físicas e químicas muito semelhantes. No caso do carbono 14, ao contrário do carbono 12, é um isótopo radioativo que está presente em todos os elementos que contêm carbono, incluindo os seres vivos.
E com isso encerramos esta lição sobre a estrutura do átomo e suas características. Esperamos que tenha ajudado você.

Imagem: Suas Tarefas
Como os átomos são encontrados na natureza?
Os átomos podem ser encontrados isoladamente, mas o mais normal é encontrá-los combinados em grupos chamado moléculas.
As moléculas podem ser constituídas por átomos do mesmo elemento (como a molécula de oxigênio, composta por dois átomos de oxigênio) ou por grupos com átomos de elementos diferentes (dois átomos de hidrogênio e um de oxigênio formam a molécula de Água). Esses grupos de elementos são chamados de moléculas, que por sua vez podem ser combinadas entre si e formando diferentes agrupamentos cada vez mais complexos de acordo com sua reatividade e sua afinidade química para meio de ligações químicas.
Se você quiser ler mais artigos semelhantes a Estrutura e características do átomo, recomendamos que você insira nossa categoria de O átomo.