Glutamat (neurotransmițător): definiție și funcții
glutamat mediază cele mai multe sinapse excitatorii din sistemul nervos central (SNC). Este principalul mediator al informațiilor senzoriale, motorii, cognitive și emoționale și este implicat în formarea amintirilor și recuperarea lor, fiind prezent în 80-90% din sinapsele creierului.
Ca și cum toate acestea ar fi puțin merite, ele intervin și în neuroplasticitate, în procesele de învățare și este precursorul GABA –Neurotransmițătorul principal inhibitor al SNC. Ce mai poți cere unei molecule?
Ce este glutamatul?
Eventual a fost unul dintre cei mai studiați neurotransmițători din sistemul nervos. În ultimii ani, studiul său a crescut datorită relației sale cu diverse patologii neurodegenerative (cum ar fi boala Alzheimer), care l-a transformat într-o țintă puternică de droguri în diferite boli.
De asemenea, merită menționat faptul că, având în vedere complexitatea receptorilor săi, acesta este unul dintre cei mai complicați neurotransmițători de studiat.
Procesul de sinteză
Procesul de sinteză a glutamatului începe în ciclul Krebs sau în ciclul acidului tricarboxilic. Ciclul Krebs este o cale metabolică sau, pentru noi să înțelegem,
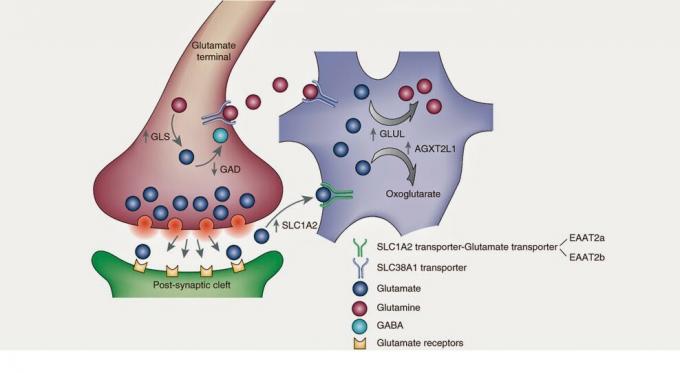
o succesiune de reacții chimice pentru a produce respirația celulară în mitocondrii. Un ciclu metabolic poate fi înțeles ca mecanismul unui ceas, în care fiecare angrenaj îndeplinește un funcția și simpla defecțiune a unei piese pot provoca sau nu deteriorarea ceasului ora. Ciclurile din biochimie sunt aceleași. O moleculă, prin reacții enzimatice continue - angrenajele ceasului -, își schimbă forma și compoziția pentru a da naștere unei funcții celulare. Precursorul principal al glutamatului va fi alfa-cetoglutaratul, care va primi o grupare amino prin transaminare pentru a deveni glutamat.De asemenea, merită menționat un alt precursor destul de semnificativ: glutamina. Când celula eliberează glutamat în spațiul extracelular, astrocitele - un tip de celulă glial - recuperați acest glutamat care, printr-o enzimă numită glutamină sintetază, va deveni glutamina. Mai tarziu, glutamina este eliberată de astrocite, care este recuperată de neuroni pentru a fi transformată înapoi în glutamat. Și, probabil, mai mulți vor întreba următoarele: Și dacă trebuie să returneze glutamina la glutamat în neuron, de ce astrocitul transformă glutamatul sărac în glutamină? Ei bine, nici eu nu știu. Poate că astrocitele și neuronii nu sunt de acord sau poate că Neuroștiințe Este atât de complicat În orice caz, am vrut să fac o revizuire a astrocitelor, deoarece colaborarea lor reprezintă 40% din cifra de afaceri glutamat, ceea ce înseamnă că cea mai mare parte a glutamatului este recuperată de aceste celule gliale.
Există alți precursori și alte căi prin care se recuperează glutamatul care este eliberat în spațiul extracelular. De exemplu, există neuroni care conțin un transportor specific de glutamat –EAAT1 / 2– care recuperează direct glutamatul la nivelul neuronului și permit terminarea semnalului excitator. Pentru un studiu suplimentar al sintezei și metabolismului glutamatului, vă recomand să citiți bibliografia.
Receptorii glutamatului
După cum ne învață de obicei, fiecare neurotransmițător are receptorii săi pe celula postsinaptică. Receptorii, localizați pe membrana celulară, sunt proteine de care se leagă un neurotransmițător, hormonul neuropeptidă etc., pentru a da naștere la o serie de modificări ale metabolismului celular al celulei în care se află receptorul. În neuroni, în general, plasăm receptorii pe celulele postsinaptice, deși nu trebuie să fie așa.
De asemenea, ne învață de obicei în primul an că există două tipuri principale de receptori: ionotrop și metabotrop. Ionotropele sunt acelea în care atunci când ligandul lor - „cheia” receptorului - se leagă, deschid canale care permit trecerea ionilor în celulă. Metabotropii, pe de altă parte, atunci când ligandul se leagă, provoacă modificări în celulă prin al doilea mesager. În această recenzie voi vorbi despre principalele tipuri de receptori ionotropi de glutamat, deși recomand studierea literaturii pentru a înțelege receptorii metabotropi. Iată principalii receptori ionotropi:
- Receptor NMDA.
- Receptor AMPA.
- Kainado catcher.
Receptorii NMDA și AMPA și relația lor strânsă
Se crede că ambele tipuri de receptori sunt macromolecule formate din patru domenii transmembranare - adică sunt formate din patru subunități care traversează bistratul lipidic al membranei celulare - și ambii sunt receptori de glutamat care vor deschide canale de cationi - ioni încărcați pozitiv. Dar chiar și așa, acestea sunt semnificativ diferite.
Una dintre diferențele lor este pragul la care sunt activate. În primul rând, receptorii AMPA se activează mult mai rapid; în timp ce receptorii NMDA nu pot fi activați până când neuronul nu are un potențial de membrană de aproximativ -50mV - un neuron atunci când este inactivat este de obicei în jur de -70mV-. În al doilea rând, pasul cationilor va fi diferit în fiecare caz. Receptorii AMPA vor realiza potențiale de membrană mult mai mari decât receptorii NMDA, care vor colabora mult mai modest. În schimb, receptorii NMDA vor realiza activări mult mai susținute în timp decât receptorii AMPA. Prin urmare, cele din AMPA se activează rapid și produc potențiale excitatorii mai puternice, dar se dezactivează rapid. Și cei din NMDA își iau timp să se activeze, dar reușesc să mențină potențialul de excitare pe care îl generează mult mai mult.
Pentru a o înțelege mai bine, să ne imaginăm că suntem soldați și că armele noastre reprezintă diferiții receptori. Să ne imaginăm că spațiul extracelular este o tranșee. Avem două tipuri de arme: revolver și grenade. Grenadele sunt simple și rapide de utilizat: scoateți inelul, îl aruncați și așteptați să explodeze. Au mult potențial distructiv, dar odată ce le-am aruncat pe toate, s-a terminat. Revolverul este o armă care necesită timp pentru încărcare, deoarece trebuie să scoateți tamburul și să puneți gloanțele unul câte unul. Dar, odată ce l-am încărcat, avem șase fotografii cu care putem supraviețui o vreme, deși cu mult mai puțin potențial decât o grenadă. Revolverele noastre cerebrale sunt receptori NMDA, iar grenadele noastre sunt receptori AMPA.
Excesele de glutamat și pericolele acestora
Ei spun că în exces nimic nu este bun și în cazul glutamatului este îndeplinit. Atunci vom cita câteva patologii și probleme neurologice în care este legat un exces de glutamat.
1. Analogii glutamatului pot provoca exotoxicitate
Medicamentele analoage glutamatului - adică îndeplinesc aceeași funcție ca glutamatul - cum ar fi NMDA - căruia receptorul NMDA își datorează numele - poate provoca efecte neurodegenerative la doze mari în cele mai vulnerabile regiuni ale creierului precum nucleul arcuat al hipotalamusului. Mecanismele implicate în această neurodegenerare sunt diverse și implică diferite tipuri de receptori de glutamat.
2. Unele neurotoxine pe care le putem ingera în dieta noastră exercită moartea neuronală prin excesul de glutamat
Diferite otrăvuri ale unor animale și plante își exercită efectele prin căile nervoase glutamate. Un exemplu este otravă din semințele Cycas Circinalis, o plantă otrăvitoare pe care o putem găsi pe insula Guam din Pacific. Această otravă a provocat o prevalență ridicată a Scleroza laterala amiotrofica pe această insulă unde locuitorii săi au ingerat-o zilnic, crezând că este benignă.
3. Glutamatul contribuie la moartea neuronală ischemică
Glutamatul este principalul neurotransmițător în tulburările acute ale creierului, cum ar fi infarctul, stop cardiac, hipoxie pre / perinatală. În aceste evenimente în care există o lipsă de oxigen în țesutul cerebral, neuronii rămân într-o stare de depolarizare permanentă; datorită diferitelor procese biochimice. Acest lucru duce la eliberarea permanentă a glutamatului din celule, cu activarea susținută ulterioară a receptorilor de glutamat. Receptorul NMDA este permeabil în special calciului în comparație cu alți receptori ionotropi, iar excesul de calciu duce la moartea neuronală. Prin urmare, hiperactivitatea receptorilor glutamatergici duce la moartea neuronală din cauza creșterii calciului intraneuronal.
4. Epilepsie
Relația dintre glutamat și epilepsie este bine documentată. Activitatea epileptică este considerată a fi în special legată de receptorii AMPA, deși pe măsură ce epilepsia progresează, receptorii NMDA devin importanți.
Glutamatul este bun? Glutamatul este rău?
De obicei, când cineva citește acest tip de text, el ajunge să umanizeze moleculele punând etichete pe ele ca „bune” sau „rele” - care are un nume și se numește antropomorfism, foarte la modă în epoca medievală. Realitatea este departe de aceste judecăți simpliste.
Într-o societate în care am generat un concept de „sănătate” este ușor ca unele dintre mecanismele naturii să ne deranjeze. Problema este că natura nu înțelege „sănătatea”. Am creat acest lucru prin medicină, industrii farmaceutice și psihologie. Este un concept social și, ca toate conceptele sociale, este supus progresului societăților, fie că este uman sau științific. Progresele arată că glutamatul este asociat cu o serie de patologii precum Alzheimer sau Schizofrenie. Acesta nu este un ochi malefic al evoluției pentru ființa umană, ci mai degrabă este o nepotrivire biochimică a unui concept pe care natura încă nu îl înțelege: societatea umană din secolul XXI.
Și ca întotdeauna, de ce să studiezi acest lucru? În acest caz, cred că răspunsul este foarte clar. Datorită rolului pe care glutamatul îl are în diferite patologii neurodegenerative, rezultă o țintă farmacologică importantă - deși complexă -. Câteva exemple ale acestor boli, deși nu am vorbit despre ele în această recenzie, deoarece consider că o intrare ar putea fi scrisă exclusiv despre aceasta, sunt boala Alzheimer și Schizofrenie. Subiectiv, găsesc căutarea de noi medicamente pentru schizofrenie din două motive principale: prevalența acestei boli și costul asistenței medicale poartă; și efectele adverse ale antipsihoticelor actuale, care în multe cazuri împiedică aderarea la terapie.
Text corectat și editat de Frederic Muniente Peix
Referințe bibliografice:
Cărți:
- Siegel, G. (2006). Neurochimie de bază. Amsterdam: Elsevier.
Articole:
- Citri, A. & Malenka, R. (2007). Plasticitatea sinaptică: forme, funcții și mecanisme multiple. Neuropsihofarmacologie, 33 (1), 18-41. http://dx.doi.org/10.1038/sj.npp.1301559
- Hardingham, G. & Bading, H. (2010). Semnalizarea receptorului Naptă sinaptică versus extrasinaptică: implicații pentru tulburările neurodegenerative. Nature Reviews Neuroscience, 11 (10), 682-696. http://dx.doi.org/10.1038/nrn2911
- Hardingham, G. & Bading, H. (2010). Semnalizarea receptorului Naptă sinaptică versus extrasinaptică: implicații pentru tulburările neurodegenerative. Nature Reviews Neuroscience, 11 (10), 682-696. http://dx.doi.org/10.1038/nrn2911
- Kerchner, G. & Nicoll, R. (2008). Sinapse silențioase și apariția unui mecanism postsinaptic pentru LTP. Nature Reviews Neuroscience, 9 (11), 813-825. http://dx.doi.org/10.1038/nrn2501
- Papouin, T. & Oliet, S. (2014). Organizarea, controlul și funcționarea receptorilor NMDA extrasinaptici. Tranzacții filozofice ale Societății Regale B: Științe biologice, 369 (1654), 20130601-20130601. http://dx.doi.org/10.1098/rstb.2013.0601
