Части атома и их характеристики
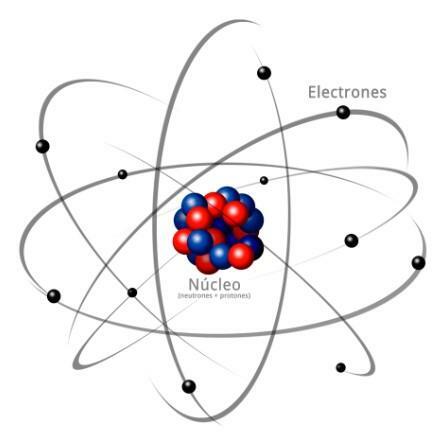
Изображение: Answers.tips
Атомы - это основные элементы, которые форма материи, присутствуя во всех состояниях материи. Это очень маленькие элементы, которые невозможно увидеть человеческим глазом, но они действительно важны для нашей Вселенной. Чтобы лучше понять, что такое атомы и как они работают, в этом уроке УЧИТЕЛЯ мы поговорим о части атома и их характеристики.
Все атомы состоят из сердцевина и корочка. Ядро, как указывает его название, является центральной частью атома, где находятся частицы с положительным зарядом, которые называются протоны, а частицы с нейтральным зарядом, т. е. не имеют электрического заряда, получив название нейтроны. Масса обеих частиц, как протонов, так и нейтронов, одинакова. Все атомы одного и того же химического элемента имеют равное количество протонов, получая это число как название атомного номера и используя букву Z для его обозначения.
С другой стороны, есть Кора Что это внешняя часть атома. В коре мы находим электроны, которые являются отрицательно заряженными частицами. Электроны вращаются с большой скоростью вокруг ядра на разных уровнях, будучи частицами намного меньшими, чем те, что находятся в ядре.
Будучи нейтральными нейтронами, положительными протонами и отрицательными электронами, атом имеет нейтральный электрический заряд, поскольку у них такое же количество протонов, как и у электронов. Хотя бывают случаи, когда электронов меньше или больше, чем протонов, что вызывает заряд атом отрицательный или положительный, в этом случае он получает название ион, анион, если он отрицательный, или катион, если он положительный.
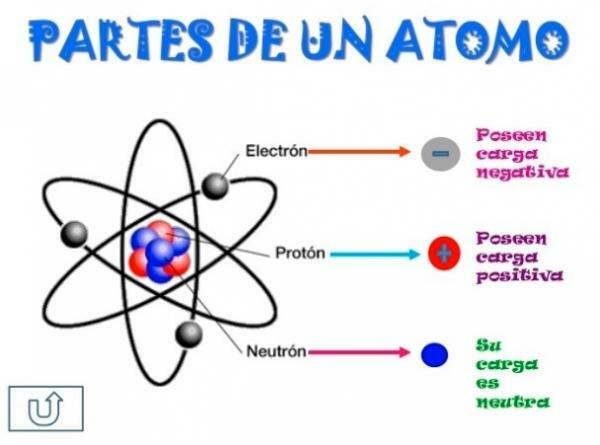
Изображение: Brainly
Чтобы продолжить этот урок о частях атома и их характеристиках, мы должны поговорить об эволюции, которую претерпели части атома с тех пор, как атомная модель со временем изменилась благодаря исследованиям ученых. Следует отметить, что некоторые модели, которые мы собираемся объяснить, устарели и не используются. в настоящее время, но они необходимы для понимания эволюции научного сообщества по этому вопросу.
Историческая эволюция атомной модели характеризуется следующие ученые:
- Модель Дальтона: Первая атомная модель была работой Джона Далтона в 1803 году. Это очень примитивная модель, в которой отсутствуют многие элементы, такие как наличие электронов и протонов.
- Модель Томсона: Джону Томсону удалось создать более полную модель атома, чем модель Далтона, добавив несколько ключевых элементов. Томсон обнаружил существование электронов, а также положительных и отрицательных зарядов.
- Модель Нагаока: Японский физик Нагаока не согласился с моделью Томсона, он считал, что атом должен иметь большое положительно заряженное ядро, на котором вращаются отрицательно заряженные электроны. Его теория называется сатурнианской, поскольку он сравнил электроны с кольцами Сатурна. Часто эта модель не называется, но важно понимать, какой большой шаг был сделан в настоящее время.
- Модель Резерфорда: Модель Резерфорда основана на существовании положительно заряженного ядра, на котором вращаются отрицательно заряженные электроны. Эта модель очень похожа на модель Нагаока, будучи очень близких лет, хотя японская модель более ранняя.
- Модель Бора: Бор считал, что электроны должны находиться далеко от слоистого ядра и число этих орбитальных частиц должно быть равно атомному номеру. Его модель также понимает, что количество электронов варьируется в каждой оболочке, причем в первой оболочке меньше электронов, чем в последней.
- Модель Шредингера: Шредингер разрушил представление о том, что электроны - это крошечные частицы, вращающиеся вокруг ядра. Австрийский ученый утверждал, что электроны перемещаются посредством волновой функции, то есть посредством орбитальная форма.
- Модель Дирака: Дирак модифицировал идеи Шредингера для своей модели, используя «уравнение Дирака», чтобы дать более правильное представление об орбитальной форме электронов.