Узнайте, как ПРОСТО И ПРАКТИЧНО организован ПЕРИОДИЧЕСКИЙ ТАБЛИЦА

Изображение: ptable.com
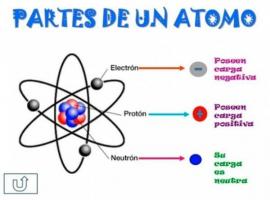
В 1869 году русский химик Дмитрий Иванович Менделеев разработал способ классифицировать все химические элементы которые появляются в природе. Этот метод классификации - периодическая таблица, и многие называют ее «сердцем химии». В периодической таблице было всего 63 химических элемента, но, когда они были обнаружены, в ее ряды были добавлены многочисленные химические элементы.
В этом уроке УЧИТЕЛЯ мы рассмотрим как устроена таблица Менделеева, видя, какие критерии соблюдаются при помещении различных элементов в поля этой таблицы.
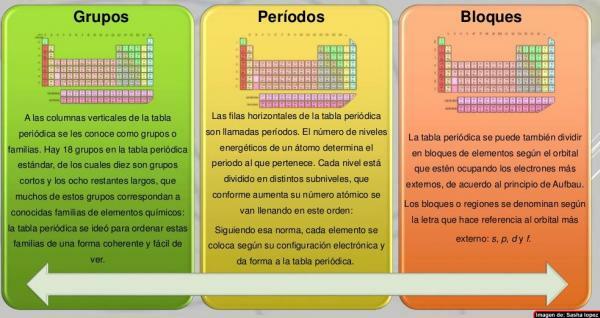
В столбцы периодической таблицы их назвали группами. В настоящее время в обычно используемой таблице Менделеева, то есть стандартной, насчитывается 18 групп, пронумерованных слева направо от 1 до 18. Этот способ наименования группы (номенклатура) может варьироваться: иногда используется смешанная номенклатура римских цифр и букв, в других случаях группы имеют общие названия (металлы щелочи, галогены, благородные газы и т. д.), а в других они называются «группой ...» и именем ее первого члена (например, «группа скандия» для группы 3).
Элементы одной группы могут иметь паттерны разного свойства:
- Увеличение атомного радиуса, сверху вниз в группе. По мере того, как мы опускаемся в периодической таблице, количество электронов увеличивается, а следовательно, и количество заполненных ими оболочек. Следовательно, электроны в последней оболочке (валентной оболочке) находятся дальше от ядра, а атомы становятся все больше и больше, то есть имеют больший радиус.
- Сверху каждый элемент имеет меньшая энергия ионизации. Поскольку электронов больше, они находятся в валентной оболочке дальше от ядра и, следовательно, Это привлекает их с меньшей силой, облегчая удаление электронов по мере того, как мы спускаемся по столу. периодический.
- Наконец, мы также наблюдаем уменьшение электроотрицательности внутри одной группы. Опять же, по мере того, как расстояние между валентными электронами и ядром увеличивается, электроны других атомов изменяются. дальше от силы притяжения ядра, и поэтому он притягивает их с меньшей силой, чем атомы меньшего размера (группы выше).
Эти закономерности являются тенденциями, то есть есть определенные исключения, такие как то, что происходит в группе 11, где электроотрицательность возрастает дальше по группе. Более того, в некоторых частях периодической таблицы, таких как блоки d и f, горизонтальное сходство между элементами одной и той же группы не так сильно выражено.

Изображение: Исследовательская библиотека
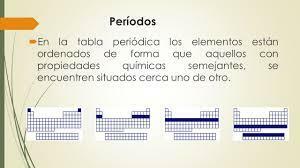
Семь горизонтальных рядов таблицы Менделеева называются периоды. Количество энергетических уровней атома определяет период, к которому он принадлежит. Каждый уровень разделен на разные категории, называемые оболочками или электронными орбиталями, которые могут быть типа s, p, d и f.
Как то, что произошло в группах, предметы того же периода имеют похожие модели атомный радиус, энергия ионизации, сродство к электрону и электроотрицательность:
- В какой-то период атомный радиус обычно она снижается, если мы перемещаемся вправо по периодической таблице. Когда мы переходим от одного элемента к другому, протоны и электроны добавляются, заставляя их электроны втягиваются в ядро (помните, что электроны слишком легкие для силы притяжения основной).
- Уменьшение атомного радиуса за тот же период приводит к увеличению энергия ионизации и электроотрицательность увеличивается слева направо, так как притяжение, которое ядро оказывает на электроны, увеличивается.
- В Электронная близость он также показывает закономерность за период, хотя и более мягкую. Металлы, которые находятся слева от периодической таблицы, обычно имеют более низкое сродство, чем неметаллы, которые находятся справа от периода. Это общее правило и неверно для благородных газов, последний слой которых (валентный слой) заполнен, и поэтому они очень слабо реактивны.
Изображение: SlidePlayer
Элементы таблицы Менделеева можно разделить в блоках в соответствии с порядком сборки электронных оболочек элементов. Каждый блок назван в соответствии с последнийорбиталь, на которой, по идее, находится последний электрон (s, p, d или f):
- Блок s Он состоит из первых двух групп, водорода и гелия.
- Блок p Он состоит из последних шести групп (группы с 13 по 18).
- Блок d Он состоит из групп с 3 по 12 (обычно называемых переходными металлами).
- Блок f, который обычно помещается отдельно под остальной частью таблицы Менделеева, не имеет номеров групп и состоит из лантаноидов и актинидов.
Периодическая таблица элементов сохранилась столько лет, потому что это система, которая оказалась очень полезной, и, прежде всего, потому, что ее можно обновлять. Теоретически могло быть больше элементов, которые могли бы заполнить другие орбитали, но они еще не синтезированы или не открыты. В случае обнаружения новых атомных элементов исследователи продолжали бы в алфавитном порядке называть различные блоки (блок g, блок h и т. Д.).
Изображение: Educando, Доминиканский образовательный портал