Značilnosti skupin PERIODIČNE MIZE
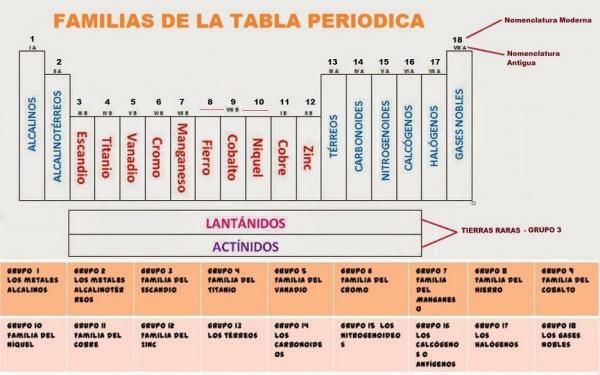
Slika: Naravoslovje
The periodni sistem elementov naroči vse kemični elementi doslej znano. Čeprav se zdi drugače, so ti elementi razporejeni po natančnih pravilih od njegove velikosti do reaktivnosti, ki prehaja skozi druge lastnosti, kot je število elektronov v zadnji lupini atomska.
Periodična tabela je v bistvu tabela, ki je sestavljena iz vrstic in stolpcev. Vrstice, ki so razporejene v obliki vodoravno, s tako imenovanimi obdobja medtem ko stolpcivertikalno so skupin. Kaj pa določa, da sta dva elementa v isti skupini ali v drugi skupini? V tej lekciji učitelja bomo videli značilnosti skupin periodnega sistema.
Kazalo
- Katere so skupine periodnega sistema? Koliko skupin je v periodnem sistemu?
- Značilnosti skupine 1 (IA)
- Značilnosti skupine 2 (IIA)
- Značilnosti skupin 3 do 12 (B)
- Značilnosti skupine 13 (IIIA)
- Značilnosti skupine 14 (DDV)
- Značilnosti skupine 15 (VA)
- Značilnosti skupine 16 (VIA)
- Značilnosti skupine 17 (VIIA)
- Značilnosti skupine 18 (VIIIA)
Katere so skupine periodnega sistema? Koliko skupin je v periodnem sistemu?
Preden začnemo govoriti o značilnostih skupin v periodnem sistemu, moramo vedeti, iz česa je sestavljen ta sistem. Za preučevanje do zdaj odkritih kemičnih elementov Mendelejev je ta vzorec zasnoval v tabeli: periodni sistem elementov. V periodični tabeli se pojavijo vodoravne vrstice in navpični stolpci. Stolpci periodnega sistema se imenujejo skupine in elementi iste skupine (v isti stolpca) imajo enako valenco in podobne kemijske lastnosti, ki jih bomo videli v nadaljevanju oddelkov.
Trenutno je periodni sistem sestavljen iz 18 skupin. Vsaki od skupin je dodeljena koda in v nekaterih primerih splošno ime.
The 18 skupin periodnega sistema To so:
- Skupina 1, IA ali alkalijske kovine. Sestavljen iz litija (Li), natrija (Na), kalija (K), rubidija (Rb), cezija (Cs) in francija (Fr)
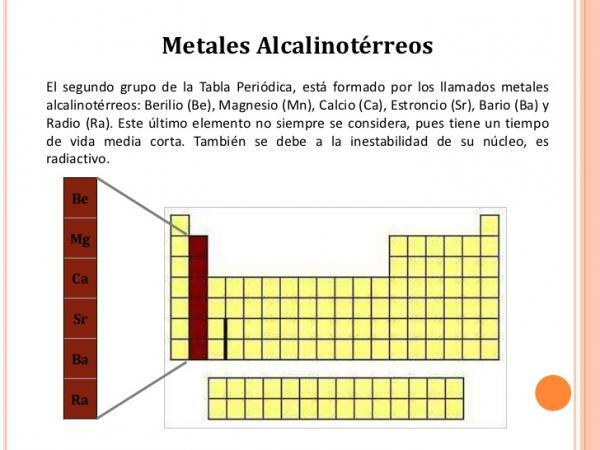
- Skupina 2, II A ali zemeljskoalkalijske kovine. Sestavljen je iz berilija (Be), magnezija (Mg), kalcija (Ca), stroncija (Sr), barija (Ba) in radija (Ra).
- Skupina 3, IIIB ali družina Escandio. Sestavljeno iz: Scandium (Sc), Ytrium (Y), Lutetium (Lu), Lawrencio (Lr), Lanthanum (La), Actinium (Ac).
- Skupina 4, IV B ali družina titana. Sestavljen je iz elementov: titana (Ti), cirkonija (Zr) in hafnija (Hf) in ruterfordija (Rf)
- Skupina 5, družina VB ali vanadij. To skupino sestavljajo elementi: vanadij (V), niobij (Nb), tantal (Ta) in dubnij (Db).
- Skupina 6, družina VIB ali krom. V skupino 6 spadajo: krom (Cr), molibden (mo), volfram ali volfram (W) in morskiborgij (Sg).
- Skupina 7, družina VIIB ali mangan. Skupino 7 sestavljajo: mangan (Mn), tehnecij (Tc), renij (re) in bohrio (Bh).
- Skupina 8, VIIIB ali družina železa. Skupina 8 vključuje: železo (Fe), rutenij (Ru), osmij (Os) in hazij (Hs).
- Skupina 9, IXB ali družina kobalta. Skupino 9 sestavljajo: kobalt (Co), rod (Rh), iridij (Ir) in meitnerij (Mt).
- Skupina 10, družina XB ali nikelj. To skupino sestavljajo: nikelj (Ni), paladij (Pd), platina (Pt) in darmstadij (Ds) (prej Ununnilio (Uun).
- Skupina 11, XIB, družina bakra ali kovanje kovin. V to skupino spadajo: baker (Cu), srebro (Ag), zlato (Au) in roentgenij (Rg).
- Skupina 12, XIIB ali družina cinka. Skupino 12 sestavljajo: cink (Zn), kadmij (Cd), živo srebro (Hg) in Kopernik (Cn).
- Skupina 13, IIIA ali družina Bor. Tvorijo ga bor (B), aluminij (Al), galij (ga), indij (v), talij (Tl) in nihonij (Nh).
- Skupina 14, IVA, družina ogljika ali karbonidov. Skupino 14 sestavljajo elementi: ogljik (C), silicij (Si), germanij (Ge), kositer (Sn), svinec (Pb) in flerovij (Fl).
- Skupina 15, V5, družina pnicógenos ali nitrogenoides. Sestavljajo ga: dušik (N), fosfor (P), arzen (As), antimon (Sb), bizmut (Bi) in muscovio (Mc).
- Skupina 16, VIA, amfogeni, halkogeni ali družina kisika. Sestavljajo ga: kisik (O), žveplo (S), selen (Se), telur (Te), polonij (Po) in Livermorio (Lv).
- Skupina 17, VIIA ali halogeni. To skupino sestavljajo: fluor (F), klor (Cl), brom (Br), jod (I), astat (At) in tenese (Ts).
- Skupina 18, VIIIA ali plemeniti plini. Skupino tvorijo: helij (He), neon (Ne), argon (Ar), kripton (Kr), ksenon (Xe), radon (Rn) in oganesson (Og).
Druga klasifikacija kemijskih elementov
Znotraj kemijskih elementov najdemo drugo klasifikacijo skupin periodnega sistema.
- Skupine 1, 2, 13, 14, 15, 16, 17 in 18 spadajo v skupino A glavnih elementov ali skupin
- Medtem ko skupine 3, 4, 5, 6, 7, 8, 9, 10, 11 in 12 spadajo v skupino B ali prehodne kovine.
Večino teh kemičnih elementov lahko najdemo v naravi, bodisi čisti bodisi v mešanicah z drugimi spojinami ali elementi. Po drugi strani pa so nekateri izmed njih, kot je Muscovy, umetni elementi, ki jih je človek ustvaril v laboratorijih in jih v naravi še ni bilo videti. Tu vas bomo podrobneje odkrili kako je organiziran periodni sistem.
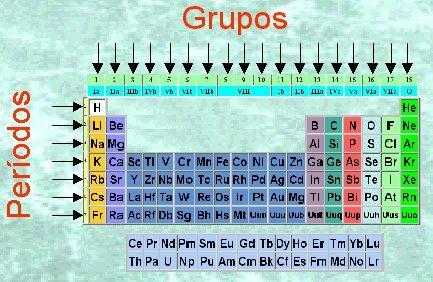
Slika: Periodni sistem
Značilnosti skupine 1 (IA)
Začnemo z analizo značilnosti skupin v periodnem sistemu in govorimo o elementi skupine 1 ki imajo naslednje Lastnosti:
- Število oksidacije +1. Zato so zelo elektropozitivni in imajo nizko ionizacijsko energijo, saj ta elektron zlahka izgubijo.
- Elektronska konfiguracija je ns1
- So kemično najbolj reaktivni kemični elementi, zato v naravi niso izolirani, temveč v obliki soli.
- So mehke kovine z nizko gostoto z nizkim tališčem. Pri njihovem rezanju ali taljenju opazimo njihovo srebrno barvo in kovinski sijaj.
- So voljni, nodularni in dobri vodniki toplote in električne energije.
- Pri reakciji z vodo tvorijo hidrokside

Slika: Diapozitiv
Značilnosti skupine 2 (IIA)
The elementi skupine 2 imajo naslednje značilnosti:
- Oksidacijsko število +2
- Elektronska konfiguracija je ns2
- Nizka ionizacijska energija, ki je s spuščanjem v skupini čedalje manj. Zato, razen berilija, vsi tvorijo jasno ionske spojine.
- Z lahkoto reagirajo s halogeni in tvorijo ionske soli.
- Imajo majhno gostoto in so obarvani in mehki
Slika: Diapozitiv
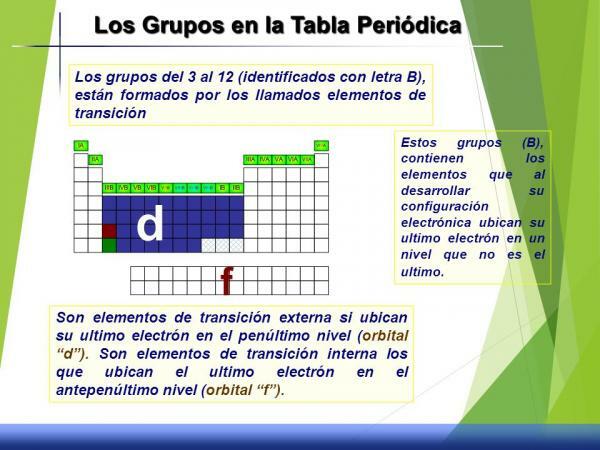
Značilnosti skupin 3 do 12 (B)
Ta niz skupin se imenuje prehodne kovine ali blok d saj je, če pogledamo njeno elektronsko konfiguracijo, d orbita delno napolnjena z elektroni.
Imajo vmesno vedenje, to pomeni, da niso zelo reaktivni, čeprav niso zelo reaktivni (malo reaktanti) nimajo značilnih oksidacijskih stanj ali stanja, gostote ali lastnosti opredeljeno.
Slika: Slideplayer
Značilnosti skupine 13 (IIIA)
Skupina 13Čeprav je po svojih značilnostih tudi precej vmesen, vidimo, da je nekoliko bolj opredeljen kot prejšnji. Elementi skupine 13 imajo:
- Imajo oksidacijsko stanje +3 in v nekaterih elementih tudi +1
- Običajno so metaloidi z zelo visokim tališčem
- Običajno imajo tipične nekovinske lastnosti

Slika: Diapozitiv
Značilnosti skupine 14 (DDV)
The karbonidi Prav tako so precej raznoliki in imajo prav posebno značilnost: ko se spustimo v skupino, imajo elementi bolj kovinske lastnosti; ogljik je nekovina, silicij in germanij sta polmetala, kasneje pa sta kositr in svinec kovine.

Slika: Slideserve
Značilnosti skupine 15 (VA)
V nadaljevanju značilnosti skupin periodnega sistema bomo zdaj govorili o skupina 15 elementov:
- Pri visoki temperaturi so zelo reaktivni. Klasičen primer je reakcija dušika s kisikom in vodikom, ki se pojavi le pri visoki temperaturi ali tlaku.
- Imajo 5 valentnih elektronov.
- Kovalentne vezi se običajno tvorijo med N in P, ionske vezi med Sb in Bi in drugimi elementi.

Slika: Slideplayer
Značilnosti skupine 16 (VIA)
Značilnosti skupina 16 elementov To so:
- Imajo šest valentnih elektronov (zadnja lupina s2str4)
- Njegove lastnosti se spreminjajo od nekovinskih do kovinskih, saj se atomsko število poveča.
- Njegova atomska prostornina, gostota, polmer aniona ter tališča in vrelišča se povečujejo, ko se premikamo po skupini navzdol.
- Njegova specifična toplota in toplota tvorbe hidrida se zmanjšujeta, ko se spuščamo v skupini.

Slika: Slideplayer
Značilnosti skupine 17 (VIIA)
Značilnosti skupina 17 ali halogeni so naslednji:
- So monovalentni elementi, to pomeni, da imajo samo eno valentno število. V halogenih je valenca -1.
- Običajno se kombinirajo s kovinami in tvorijo halogenide, halogenide ali hidracide.
- Imajo malo afinitete za kisik, zato ne tvorijo oksidov, ampak pri zelo visokih temperaturah.

Slika: Slideplayer
Značilnosti skupine 18 (VIIIA)
In to lekcijo o značilnostih skupin periodnega sistema zaključimo s pogovorom o žlahtni plini ali elementi iz skupine 18 ki imajo naslednje značilnosti:
- Predstavljajo stanje plina v naravi.
- Njihov elektronski sloj ali zadnji valentni sloj je popoln, zato niso preveč reaktivni.
- V naravi jih je zelo veliko. Po vodiku je helij najpogostejši element v znanem vesolju.
- Imajo nizka tališča in vrelišča
- Kažejo negativno elektronsko afiniteto
- Nekateri med njimi so radioaktivni, zaradi česar so z gospodarskega vidika zelo pomembni.

Slika: Slideplayer
Če želite prebrati več podobnih člankov Značilnosti skupin periodnega sistema, priporočamo, da vnesete našo kategorijo Atom.
Bibliografija
- Quimicas.net (julij 2015) Skupine kemičnih elementov. Pridobljeno od https://www.quimicas.net/2015/07/grupos-de-elementos-quimicos.html
- Pacheco, A (s.f) Skupine periodnega sistema, njihov opis in značilnosti http://www.universidadcultural.com.mx/online/claroline/work/user_work.php? cmd = exDownload & authId = 7750 & assigId = 3 & workId = 131 & cidReset = true & cidReq = CIIS1_002
- Znanstveno področje (s.f) Skupine periodnega sistema, obnovljene iz https://www.areaciencias.com/quimica/familias-de-la-tabla-periodica.html