Razlika med endotermnimi in eksotermnimi reakcijami
A endotermna reakcija zahteva moč, medtem ko a eksotermna reakcija sprošča energijo. Ta klasifikacija kemičnih reakcij upošteva sodelovanje energije bodisi kot reaktanta bodisi kot produkta.
Energija je sposobnost dela ali proizvodnje toplote. Ne pozabite, da kemične reakcije vključujejo reorganizacijo atomov med snovmi, ki se pretrgajo ali tvorijo kemične vezi. Na splošno to tvorbo ali prekinitev kemičnih vezi spremljajo spremembe v energiji sistema.
| Endotermična reakcija | Eksotermna reakcija | |
|---|---|---|
| Definicija | Kemična reakcija, kjer se absorbira energija. | Kemična reakcija, pri kateri se energija sprošča v obliki toplote. |
| Izvor energije | Od okolja | Sistema |
| Potencialna energija | Nižje v reaktantih kot v izdelkih. | Več v reaktantih kot v izdelkih. |
| Proizvodnja | Ne spontano | Spontano |
| Notranja sprememba energije | ΔE> 0; notranja sprememba energije večja od nič. | ΔE <0; notranja sprememba energije manjša od nič. |
| Temperatura | Zmanjšuje | Poveča |
| Primeri | Reakcije pri fotosintezi in sintezi na splošno. | Pekoča vžigalica, reakcije izgorevanja. |
Kaj je endotermna reakcija?
Kemična reakcija je endotermna, ko absorbira energijo iz okolja. V tem primeru se toplota prenese od zunaj v notranjost sistema. Ko postavimo termometer, medtem ko poteka endotermna reakcija, temperatura pade.
Beseda "endotermna" izhaja iz grščine endon kar pomeni "znotraj" in terme kar pomeni "toplota". Endotermne reakcije ne potekajo spontano.
Od kod energija v endotermnih reakcijah?
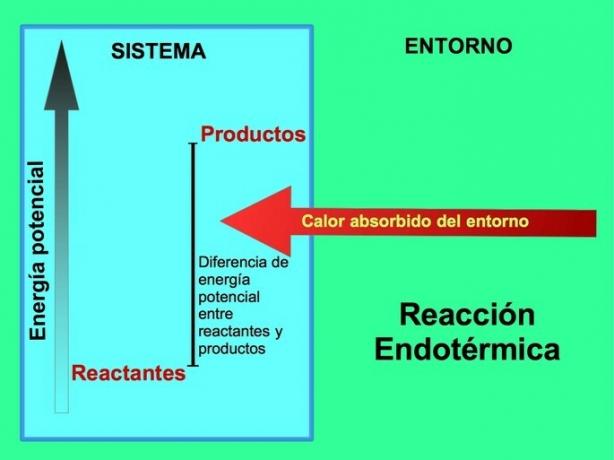
Pri endotermnih reakcijah energija prihaja iz okolja zunaj sistema. Količina potencialne energije produktov je večja od potencialne energije reaktantov. Zato je treba reaktantom dodati energijo za nadaljevanje reakcije. Ta energija prihaja iz okoljske toplote.
Na primer fotosinteza je endotermni proces, kjer rastline zajemajo sončno energijo za proizvodnjo glukoze iz ogljikovega dioksida in kisika:

Produkti reakcije fotosinteze, glukoza in kisik, imajo večjo količino potencialne energije glede na reaktante, ogljikov dioksid in vodo. Drugi primeri endotermnih kemičnih reakcij s porabljeno količino energije:

Primeri endotermne reakcije
Ne pride samo do reakcij v kemijskem laboratoriju. Vsakodnevno najdemo tudi situacije, ko se pojavijo endotermne reakcije.
Kuhanje hrane
Čeprav se morda ne zdi tako, je postopek kuhanja hrane endotermičen. Za uživanje določenih živil moramo zagotoviti toploto.
Takojšnja hladna vrečka
Hladna pakiranja, ki se uporabljajo za zdravljenje izboklin ali zvinov, se napolnijo z vodo, vendar se ob stresanju ali trku kapsula z amonijevim nitratom vdre v notranjost. Mešanje amonijevega nitrata z vodo je endotermna reakcija, zaradi katere se vreča ohladi.
Morda vas zanima ogled Razlika med toploto in temperaturo.
Kaj je eksotermna reakcija?
A eksotermna reakcija je tista, pri kateri energija teče iz sistema. Ta energija se sprosti v obliki toplote, zato postavitev termometra v reakcijski sistem poveča temperaturo.
Beseda "eksotermno" tvori exo kar pomeni "navzven" in terme, kar pomeni "toplota". Eksotermne reakcije se lahko pojavijo spontano in so v nekaterih primerih eksplozivne, na primer kombinacija alkalijskih kovin in vode.
Od kod energija v eksotermnih reakcijah?
V kemijski reakciji so reaktanti spojine, ki se preoblikujejo in tvorijo produkte. Na primer, ko natrij Na reagira s klorom Cl, so to reaktanti in produkt je natrijev klorid NaCl:

Tako reaktanti kot izdelki imajo shranjeno potencialno energijo. Iz lvarčevanje z energijo ta energija se ne izgubi in ne pridobi, zato mora biti energija reaktantov enaka energiji produktov.
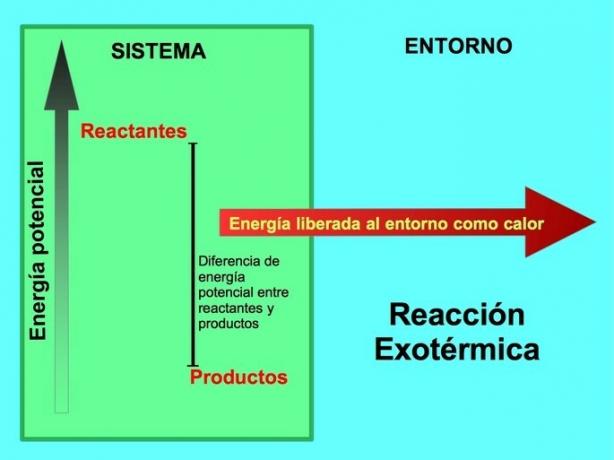
V eksotermni reakciji je lreaktanti imajo več potencialne energije v primerjavi z izdelki, tako da se odvečna energija sprosti kot toplota. V tem primeru se energija šteje tudi kot del izdelkov:

V katerem koli eksotermnem procesu se del potencialne energije, shranjene v kemičnih vezah, s toploto pretvori v toplotno energijo.
Primeri eksotermne reakcije
Detergent za pranje perila
Ko v rokah raztopimo malo pralnega praška z vodo, začutimo rahlo segrevanje.
Domače zgorevanje plina
Izgorevanje plinov za domačo uporabo, kot sta metan ali butan, vključuje kemično reakcijo s kisikom s tvorbo ogljikovega dioksida in vode ter sproščanje energije. To je tipična eksotermna reakcija v vsakdanji uporabi:
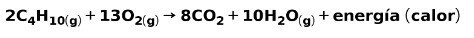
Energija, ki se sprosti v procesu zgorevanja, se porabi za kuhanje hrane.
Morda vas bo zanimalo tudi, kaj so Odprt sistem, zaprt sistem in izoliran sistem.


