Чему служи ПЕРИОДИЧНИ СТОЛ?
Периодни систем је систем класификације атомских елемената који је 1869. године изумео руски хемичар Дмитрија Менделејева, а касније су га реорганизовали и ажурирали други хемичари све док није постигао његов изглед Тренутни. Иако је алат који се током историје показао корисним (зато се и даље користи и ажурира), он је тако заморно учити и разумети, због чега смо сви поставили себи питање „Чему служи табела? периодично? ".
Ако желите да знате чему служи периодни систем и зашто је важно разумети његове особине, наставите да читате ову лекцију од УЧИТЕЉА.
Индекс
- Класификација периодног система
- Проналажење имена или симбола елемента уз периодни систем
- Знати атомску масу елемента
- Знати атомски број елемента
- Предвидите атомски радијус елемента
- Упоредите енергију јонизације два елемента
- Проналажење електронегативности хемијског елемента
- Упоредите афинитет електрона два елемента
Класификација периодног система.
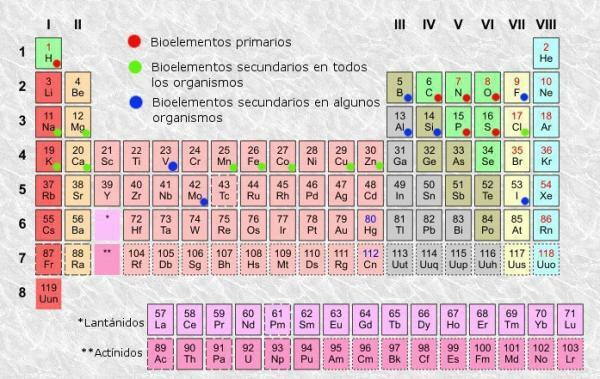
Као у било којој табели, и у периодни систем од елемената можемо разликовати колоне (вертикално) и редове (хоризонтално). У периодном систему постоји 18 колона или група и 7 редова или тачака.
Поред тога, могли сте да проверите да ли се нормално у сваком од поља у табели појављују најмање следеће информације:
- Симбол хемијског елемента: скраћенице или знакови који се користе за идентификацију елемената. Обично се састоје од једног или два слова, од којих је прво увек велико.
- Назив хемијског елемента: назив хемијског елемента који одговара горњој скраћеници. Обично је испод симбола.
- Атомски број: укупан број протона које има сваки атом тог елемента. Обично се појављује у горњем левом углу оквира са ставкама (или у горњем десном углу комплетнијих табела).
- Атомска маса: Маса атома се нормално може сматрати укупном масом протона и неутрона у једном атому. Доступан је испод имена елемента у најједноставнијим табелама, мада се у другима може појавити у горњем десном делу оквира са елементима.
Постоје периодичне табеле које укључују и друге сложеније и конкретније информације као што су оксидациона стања (корисно при формулисању хемијских једињења, на пример), енергија јонизације, електронегативност итд., али основне периодичне таблице обично дају довољно информација и обично су довољне за просечног корисника, који од њих може сазнати информације попут оне коју ћемо вам рећи у наставку.

Пронађите име или симбол елемента уз периодни систем.
Понекад знамо симбол хемијског елемента али му не знамо име. У другим случајевима знамо назив хемијског елемента, али не и његову скраћеницу или симбол. У ствари, врло је лако да вам се ово икада догодило на часу.
У тим случајевима можемо користити периодни систем, без потребе да буде сложен, и брзо и тачно прегледати податке који недостају.
Знати атомску масу елемента.
Понекад знамо хемијски елемент са којим имамо посла, али морамо да га знамо атомска маса, односно колико тежи атом тог елемента.
Ове информације ће бити корисне, на пример, приликом обављања следећих задатака:
- Израчунајте одређену количину супстанце.
- Анализирајте резултате добијене у тестовима или експериментима.
- Израчунати проценат масе.
- Разумети тачне моларне масе сложених молекула.
Знати атомски број елемента.
Атомски број је укупан број протона које има атом елемента. У електрично неутралном атому, осим катиону (позитивно наелектрисан, са једним електроном мањим од нормалног стања) или ањона (негативно наелектрисаног, са још једним електроном више од његовог нормалног стања), број протона је једнак броју електрони.
Број протона је одлучујући фактор када је у питању разликовање једног елемента од другог, јер број електрона или неутрона не мења врсту елемента.

Предвидите атомски радијус елемента.
Атомски радијус је половина удаљености између средишта два атома истог елемента који се једва додирују. У овом случају, знајте положај хемијског елемента на периодном систему Може нам помоћи да откријемо приближни атомски радијус или упоредимо га са другим елементом. За ово морамо то знати атомски радијус:
- Повећава се како се крећемо од врха до дна периодног система.
- Спушта се док се крећемо с лева на десно кроз периодни систем.
На овај начин, калцијум је мањи од рубидијума, али већи од гвожђа.
Сазнајте више о Колики је атомски радијус уз ову другу видео лекцију од НАСТАВНИКА.
Упоредите енергију јонизације два елемента.
Тхе енергија јонизације је енергија потребна за уклањање електрона из атома елемента. У овом случају, ако знамо положај два елемента у периодном систему, можемо знати којем елементу ће бити лакше „уклонити“ електрон. Морамо узети у обзир само следеће:
- Енергија јонизације опада како се креће горе-доле по периодном систему.
- Енергија јонизације се повећава како се крећете са леве на десну страну периодног система.
Између берилијума и кисеоника, кисеоник има више енергије јонизације. Ако упоредимо кисеоник и сумпор, који су у истој групи, али у наредном периоду, кисеоник такође има већу енергију јонизације, јер је већи на периодном систему.
Наћи електронегативност хемијског елемента.
Електронегативност је способност атома да привлачи електроне. У пракси се то преводи у способност стварања хемијске везе. Да бисмо знали да ли ће хемијски елемент имати велики капацитет да формира хемијску везу или не, морамо само узети у обзир образац који следи у периодном систему, то јест:
- Спушта се док се креће горе-доле.
- Повећава се кретањем слева удесно.
Као и у претходном случају, кисеоник је електронегативнији од берилија и сумпора, јер је даље десно од првог и већи од сумпора.

Упоредите афинитет електрона два елемента.
Тхе Електронски афинитет Је ли он промена енергије коју доживљава неутрални атом када привлачи електрон да постане негативни јон. У овом случају, електронски афинитет се не разликује тачно као у претходним случајевима, мада можемо рећи да, генерално, електронски афинитет:
- Подиже се, у истом периоду, слева надесно.
- Попните се, у истој групи, одоздо према горе.
Ако желите да прочитате још чланака сличних Чему служи периодни систем?, препоручујемо вам да уђете у нашу категорију Атом.
Референце
Да ли имате било какав инпут или коментар о употреби периодног система? Слободно то оставите у нашем одељку за коментаре! Да ли вам се свидео овај чланак? Такође можете да оставите оцену испод!