З’ясуйте, де електрони знаходяться в атомі

Електрони - це субатомні частинки, які обертаються навколо атомного ядра в електронній хмарі, яка називається електронна кора. На цьому уроці від ВЧИТЕЛЯ ми побачимо де електрони в атомній структурі, а також поведінка електронів у різних станах атомів (ґрунтовий та збудливий стан), коли утворюються атоми одноатомні іони і коли електрони не зв’язані з яким-небудь конкретним атомом.
Індекс
- Що таке електрони і де вони знайдені?
- Як дізнатися, що таке валентні електрони?
- Електрони атома: основний стан та стан збудження
- Приріст або втрата електрона: одноатомне утворення іонів
- Електрони в русі: електричний струм
Що таке електрони і де вони знайдені?
електрони я знаю вони знаходять всередині з атомиякі є найменшими одиницями, з яких складається речовина. Атоми неподільні, а їх будова та склад визначають характеристики матеріалів.
Атоми складаються з трьох типів субатомні частинки:
- Протони: це частинки з масою і позитивним зарядом
- Нейтрони: це частинки з масою і без електричного заряду
- Електрони: Це безмасові та негативно заряджені частинки.
Протони та нейтрони є частиною ядра атома, так що атомне ядро він концентрує всю масу і позитивний заряд атома.
З іншого боку, електрони обертаються навколо ядра на певних орбітах, утворюючи електронну хмару, яку називають електронна кора. Електронна оболонка атома концентрує весь негативний заряд і не має маси.
Орбіти електронів
Орбіти, які описують електрони навколо атомного ядра, є певними заздалегідь визначеними орбітами. Тобто шляхи руху електронів навколо атомного ядра не є випадковими. Усередині електронної оболонки існує лише кілька можливих орбіт для електронів; тоді як інші орбіти заборонені. визначається як атомна орбіталь ту область навколо ядра, в якій ймовірність знаходження електрона перевищує 90%.
На кожній з цих можливих орбіталей електрон, який циркулює через нього, набуває певної енергії, яка збільшується в міру віддалення орбіталей від ядра. Орбіталі згруповані в різні енергетичні рівні (n) або шарів, загалом існує 7 енергетичних рівнів, причому n = 1 є найнижчим енергетичним рівнем і найближчим до ядра атома. На кожному з енергетичних рівнів або шару є різні типи орбіталей (s, p, d та f орбіталей)
Схема розподілу електронів на різних енергетичних рівнях та орбіталях в атомі відома як електронна конфігурація.
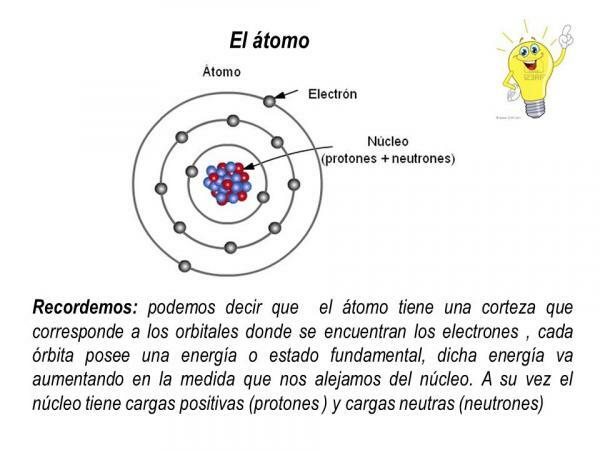
Зображення: Slideplayer
Як дізнатися, що таке валентні електрони?
Фізичні та хімічні характеристики атомів визначаються їх складом і, особливо, електронною конфігурацією крайній шар (валентний шар).
Хімічні елементи - це різні типи атомів, які існують і визначаються їх атомним номером (Z) та масовим числом (A).
- Атомне число (Z): число протонів атомного елемента, яке дорівнює кількості електронів, якщо атом нейтральний.
- Масове число (A): кількість частинок з масою атомного елемента, тобто сума частинок атомного ядра (протони плюс нейтрони).
Кожному елементу присвоєно a хімічний символ що представляє його, і сукупність усіх з них записана в науковому документі, який порядки за їх атомним номером та групує їх за їхніми характеристиками у сімейства та групи афін: Періодична таблиця.
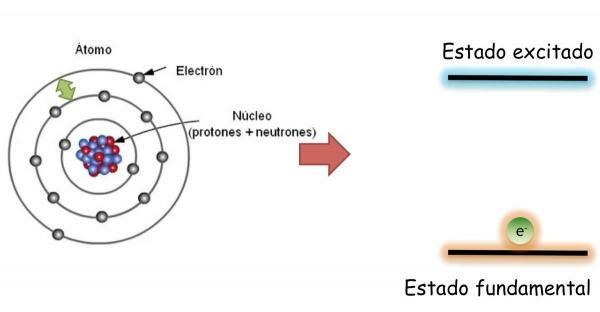
Електрони атома: основний стан та стан збудження.
В фундаментальна держава, який визначається як стан мінімальної енергії та максимальної стійкості атома; електрони не розподіляються хаотично на різних атомних орбіталях, а займають різні орбіталі впорядковано, завжди заповнюючи, по-перше, нижчі орбіталі без енергії.
У цьому стані атом має таку ж кількість електронів, як і протони, а позитивні та негативні заряди компенсують один одного, тому атом в цілому нейтральний (він не має чистого заряду).
Однак електрони може перестрибувати з однієї орбіти на іншу віддаючи або поглинаючи енергію. Коли електрони атома не заповнюють орбіталі впорядковано, кажуть, що атом знаходиться збуджений стан. У стані збудження один або кілька електронів займають орбітали вищої енергії, залишаючи порожні інші меншої енергії. У збудженому стані атоми вкрай нестійкі і мають тенденцію до швидкого повернення в основний стан.
При зміні орбіти електрон випромінює або поглинає енергію. Якщо електрон стрибне з меншої енергетичної орбіти на більш енергетичну, атом поглине енергію; тоді як якщо стрибок здійснений у зворотному напрямку (з орбіталі з вищою енергією на одну з нижчої енергії), атом випустить енергію.
Втрата або приріст електронів: утворення одноатомних іонів.
Електрони в зовнішній оболонці електронної кори (так званої валентної оболонки) є електронами, які вони можуть залишити атом або їх можна включити для цього. Таким чином атом може отримувати або втрачати електрони.
В нейтральний атом кількість протонів, присутніх в ядрі, дорівнює кількості електронів, що складають його електронну оболонку. Тобто кількість позитивних зарядів дорівнює кількості негативних зарядів. Коли відбувається приріст або втрата електронів, атоми утворюються одноатомні іони.
Типи одноатомних іонів
За зарядом іона розрізняють два типи:
- Одноатомні катіони: атоми, які втратили один або кілька електронів, так що частина позитивного заряду ядра не компенсується. Тому атом набуває чистого позитивного заряду.
- Одноатомні аніони: атоми, які набрали один або кілька електронів, так що число електронів більше, ніж число протонів в ядрі, так що атом набуває чистого негативного заряду.

Електрони в русі: електричний струм.
Коли електрони вони не пов'язані ні з одним атомом зокрема вони рухаються через вільний простір між атомами. Цей незалежний рух електронів утворює потік електричного заряду, який може рухатися через певні матеріали (провідні та напівпровідникові матеріали).
Так, наприклад, трапляється у випадку з електричний струм що забезпечує живлення будинків, транспортних засобів тощо.
Якщо ви хочете прочитати більше статей, подібних до Де знайдені електрони?, ми рекомендуємо вам ввести нашу категорію Атом.
Бібліографія
Alejandrina Gallego Picó, Rosa Mª Garcinuño Martínez, Mª José Morcillo Ortega, Miguel Ángel Vázquez Segura. (2018) Базова хімія. Мадрид: Без розсилки