أجزاء من الذرة وخصائصها
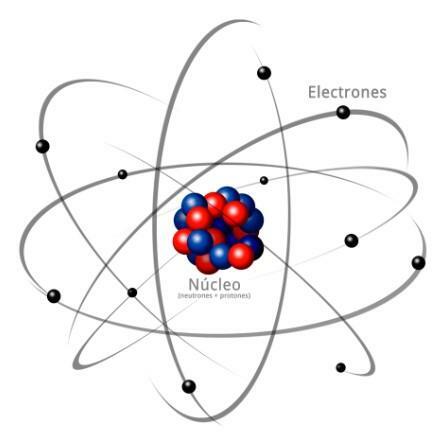
الصورة: Answers.tips
الذرات هي العناصر الأساسية التي شكل المسألة، التواجد في جميع حالات المادة. إنها عناصر صغيرة جدًا ، من المستحيل رؤيتها بالعين البشرية ولكنها مهمة حقًا لكوننا. لفهم كيفية عمل الذرات بشكل أفضل ، سنتحدث في هذا الدرس من المعلم أجزاء من الذرة وخصائصها.
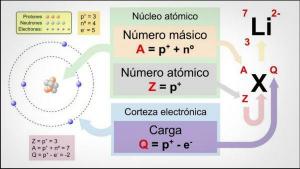
تتكون جميع الذرات من لب وقشرة. النواة ، كما يشير اسمها ، هي الجزء المركزي من الذرة ، حيث الجسيمات التي تكون شحنتها موجبة والتي تسمى البروتونات، والجسيمات التي تكون شحنتها متعادلة ، أي ليس لها شحنة كهربائية ، وتحمل اسم النيوترونات. كتلة كلا الجسيمين ، البروتونات والنيوترونات ، متشابهة. جميع ذرات نفس العنصر الكيميائي لها عدد متساوٍ من البروتونات ، وتحصل على هذا الرقم اسم العدد الذري وتستخدم الحرف Z لتمثيله.
من ناحية أخرى هناك اللحاء ما هو ال الجزء الخارجي من الذرة. في اللحاء نجد الإلكترونات، وهي جسيمات سالبة الشحنة. تدور الإلكترونات بسرعة كبيرة حول النواة على مستويات مختلفة ، فهي جسيمات أصغر بكثير من تلك الموجودة في النواة.
كونها نيوترونات محايدة وبروتونات موجبة وإلكترونات سالبة ، تحتوي الذرة على شحنة كهربائية محايدة ، لأن لديهم نفس عدد البروتونات مثل الإلكترونات. على الرغم من وجود حالات يكون فيها عدد الإلكترونات أقل أو أكبر من البروتونات ، مما يسبب الشحن الذرة سالبة أو موجبة ، في هذه الحالة تستقبل اسم أيون ، أنيون إذا كان سالبًا أو كاتيون إذا كان موجبًا.
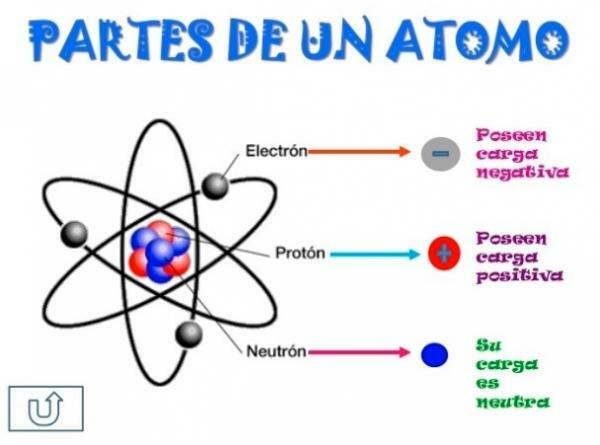
الصورة: برينلي
للاستمرار في هذا الدرس حول أجزاء الذرة وخصائصها ، يجب أن نتحدث عن التطور الذي حدث لأجزاء الذرة ، منذ ذلك الحين لقد تغير النموذج الذري بمرور الوقت بفضل دراسات العلماء. يجب أن يؤخذ في الاعتبار أن العديد من النماذج التي سنشرحها قديمة ولا يتم استخدامها في الوقت الحاضر ، لكنها ضرورية لفهم تطور المجتمع العلمي حول هذا الموضوع.
يتميز التطور التاريخي للنموذج الذري بـ اتباع العلماء:
- نموذج دالتون: كان أول نموذج ذري هو عمل جون دالتون في عام 1803. إنه نموذج بدائي للغاية يفتقد إلى العديد من العناصر مثل وجود الإلكترونات والبروتونات.
- نموذج طومسون: نجح جون طومسون في صنع نموذج ذري أكثر اكتمالًا من نموذج دالتون ، مضيفًا عدة عناصر أساسية. اكتشف طومسون وجود الإلكترونات والشحنات الموجبة والسالبة.
- نموذج ناجاوكا: لم يتفق الفيزيائي الياباني ناجاوكا مع نموذج طومسون ، فقد اعتقد أن الذرة يجب أن تحتوي على نواة كبيرة موجبة الشحنة تدور عليها الإلكترونات سالبة الشحنة. تسمى نظريته زحل ، حيث قارن الإلكترونات بحلقات زحل. في كثير من الأحيان لم يتم تسمية هذا النموذج ، ولكن من الضروري فهم الخطوة العظيمة التي يتم اتخاذها في هذا الوقت.
- نموذج رذرفورد: اعتمد نموذج رذرفورد على وجود نواة موجبة الشحنة تدور عليها الإلكترونات سالبة الشحنة. هذا النموذج مشابه جدًا لنموذج ناجاوكا، كونها من السنوات القريبة جدًا ، على الرغم من أن النموذج الياباني أقدم.
- نموذج بوهر: اعتقد بوهر أنه يجب فصل الإلكترونات على مسافة كبيرة من النواة ذات الطبقات وأن عدد هذه الجسيمات المدارية يجب أن يكون مساويًا للعدد الذري. يدرك نموذجه أيضًا أن عدد الإلكترونات يختلف في كل غلاف ، مع عدد أقل من الإلكترونات في الغلاف الأول مقارنة بالقشرة الأخيرة.
- نموذج شرودنجر: كسر شرودنجر الاعتقاد بأن الإلكترونات هي جزيئات صغيرة تدور حول النواة. جادل العالم النمساوي بأن الإلكترونات تتحرك عن طريق دالة موجية ، أي بواسطة الشكل المداري.
- نموذج ديراك: قام ديراك بتعديل أفكار شرودنجر لنموذجه ، باستخدام "معادلة ديراك" لإعطاء رؤية أكثر دقة للشكل المداري للإلكترونات.