Charakteristika skupin PERIODICKÉ TABULKY
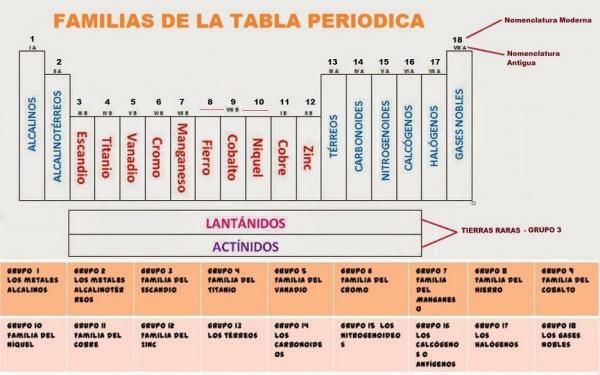
Obrázek: Přírodní vědy
The periodická tabulka prvků objednat vše chemické prvky dosud známé. I když se to může zdát jinak, tyto prvky jsou uspořádány podle pečlivých pravidel, která platí od jeho velikosti k jeho reaktivitě, procházející dalšími vlastnostmi, jako je počet elektronů v poslední skořápce atomový.
Periodická tabulka je v podstatě tabulka složená z řádků a sloupců. Řádky, které jsou uspořádány do formuláře horizontální, s tzv období zatímco sloupce, svisle, jsou skupiny. Co však určuje, že dva prvky jsou ve stejné skupině nebo v jiné skupině? V této lekci od UČITELE uvidíme charakteristika skupin periodické tabulky.
Index
- Jaké jsou skupiny periodické tabulky? Kolik skupin je v periodické tabulce?
- Vlastnosti skupiny 1 (IA)
- Vlastnosti skupiny 2 (IIA)
- Charakteristika skupin 3 až 12 (B)
- Vlastnosti skupiny 13 (IIIA)
- Charakteristika skupiny 14 (DPH)
- Vlastnosti skupiny 15 (VA)
- Vlastnosti skupiny 16 (VIA)
- Vlastnosti skupiny 17 (VIIA)
- Vlastnosti skupiny 18 (VIIIA)
Jaké jsou skupiny periodické tabulky? Kolik skupin je v periodické tabulce?
Než začneme mluvit o vlastnostech skupin v periodické tabulce, musíme vědět, z čeho se tento systém skládá. Chcete-li studovat dosud objevené chemické prvky, Mendělejev vymyslel tento vzor v tabulce: periodická tabulka prvků. V periodické tabulce se objevují vodorovné řádky a svislé sloupce. Sloupce periodické tabulky se nazývají skupiny a prvky stejné skupiny (ve stejné sloupec) mají stejnou valenci a podobné chemické vlastnosti, které uvidíme dále sekce.
V současné době je periodická tabulka složená z 18 skupin. Každá ze skupin má přidělen kód a v některých případech i běžný název.
The 18 skupin periodické tabulky Oni jsou:
- Skupina 1, IA nebo alkalické kovy. Skládá se z lithia (Li), sodíku (Na), draslíku (K), rubidia (Rb), cesia (Cs) a francium (Fr)
- Skupina 2, II A nebo kovy alkalických zemin. Skládá se z berylia (Be), hořčíku (Mg), vápníku (Ca), stroncia (Sr), barya (Ba) a radia (Ra).
- Skupina 3, IIIB nebo Escandio. Složení: Scandium (Sc), Yttrium (Y), Lutetium (Lu), Lawrencio (Lr), Lanthanum (La), Actinium (Ac).
- Skupina 4, IV B nebo titanová rodina. Skládá se z prvků: titan (Ti), zirkonium (Zr) a hafnium (Hf) a rutherfordium (Rf)
- Skupina 5, VB nebo Vanadium Family. Tuto skupinu tvoří prvky: vanad (V), niob (Nb), tantal (Ta) a dubnium (Db).
- Skupina 6, skupina VIB nebo chrom. Ve skupině 6 jsou zahrnuty: Chrom (Cr), Molybden (Mo), Wolfram nebo Tungsten (W) a Seaborgium (Sg).
- Skupina 7, VIIB nebo manganová rodina. Skupina 7 se skládá z: manganu (Mn), technecia (Tc), rhenia (Re) a Bohrio (Bh).
- Skupina 8, VIIIB nebo rodina železa. Skupina 8 zahrnuje: Železo (Fe), Ruthenium (Ru), Osmium (Os) a Draslík (Hs).
- Skupina 9, IXB nebo kobaltová rodina. Skupina 9 se skládá z: kobaltu (Co), rhodia (Rh), iridia (Ir) a meitneria (Mt).
- Skupina 10, XB nebo nikl. Tuto skupinu tvoří: nikl (Ni), palladium (Pd), platina (Pt) a darmstad (Ds) (dříve Ununnilio (Uun)).
- Skupina 11, XIB, skupina mědi nebo ražby kovů. Tato skupina zahrnuje: měď (Cu), stříbro (Ag), zlato (Au) a Roentgenium (Rg).
- Skupina 12, XIIB nebo rodina zinku. Skupina 12 se skládá z: Zinek (Zn), Kadmium (Cd), Rtuť (Hg) a Koperník (Cn).
- Skupina 13, IIIA nebo rodina Boronů. Tvoří je bor (B), hliník (Al), galium (Ga), indium (in), thallium (Tl) a nihonium (NH).
- Skupina 14, IVA, uhlík nebo skupina karbonidů. Skupina 14 se skládá z prvků: uhlík (C), křemík (Si), germanium (Ge), cín (Sn), olovo (Pb) a phlerovium (Fl).
- Skupina 15, V5, rodina pnicógenos nebo nitrogenoidů. Skládá se z: dusíku (N), fosforu (P), arsenu (As), antimonu (Sb), bismutu (Bi) a muscovio (Mc).
- Skupina 16, VIA, amfogeny, chalkogeny nebo skupina kyslíku. Skládá se z: Kyslík (O), Síra (S), Selen (Se), Tellurium (Te), Polonium (Po) a Livermorio (Lv).
- Skupina 17, VIIA nebo halogeny. Tato skupina se skládá z: fluoru (F), chloru (Cl), bromu (Br), jodu (I), astátu (At) a tenese (Ts).
- Skupina 18, VIIIA nebo vzácné plyny. Skupinu tvoří: hélium (He), neon (Ne), argon (Ar), krypton (Kr), xenon (Xe), radon (Rn) a oganesson (Og).
Druhá klasifikace chemických prvků
V rámci chemických prvků můžeme najít druhou klasifikaci skupin periodické tabulky.
- Skupiny 1, 2, 13, 14, 15, 16, 17 a 18 patří do skupiny A hlavních prvků nebo skupin
- Zatímco skupiny 3, 4, 5, 6, 7, 8, 9, 10, 11 a 12 patří do skupiny B nebo přechodných kovů.
Většina z těchto chemických prvků se nachází v přírodě, a to buď čistá, nebo ve směsích s jinými sloučeninami nebo prvky. Na druhou stranu, některé z nich, stejně jako pižmoň, jsou umělé prvky, které vytvořil člověk v laboratořích a které v přírodě nikdy nebyly vidět. Zde vás objevíme podrobněji jak je periodická tabulka organizována.
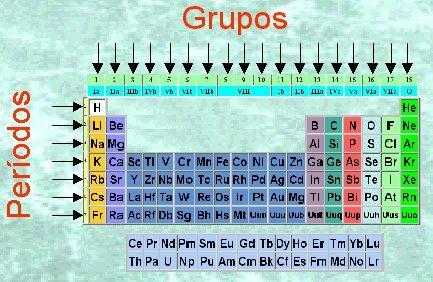
Obrázek: Periodická tabulka
Vlastnosti skupiny 1 (IA)
Začneme analýzou charakteristik skupin v periodické tabulce a mluvíme o prvky skupiny 1 které mají následující funkce:
- Oxidační číslo +1. Jsou proto velmi elektropozitivní a mají nízkou ionizační energii, protože tento elektron snadno ztratí.
- Elektronická konfigurace je ns1
- Jedná se o chemicky nejvíce reaktivní chemické prvky, a proto v přírodě nejsou izolovány, ale ve formě solí.
- Jsou to měkké kovy s nízkou hustotou s nízkými teplotami tání. Při řezání nebo tavení je pozorována jejich stříbrná barva a kovový lesk.
- Jsou tvárné, tvárné a dobré vodiče tepla a elektřiny.
- Při reakci s vodou tvoří hydroxidy

Obrázek: Prezentace
Vlastnosti skupiny 2 (IIA)
The skupina 2 prvky mají následující vlastnosti:
- Oxidační číslo +2
- Elektronická konfigurace je ns2
- Nízká ionizační energie, která se s klesáním ve skupině zmenšuje. Proto, kromě berylia, všechny tvoří jasně iontové sloučeniny.
- Snadno reagují s halogeny za vzniku iontových solí.
- Mají nízkou hustotu a jsou barevné a měkké
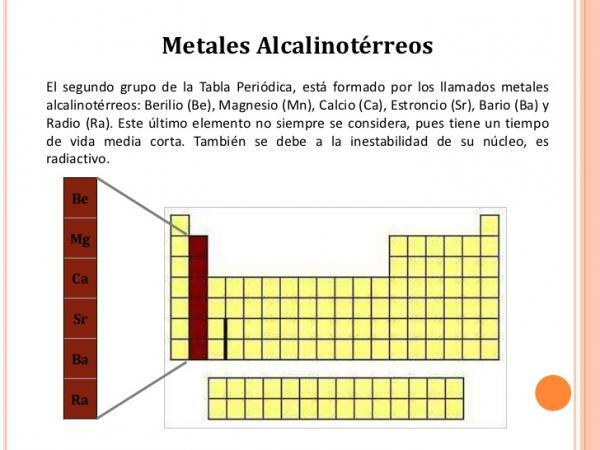
Obrázek: Prezentace
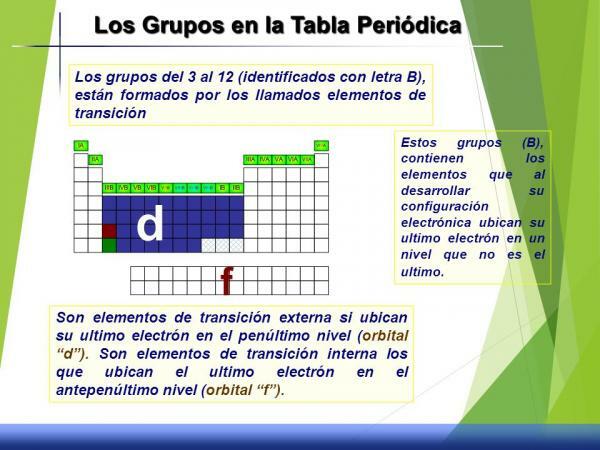
Charakteristika skupin 3 až 12 (B)
Tato skupina skupin se nazývá přechodné kovy nebo blok d protože když se podíváme na jeho elektronickou konfiguraci, d orbitál je částečně naplněn elektrony.
Mají střední chování, to znamená, že aniž by byli velmi reaktivní, nejsou příliš inertní (málo reaktanty), nemají jasně charakteristické oxidační stavy nebo stav, hustotu nebo vlastnosti definované.
Obrázek: Slideplayer
Vlastnosti skupiny 13 (IIIA)
Skupina 13Přestože je z hlediska svých charakteristik také docela středně pokročilý, vidíme, že je poněkud definovanější než ty předchozí. Prvky skupiny 13 mají:
- Mají oxidační stav +3 a v některých prvcích také +1
- Obvykle se jedná o metaloidy s velmi vysokou teplotou tání
- Mívají typické nekovové vlastnosti

Obrázek: Prezentace
Charakteristika skupiny 14 (DPH)
The karbonidové prvky Jsou také velmi rozmanité a mají velmi zvláštní charakteristiku: Jak sestupujeme do skupiny, prvky mají více kovových charakteristik; uhlík je nekov, křemík a germanium jsou polokovy a dále ve skupině jsou cín a olovo kovy.

Obrázek: Slideserve
Vlastnosti skupiny 15 (VA)
Pokračováním charakteristik skupin periodické tabulky si nyní povíme o skupina 15 prvků:
- Jsou velmi reaktivní při vysoké teplotě. Klasickým příkladem je reakce dusíku s kyslíkem a vodíkem, ke které dochází pouze při vysoké teplotě nebo tlaku.
- Mají 5 valenčních elektronů.
- Kovalentní vazby se obvykle tvoří mezi N a P, iontové vazby mezi Sb a Bi a dalšími prvky.

Obrázek: Slideplayer
Vlastnosti skupiny 16 (VIA)
Vlastnosti skupina 16 prvků Oni jsou:
- Mají šest valenčních elektronů (poslední skořápky s2str4)
- Jeho vlastnosti se liší od nekovových ke kovovým, protože se zvyšuje jeho atomové číslo.
- Jeho atomový objem, hustota, poloměr anionu a body tání a bodu varu se zvyšují, jak se pohybujeme dolů ve skupině.
- Jeho specifické teplo a teplo tvorby hydridu se snižují, jak sestupujeme ve skupině.

Obrázek: Slideplayer
Vlastnosti skupiny 17 (VIIA)
Vlastnosti skupina 17 nebo halogeny jsou následující:
- Jsou to jednomocné prvky, to znamená, že mají pouze jedno valenční číslo. U halogenů je valence -1.
- Obvykle se kombinují s kovy a vytvářejí halogenidy, halogenidy nebo hydrokovidy.
- Mají malou afinitu ke kyslíku, takže netvoří oxidy, ale při velmi vysokých teplotách.

Obrázek: Slideplayer
Vlastnosti skupiny 18 (VIIIA)
A tuto lekci o vlastnostech skupin periodické tabulky zakončíme rozhovorem o vzácné plyny nebo prvky skupiny 18 které mají následující vlastnosti:
- Představují stav plynu v přírodě.
- Jejich elektronická vrstva nebo vrstva poslední valence je úplná, takže nejsou příliš reaktivní.
- Mají velmi bohatou povahu. Po vodíku je hélium nejhojnějším prvkem ve známém vesmíru.
- Mají nízkou teplotu tání a teplotu varu
- Vykazují negativní elektronickou afinitu
- Některé z nich jsou radioaktivní, což je činí z ekonomického hlediska velmi důležitými.

Obrázek: Slideplayer
Pokud si chcete přečíst více podobných článků Charakteristika skupin periodické tabulky, doporučujeme vám zadat naši kategorii Atom.
Bibliografie
- Quimicas.net (červenec 2015) Skupiny chemických prvků. Obnoveno z https://www.quimicas.net/2015/07/grupos-de-elementos-quimicos.html
- Pacheco, A (s.f) Skupiny periodické tabulky, jejich popis a vlastnosti http://www.universidadcultural.com.mx/online/claroline/work/user_work.php? cmd = exDownload & authId = 7750 & assigId = 3 & workId = 131 & cidReset = true & cidReq = CIIS1_002
- Vědecké oblasti (s.f) Skupiny periodických tabulek získané z https://www.areaciencias.com/quimica/familias-de-la-tabla-periodica.html