DEFINITION von positiven oder negativen IONen

Wie wir bereits wissen, Atome sie werden gebildet von subatomare Partikel. Von den drei Arten subatomarer Teilchen haben nur Neutronen keine elektrische Ladung. Stattdessen haben Protonen eine positive elektrische Ladung, während Elektronen eine negative Ladung haben. Nur die Elektronen, die die Peripherie des Atoms besetzen, können von einem Atom zum anderen übertragen werden, während die Protonen im Kern ihre Zahl stabil halten. In dieser Lektion von einem LEHRER werden wir sehen, was passiert, wenn Atome oder Moleküle Elektronen aufnehmen oder verlieren. Das heißt, wir werden sehen die Definition und Beispiele für positive oder negative Ionen.
Index
- Was sind Ionen? Einfache Definition
- Ionenbildung: Elektroaffinität und Elektronegativität
- Was sind negative Ionen? Mit Beispielen
- Was sind positive Ionen? Mit Beispielen
Was sind Ionen? Einfache Definition.
EIN Ion ist irgendwas Atom oder Molekül mit elektrischer Nettoladung. Das heißt, es ist ein Atom oder eine Gruppe von Atomen, die miteinander verbunden sind und deren elektrische Ladungen
werden nicht entschädigt. Diese Ladungsdekompensation tritt auf, wenn ein oder mehrere Elektronen ein Atom oder eine Gruppe von Atomen verbinden oder verlassen.Die Ionen sind also geladene Atome oder Moleküle, aufgrund des Gewinns oder Verlusts von Elektronen (subatomare Teilchen mit negativer Ladung und vernachlässigbarer Masse).
Ionentypen: einatomig und mehratomig
Wenn wir die Zusammensetzung von Ionen berücksichtigen, werden zwei Arten unterschieden: einatomige Ionen und mehratomige Ionen.
- Wie der Name schon sagt, einatomige Ionen diejenigen, die von a gebildet werden einzelnes Atom.
- Ionische Verbindungen aus Polyatomionen sind solche, in denen die Atome kovalent gebunden sind (ein oder mehrere Elektronenpaare in der Bindung teilen) und eine Anzahl von Neutronen im Molekül anders als die Gesamtzahl der Elektronen.
- Das Polyatomionen sie enthalten normalerweise Sauerstoff und sie haben normalerweise eine Struktur mit einem Zentralatom, um das die restlichen Elemente, aus denen das Molekül besteht, angeordnet sind.
- Das Ladung einatomiger Ionen der repräsentativen Elemente (Familien 1 und 2 des Periodensystems und Familien 13 bis 17 des Periodensystems) können leicht abgeleitet werden, wenn ihre Lage im Periodensystem bekannt ist. In diesen Fällen gewinnen oder verlieren die Atome Elektronen, um in ihrer Valenzschale die Konfiguration des Edelgases seiner Periode zu erreichen (so2p6), oder was gleich ist, erfülle die Oktettregel.
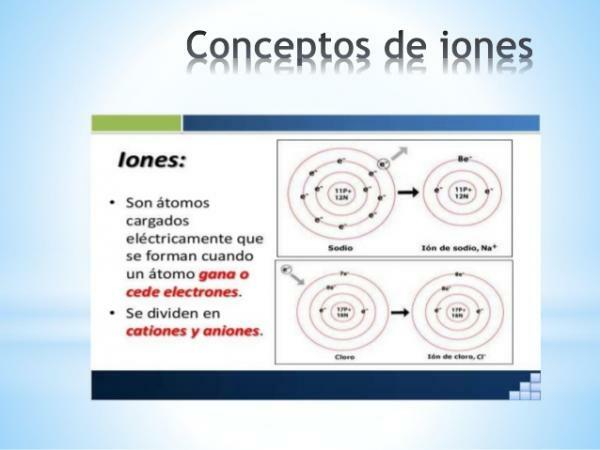
Bild: Slideshare
Ionenbildung: Elektroaffinität und Elektronegativität.
Die Fähigkeit von Atomen oder Molekülen, Ionen bilden wird durch zwei periodische Eigenschaften bestimmt: Elektroaffinität und Elektronegativität. Beide Eigenschaften steigen im Laufe einer Periode an Wert und nehmen ab, wenn wir durch eine Gruppe oder Familie des Periodensystems absteigen.
Das Elektroaffinität, auch Elektronenaffinität genannt, ist eine atomare Eigenschaft, die als die Fähigkeit eines Atoms definiert ist, Elektronen anzuziehen. Bei Verbindungen wird eine ähnliche Eigenschaft namens property Elektronegativität Dies ist definiert als die Fähigkeit eines Atoms, Elektronen anzuziehen, wenn es eine Bindung mit einem anderen Atom eingeht. Beide Eigenschaften definieren somit die Tendenz eines Elements, Elektronen einzufangen oder zu verlieren.
Ionische Bindungen
Ionen bilden in fester Form Verbindungen oder Ionenkristalle (Salze), gebildet durch die Kombination von Ionen unterschiedlichen Vorzeichens, die miteinander verbunden sind durch ionische Bindungen. Das bekannteste Beispiel für diese Art von Verbindung ist Kochsalz (Natriumchlorid: NaCl).
Die Ionenbindung besteht aus Vereinigungen von Ionen unterschiedlichen Vorzeichens durch elektrostatische Anziehungskräfte (Anziehung zwischen Ladungen mit entgegengesetztem Vorzeichen). In diese Art von Verbindungen greifen Elemente ein, deren Elektronegativität oder Elektroaffinität sehr unterschiedlich ist (metallische und nichtmetallische Elemente). In den meisten Fällen sind diese ionischen Verbindungen in Wasser löslich und andere polare Lösungsmittel.
In wässrigen Lösungen dissoziieren ionische Verbindungen in freie Ionen, die als Elektrolyte, da sich das Wasser durch seine Anwesenheit in der Lösung wie ein elektrischer Leiter verhält.
Was sind negative Ionen? Mit Beispielen.
Das negative Ionen Sie heißen Anionen. In allen Fällen handelt es sich um Atome nichtmetallischer Elemente oder um Moleküle, die nichtmetallische Elemente enthalten. Diese Elemente zeichnen sich durch eine sehr hohe Elektroaffinität und Elektronegativität aus. Mit anderen Worten, es sind Ionen, die von Elementen mit. gebildet werden eine hohe Tendenz, Elektronen einzufangen.
Einatomige Anionen: Definition und Beispiele
Sie sind die Anionen, die von Atomen nichtmetallischer Elemente (Gruppen 13 bis 17 des Periodensystems) gebildet werden, die ein oder mehrere Elektronen gewonnen haben. Diesen Anionen ist die elektronische Edelgasstruktur (s2p6) in seiner äußersten Elektronenschale (Valenzschale).
Beispiele:
- Chloridion: Cl-
- Fluoridion: F-
- Ionenjodid: I-
- Sulfidion: S-2
- Nitrid-Ion: N-3
Mehratomige Anionen: Definition und Beispiele
Sie sind negativ geladene Ionen, die von zwei oder mehr Atomen nichtmetallischer Elemente gebildet werden, die durch kovalente Bindungen verbunden sind. Sie sind die häufigsten mehratomigen Ionen. Die häufigsten mehratomigen Anionen sind Oxoanionen, die aus einem zentralen Nichtmetallatom bestehen und Sauerstoff enthalten.
Im Allgemeinen gelten sie als chemische Verbindungen, die erhalten werden, wenn eine saure Verbindung ein oder mehrere Protonen (H+). Diese mehratomigen Anionen können etwas Wasserstoff in ihrer Struktur behalten, was ihnen einen gewissen Säurecharakter verleiht (Fähigkeit, Protonen abzugeben).
Beispiele:
- Nitration: NO3-
- Permanganat-Ion: MnO4-
- Phosphat-Ion: PO4-3
- Hydrogencarbonat oder Bicarbonat-Ion: HCO3-
- Sulfit-Ion: SO3-2
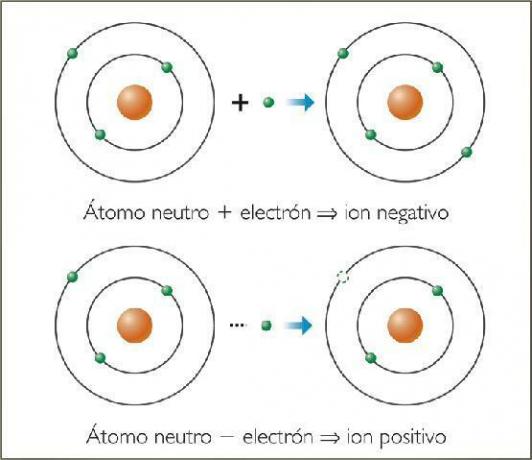
Bild: Naturheilkunde
Was sind positive Ionen? Mit Beispielen.
Positive Ionen heißen cationen. In fast allen Fällen handelt es sich um Atome metallischer Elemente oder um Moleküle, die metallische Elemente enthalten. Diese Elemente zeichnen sich durch eine sehr geringe Elektroaffinität und Elektronegativität aus, weshalb sie eine deutliche Tendenz zum Elektronenverlust zeigen.
Einatomische Kationen: Definition und Beispiele
Sie sind Ionen mit einer positiven Ladung (aufgrund des Elektronenverlustes), die von einem einzelnen Atom eines metallischen Elements gebildet werden. In diesem Fall wird das Kation durch den Verlust von Elektronen gebildet, die es dem Element ermöglichen, seine äußerste elektronische Schicht zu leeren und eine Edelgaskonfiguration anzunehmen (s2p6) von der unteren Ebene. Sie sind die häufigste Art von Kationen.
Beispiele:
- Wasserstoff oder Hydron-Kation (auch Proton genannt): H+
- Natriumkation: Na+
- Eisen(III)-Kation oder Eisen(III)-Kation: Fe+3
- Calciumkation: Ca+2
- Kupfer (II) oder Kupfer(II)-Kation: Cu+2
Mehratomige Kationen: Definition und Beispiele
Mehratomige Kationen sind solche, die von zwei oder mehr Atomen gebildet werden. Sie sind selten, am häufigsten sind die sogenannten homopolyatomaren Kationen, die mehr als eins enthalten Atom des gleichen Elements ist es im Fall des Triwasserstoff-Ions eines der am häufigsten vorkommenden Moleküle im Universum. Mehratomige Kationen, die von Atomen verschiedener Elemente gebildet werden, sind nicht üblich, aber gekennzeichnet durch die Anwesenheit von Wasserstoff und wird als entstanden angesehen, wenn eine basische Verbindung ein Proton einfängt (H+).
Beispiele:
- Ammoniumkation: NH4+
- Oxonium-Kation: HO3+
- Phosphoniumkation: PH3+
- Trihydrogenkation oder protonierter molekularer Wasserstoff: H3+
- Diquecksilberkation: Hg2+2
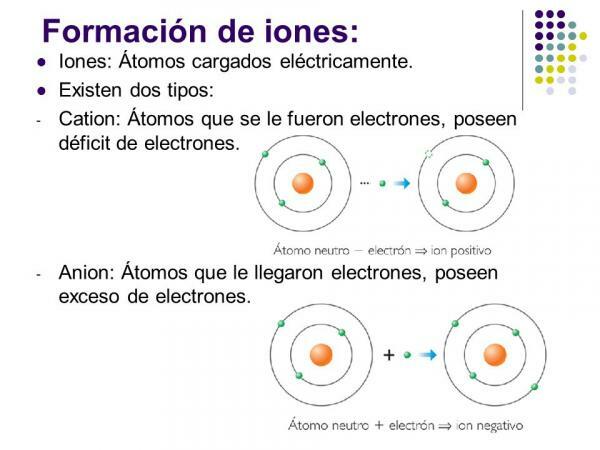
Bild: Planeten
Wenn Sie mehr ähnliche Artikel lesen möchten Negative und positive Ionen: Definition und Beispiele, wir empfehlen Ihnen, unsere Kategorie von Das Atom.
Literaturverzeichnis
Alejandrina Gallego Picó, Rosa Mª Garcinuño Martínez, Mª José Morcillo Ortega, Miguel Ángel Vázquez Segura. (2018) Grundlegende Chemie. Madrid: Uned