Finden Sie heraus, wo sich die Elektronen in einem ATOM befinden

Elektronen sind subatomare Teilchen, die sich in einer Elektronenwolke namens. um den Atomkern drehen elektronischer Kortex. In dieser Lektion von einem LEHRER werden wir sehen wo sind die elektronen innerhalb der Atomstruktur, sowie das Verhalten von Elektronen in den verschiedenen Zuständen der Atome (Grund- und Erregungszustand), wenn sich Atome bilden einatomige Ionen und wenn die Elektronen nicht an ein bestimmtes Atom gebunden sind.
Index
- Was sind Elektronen und wo kommen sie vor?
- Woher weißt du, was die Valenzelektronen sind?
- Elektronen eines Atoms: Grundzustand und im Anregungszustand
- Elektronengewinn oder -verlust: einatomare Ionenbildung
- Elektronen in Bewegung: elektrischer Strom
Was sind Elektronen und wo kommen sie vor?
Das Elektronen ich weiß drinnen finden des Atomedas sind die kleinsten Einheiten, aus denen die Materie besteht. Atome sind unteilbar und ihre Struktur und Zusammensetzung bestimmen die Eigenschaften von Materialien.
Atome bestehen aus drei Arten von subatomare Partikel:
- Protonen: sind Teilchen mit Masse und positiver Ladung
- Neutronen: sind Teilchen mit Masse und ohne elektrische Ladung
- Elektronen: Sie sind masselose und negativ geladene Teilchen.
Protonen und Neutronen sind Teil des Atomkerns, so dass die Atomkern es konzentriert die gesamte Masse und die positive Ladung des Atoms.
Die Elektronen hingegen rotieren auf definierten Bahnen um den Kern und bilden eine Elektronenwolke, die als bezeichnet wird elektronischer Kortex. Die elektronische Hülle des Atoms konzentriert die gesamte negative Ladung und hat keine Masse.
Elektronenbahnen
Die Bahnen, die die Elektronen um den Atomkern beschreiben, sind bestimmte vordefinierte Bahnen. Das heißt, die Bahnen der Elektronen um den Atomkern sind nicht zufällig. Innerhalb der Elektronenhülle gibt es nur wenige mögliche Bahnen für Elektronen; während andere Umlaufbahnen verboten sind. ist definiert als Atomorbital der Bereich um den Kern, in dem die Wahrscheinlichkeit, ein Elektron zu finden, größer als 90% ist.
In jedem dieser möglichen Orbitale erhält das darin zirkulierende Elektron eine bestimmte Energie, die zunimmt, je weiter die Orbitale vom Kern entfernt sind. Die Orbitale sind in verschiedene gruppiert Energieniveaus (n) oder Schichten gibt es insgesamt 7 Energieniveaus, wobei n = 1 das niedrigste Energieniveau ist und dem Atomkern am nächsten ist. In jedem der Energieniveaus oder Schichten gibt es verschiedene Arten von Orbitalen (s-, p-, d- und f-Orbitale)
Die Anordnung, in der Elektronen auf die verschiedenen Energieniveaus und Orbitale in einem Atom verteilt sind, nennt man elektronische Konfiguration.
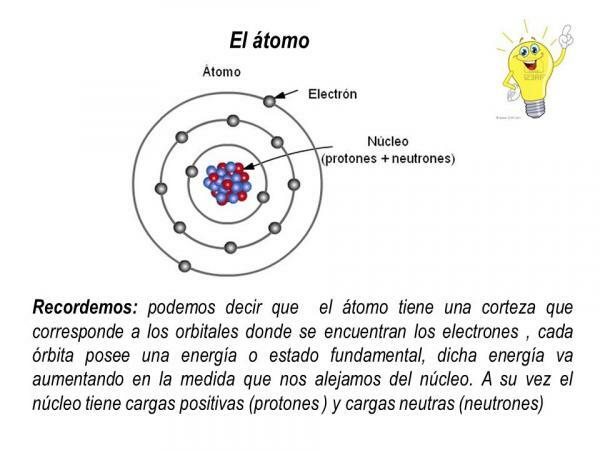
Bild: Slideplayer
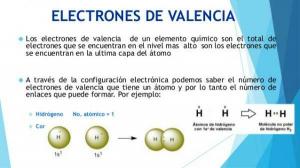
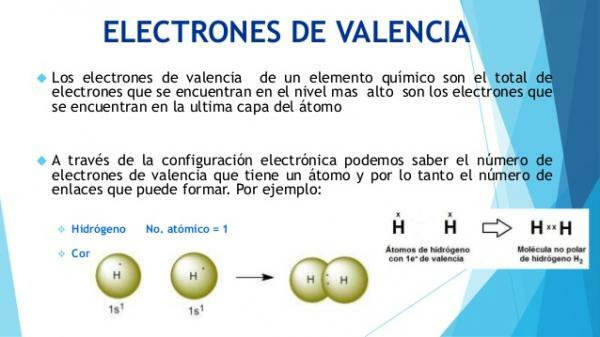
Woher weißt du, was die Valenzelektronen sind?
Die physikalischen und chemischen Eigenschaften von Atomen werden durch ihre Zusammensetzung und insbesondere durch die elektronische Konfiguration ihrer äußerste Schicht (Valenzschicht).
Chemische Elemente sind die verschiedenen Arten von Atomen, die existieren und durch ihre Ordnungszahl (Z) und ihre Massenzahl (A) definiert werden.
- Ordnungszahl (Z): Anzahl der Protonen eines atomaren Elements, die der Anzahl der Elektronen entspricht, wenn das Atom neutral ist.
- Massenzahl (A): Anzahl der Teilchen mit Masse eines atomaren Elements, also die Summe der Teilchen des Atomkerns (Protonen plus Neutronen).
Jedes Element wird a. zugewiesen chemisches Symbol das sie repräsentiert, und die Gesamtheit von ihnen ist in dem wissenschaftlichen Dokument überliefert, dass ordnet sie nach ihrer Ordnungszahl und gruppiert sie nach ihren Eigenschaften in Familien und Gruppen von affinen: Periodensystem.
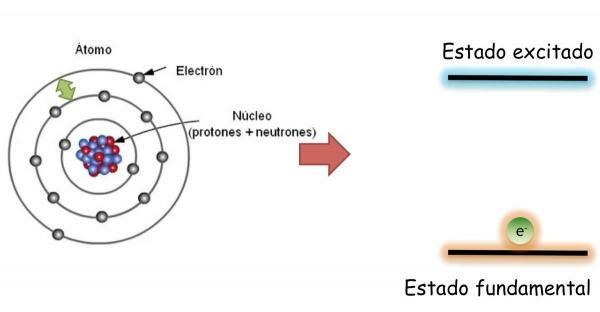
Elektronen eines Atoms: Grundzustand und im Anregungszustand.
In dem Grundzustand, die definiert ist als der Zustand minimaler Energie und maximaler Stabilität eines Atoms; die Elektronen sind nicht zufällig in den verschiedenen Atomorbitalen verteilt, sondern besetzen die verschiedenen Orbitale geordnet, immer zuerst füllend, die niedrigsten energiefreien Orbitale.
In diesem Zustand hat das Atom die gleiche Anzahl von Elektronen wie Protonen und die positiven und negativen Ladungen kompensieren sich, daher ist das Atom als Ganzes neutral (es hat keine Nettoladung).
Allerdings sind die Elektronen kann von einem Orbital zum anderen springen Energie abgeben oder aufnehmen. Wenn die Elektronen eines Atoms die Orbitale nicht geordnet füllen, spricht man von einem Atom in aufgeregter Zustand. Im Anregungszustand besetzen ein oder mehrere Elektronen Orbitale höherer Energie und lassen andere mit niedrigerer Energie leer. Im angeregten Zustand sind die Atome sehr instabil und neigen dazu, schnell in den Grundzustand zurückzukehren.
Beim Orbitalwechsel das Elektron emittiert oder absorbiert Energie. Wenn das Elektron von einer niedrigeren Energiebahn auf eine höhere Energie springt, wird das Atom Energie absorbieren; Wenn der Sprung in die entgegengesetzte Richtung erfolgt (von einem Orbital mit höherer Energie zu einem Orbital mit niedrigerer Energie), wird das Atom Energie freisetzen.
Verlust oder Gewinn von Elektronen: Bildung von einatomigen Ionen.
Die Elektronen in der äußersten Schale des elektronischen Kortex (der sogenannten Valenzschale) sind Elektronen, die sie können das Atom verlassen oder eingebaut werden für dieses. Auf diese Weise kann ein Atom Elektronen aufnehmen oder abgeben.
In einem neutrales Atom Die Anzahl der im Kern vorhandenen Protonen entspricht der der Elektronen, aus denen seine elektronische Hülle besteht. Das heißt, die Anzahl der positiven Ladungen ist gleich der Anzahl der negativen Ladungen. Bei Elektronenaufnahme oder -verlust bilden sich die Atome einatomige Ionen.
Arten von einatomigen Ionen
Je nach Ladung des Ions werden zwei Typen unterschieden:
- Einatomische Kationen: Atome, die ein oder mehrere Elektronen verloren haben, sodass ein Teil der positiven Ladung des Kerns nicht kompensiert wird. Daher erhält das Atom eine positive Nettoladung.
- Einatomische Anionen: Atome, die ein oder mehrere Elektronen aufgenommen haben, sodass die Anzahl der Elektronen größer ist als die Anzahl der Protonen im Kern, sodass das Atom eine negative Nettoladung erhält.

Elektronen in Bewegung: elektrischer Strom.
Wenn Elektronen sie sind an kein Atom gebunden insbesondere bewegen sie sich durch den freien Raum zwischen den Atomen. Diese unabhängige Bewegung von Elektronen bildet einen elektrischen Ladungsfluss, der durch bestimmte Materialien (leitende Materialien und Halbleitermaterialien) wandern kann.
Dies ist zum Beispiel der Fall bei elektrischer Strom die Energie für Gebäude, Fahrzeuge usw.
Wenn Sie mehr ähnliche Artikel lesen möchten Wo sind die Elektronen zu finden?, wir empfehlen Ihnen, unsere Kategorie von Das Atom.
Literaturverzeichnis
Alejandrina Gallego Picó, Rosa Mª Garcinuño Martínez, Mª José Morcillo Ortega, Miguel Ángel Vázquez Segura. (2018) Grundlegende Chemie. Madrid: Uned