Τι είναι τα CATIONS και σε τι χρησιμεύουν;
ο κατιόντα Είναι χημικά είδη που διαδραματίζουν θεμελιώδη ρόλο σε πολλές ζωτικές διαδικασίες και έχουν πολλαπλές εφαρμογές στη βιομηχανία και την ιατρική. Αν θέλετε να μάθετε λεπτομερώς τι είναι τα κατιόντα και τι είναι, διαβάστε αυτό το μάθημα από έναν εκπαιδευτή όπου σας το εξηγούμε
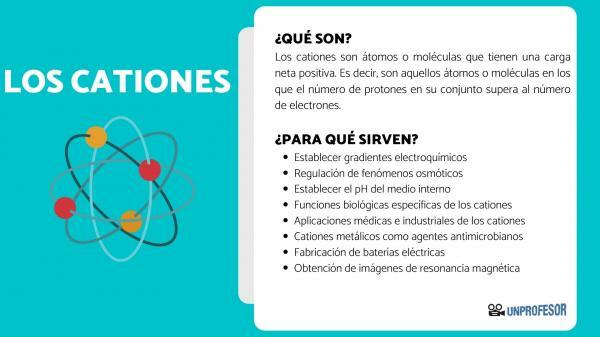
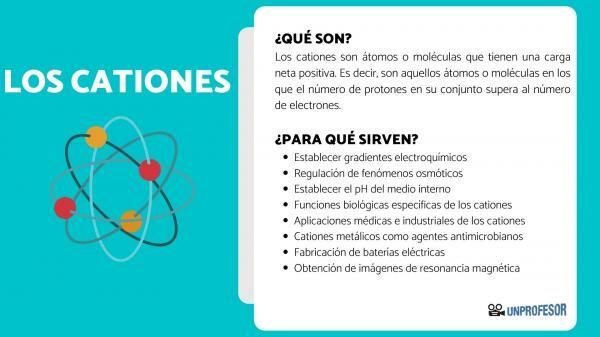
ο κατιόντα Αυτοί είναι άτομα ή μόρια που έχουν καθαρή θετική χρέωση. Δηλαδή, είναι εκείνα τα άτομα ή μόρια στα οποία ο αριθμός των πρωτονίων στο σύνολό του υπερβαίνει τον αριθμό των ηλεκτρονίων.
Αυτό το χημικό είδος παράγεται πάντα από την απώλεια ηλεκτρονίων, αφού αυτά είναι τα μόνα φορτισμένα σωματίδια που μπορούν να φύγουν ή να ενώσουν άτομα ή μόρια. Αυτό ισχύει, από τότε ηλεκτρόνια περιστρέφονται γύρω από το πυρήνας ατόμων σε ένα σύνολο τροχιών (τα οποία ονομάζονται τροχιακά) και τα οποία, στο σύνολό τους, σχηματίζουν τον ηλεκτρονικό φλοιό, το οποίο είναι το εξόχως μέρος του ατόμου.
Τα κατιόντα εμφανίζονται μόνο σε ελεύθερη μορφή σε διάλυμα σε πολικούς διαλύτες όπως νερό. Σε στερεή μορφή τα βρίσκουμε που αποτελούν μέρος των ιοντικών ενώσεων
, σε συνδυασμό με ανιόντα? σχηματισμός βγες έξω. Βρίσκονται επίσης αποτελούν μέρος μεταλλικών ουσιών, στο οποίο τα κατιόντα σχηματίζουν ένα δίκτυο μεταξύ του οποίου τα ηλεκτρόνια κινούνται σε ελεύθερη μορφή.
Τώρα που ξέρετε τι είναι τα κατιόντα, ας ανακαλύψουμε τους διαφορετικούς τύπους που υπάρχουν. Υπάρχουν δύο:
- Μονοτομικά κατιόντα: Τα μονοτομικά κατιόντα είναι εκείνα που σχηματίζονται από ένα μόνο άτομο. Αυτά είναι ιόντα μεταλλικών στοιχείων, τα οποία έχουν πολύ χαμηλή ενέργεια ιονισμού. Αυτό σημαίνει ότι είναι άτομα που αποκολλούνται πολύ εύκολα από τα ηλεκτρόνια του εξώτατου κελύφους τους (κέλυφος σθένους), για να φθάσουν στη δομή ευγενών αερίων της προηγούμενης περιόδου. Αυτή η ηλεκτρονική διαμόρφωση συνεπάγεται υψηλή σταθερότητα και τα μεταλλικά στοιχεία αποκτούν κατιονικές φόρμες πολύ εύκολα.
- Πολυτομικά κατιόντα: Σε αυτήν την περίπτωση, είναι χημικές ενώσεις που αποτελούνται από άτομα διαφορετικών στοιχείων και έχουν καθαρό θετικό φορτίο. Δεν είναι πολύ άφθονα, μερικά παραδείγματα είναι: το ιόν αμμωνίου (NH4+), υδρονίου (H3O+) ή νιτρόνιο (NO2+).
Στα πολυατομικά κατιόντα πρέπει επίσης να λάβουμε υπόψη τα οργανικά κατιόντα, είναι οργανικές ενώσεις (που σχηματίζονται από τον Carbon ως το κύριο στοιχείο) με θετικό φορτίο. Αυτός ο τύπος κατιόντων είναι συνήθως αρωματικός στη φύση, δηλαδή αποτελείται από δακτυλίους βενζολίου.

Εικόνα: Χημεία II
Τα κατιόντα είναι χημικά είδη, η ύπαρξή του δεν συνεπάγεται εγγενή «χρησιμότητα». Ωστόσο, είναι δυνατόν να μιλήσουμε για «χρησιμότητα» σε σχέση τόσο με τη φυσική-χημική όσο και τη βιολογική σημασία των κατιόντων σε μια πληθώρα διαδικασιών ή φαινομένων. φυσική που μπορεί να είναι απαραίτητη για την ορθή λειτουργία του σώματος ή των ιατρικών εφαρμογών του ή των βιομηχανικών διεργασιών που ενδιαφέρουν οικονομικός. Αν θέλετε να μάθετε για ποια είναι τα κατιόντα, σας αφήνουμε μια κριτική για τις πιο συχνές χρήσεις του, λάβετε υπόψη!
Ορίστε ηλεκτροχημικές βαθμίδες
Τα κατιόντα γενικά βρίσκονται σε διαφορετικές συγκεντρώσεις στο εσωτερικό και το εξωτερικό περιβάλλον. Αυτό καθιστά δυνατή τη δημιουργία ηλεκτροχημικών βαθμίδων σε μέσα που διαχωρίζονται από μια ημιδιαπερατή μεμβράνη όπως η κυτταρική μεμβράνη. ο κατιόντα νατρίου και καλίου Είναι ζωτικής σημασίας για τη διατήρηση της ηλεκτροχημικής κλίσης στο εσωτερικό περιβάλλον των ζωντανών οργανισμών. Ενώ το κατιόν Κ+ Είναι το πιο άφθονο στο εσωτερικό περιβάλλον των κυττάρων, το νάτριο είναι το πιο άφθονο κατιόν στο περιβάλλον (βιότοπος). Και τα δύο κατιόντα εμπλέκονται σε πολύπλοκους μηχανισμούς μεταφοράς.
Ρύθμιση των οσμωτικών φαινομένων
Η όσμωση συνίσταται στην παθητική διάχυση (συμβαίνει αυθόρμητα και δεν απαιτεί εισροή ενέργειας) νερού, μέσω μιας μεμβράνης ημιπερατό, από ένα μέσο με υψηλές συγκεντρώσεις μιας ένωσης σε διάλυμα, έως ένα μέσο στο οποίο η συγκέντρωση της εν λόγω ένωσης είναι πιο χαμηλή. Επομένως, η διέλευση νερού μέσω της μεμβράνης καθορίζεται από τις διαφορές συγκέντρωσης μεταξύ του εσωτερικού και του εξωτερικού περιβάλλοντος του κυττάρου.
Καθορίστε το pH του εσωτερικού μέσου
Το ρΗ ενός διαλύματος είναι το επίπεδο συγκέντρωσης ιόντων υδρογόνου (Η +) σε ένα διάλυμα. Αυτή η παράμετρος είναι ζωτικής σημασίας για την επιβίωση των οργανισμών και πρέπει να διατηρείται σε στενά όρια. να διασφαλίσει την ορθή λειτουργία των ενζύμων που ρυθμίζουν τις μεταβολικές αντιδράσεις και άλλες ζωτικές λειτουργίες.
Ειδικές βιολογικές λειτουργίες κατιόντων
Εκτός από τη συμμετοχή στη συντήρηση της ομοιόστασης, το pH του μέσου ή των ηλεκτροχημικών βαθμίδων. Μερικά κατιόντα εκτελούν συγκεκριμένες λειτουργίες μέσα στο σώμα. Για παράδειγμα, αυτός κατιόν ασβεστίου (Ca2+) είναι απαραίτητο στη συστολή των μυών Γ τα κατιόντα νατρίου (Na +) και καλίου (K +) είναι θεμελιώδεις στο μετάδοση ηλεκτρικής ώθησης κατά μήκος του άξονα των νευρώνων.
Βρίσκουμε επίσης κατιόντα που σχετίζονται με οργανικές ουσίες, όπως πρωτεΐνες ή άλλα βιομόρια. Είναι η περίπτωση σιδηρούχο κατιόν (Fe2+) που αποτελεί μέρος του ενεργού κέντρου του αιμοσφαιρίνη και είναι απαραίτητο για τη μεταφορά οξυγόνου στο αίμα. Ένα άλλο παράδειγμα είναι το κατιόν μαγγάνιο (Mg2 +) που είναι μέρος του ενεργού κέντρου της χλωροφύλλης, το φωτοσυνθετική χρωστική των φυτών.
Ως μέρος των αλάτων βρίσκουμε το Ασβέστιο σε στερεή μορφή αποτελούν μέρος δομών στήριξης ή προστασίας όπως κοχύλια, κοχύλια και από σκελετός.
Ιατρικές και βιομηχανικές εφαρμογές κατιόντων
Τα κατιόντα έχουν πολλαπλές εφαρμογές στη βιομηχανία και την ιατρική τόσο στην ελεύθερη μορφή τους (σε διάλυμα) όσο και ως μέρος των αλάτων. Παρακάτω θα δούμε μερικά παραδείγματα χρήσης κατιόντων ή αλάτων τόσο βιομηχανικά όσο και στην ιατρική.
Μεταλλικά κατιόντα ως αντιμικροβιακοί παράγοντες
ο ασημένιο κατιόν (Ag +) Έχει βακτηριοκτόνα αποτελέσματα σε χαμηλές συγκεντρώσεις. Στην ιατρική, χρησιμοποιείται κυρίως για τη θεραπεία εγκαυμάτων.
Σε βιομηχανικό επίπεδο, μεταλλικά κατιόντα, όπως χαλκός, ψευδάργυρος ή τιτάνιο, που περιλαμβάνονται στα νανοσωματίδια, χρησιμοποιούνται επίσης ως αντιμικροβιακοί παράγοντες. Σε τομείς εφαρμογής τόσο διαφορετικοί όσο η κλωστοϋφαντουργία, η ζωοτροφή και η φαρμακευτική και βιομηχανία καλλυντικών.
Κατασκευή ηλεκτρικών μπαταριών
Στην κατασκευή ηλεκτρικών μπαταριών επαναφορτιζόμενηΙόν λιθίου (Li+). Πρόκειται για εξαιρετικά αποδοτικές μπαταρίες γρήγορης φόρτισης με ωφέλιμη ζωή που μπορεί να φτάσει τα 10 χρόνια. Ένα άλλο πλεονέκτημα που έχουν είναι ότι είναι σχετικά φθηνά στην παραγωγή. Αυτές οι μπαταρίες έχουν πολλές εφαρμογές αφού χρησιμοποιούνται σε κινητά τηλέφωνα, φορητούς υπολογιστές και ηλεκτρικά αυτοκίνητα. Οι εφευρέτες αυτών των μπαταριών, οι Goodenough, Whittingham και Yoshino, έλαβαν το βραβείο Νόμπελ Χημείας το 2019.
Απεικόνιση μαγνητικής τομογραφίας
Τα κατιόντα είναι παραμαγνητικά, δηλαδή έχουν την τάση να ευθυγραμμίζονται παράλληλα με ένα μαγνητικό πεδίο. Αυτή η ιδιότητα χρησιμοποιείται στην ιατρική για τη λήψη εικόνων για τη διάγνωση ασθένειας ή τραυματισμού. Συγκεκριμένα, η τεχνική της μαγνητικής τομογραφίας με αντίθεση. Το Contrast είναι μια «βαφή» απεικόνισης που χορηγείται προ του ενδοφλεβίως στον ασθενή. Οι λύσεις του Κατιόν γαδολινίου (Gd3+) που συνδέεται με οργανικές ενώσεις επιτρέποντας το σχηματισμό εικόνων.