Πρωτόνια, νετρόνια και ηλεκτρόνια
Τα πρωτόνια, τα νετρόνια και τα ηλεκτρόνια είναι τα σωματίδια που αποτελούν το άτομο, το οποίο είναι το μικρότερο μέρος του στοιχείου. Αυτά τα σωματίδια καθορίζουν τα χαρακτηριστικά και τις ιδιότητες των χημικών στοιχείων.
Τα πρωτόνια και τα νετρόνια συγκεντρώνονται στον ατομικό πυρήνα, ενώ τα ηλεκτρόνια κατανέμονται στην κρούστα ή στην περιφέρεια του ατόμου. Ένα άτομο έχει τον ίδιο αριθμό ηλεκτρονίων και πρωτονίων, ενώ ο αριθμός των νετρονίων είναι μεταβλητός.
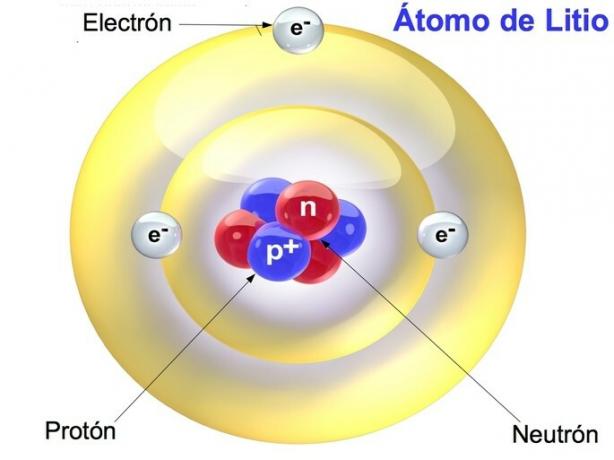
Στη συνέχεια, παρουσιάζουμε έναν συγκριτικό πίνακα μεταξύ πρωτονίων, νετρονίων και ηλεκτρονίων.
| Πρωτόνιο | Νετρόνιο | Ηλεκτρόνιο | |
|---|---|---|---|
| Ορισμός | Υποατομικό σωματίδιο θετικού φορτίου | Υποσωμικό σωματίδιο ουδέτερης φόρτισης | Αρνητικά φορτισμένο υποατομικό σωματίδιο |
| Φορτώνω | Θετικός +1 |
Ουδέτερος 0 |
Αρνητικός -1 |
| Σύμβολο | Π+ | ν0 | και- |
| Θέση στο άτομο | Πυρήνας | Πυρήνας | Περιφερικά τροχιακά |
| Μάζα (kg) | 1.673 x 10--27κιλό | 1.675 x 10--27κιλό | 9.109 x 10--31κιλό |
| Μάζα σε σύγκριση με το πρωτόνιο (amu) | 1 | 1 | 0,0005 |
| Στοιχειακό σωματίδιο | 3 κουάρκ: 2 u και 1 d | 3 κουάρκ: 2 d και 1 u | 1 λεπτό |
| Discoverer (έτος) | ΚΑΙ. Ράδερφορντ (1911) | Ι. Τσάντγουικ (1931) | Τζ. Τόμσον (1897) |
Τι είναι το πρωτόνιο;
Τα πρωτόνια είναι τα θετικά φορτισμένα σωματίδια που βρίσκονται στον πυρήνα ενός ατόμου. Κάθε άτομο ενός στοιχείου έχει έναν σταθερό αριθμό πρωτονίων, το οποίο καθορίζει τον ατομικό του αριθμό, ή Ζ. Έτσι, το υδρογόνο έχει ένα πρωτόνιο και το Ζ ισούται με 1.
Η μάζα του πρωτονίου είναι 1,673 x 10-27 kg, που αντιπροσωπεύει 1 μονάδα ατομικής μάζας ή amu (για το ακρωνύμιο της στα αγγλικά μονάδα ατομικής μάζας).
Το 1911, ο Έρνεστ Ράδερφορντ ανακάλυψε ότι ο πυρήνας ενός ατόμου ήταν μικροσκοπικός και θετικά φορτισμένος, εξ ου και η έννοια του πρωτονίου.
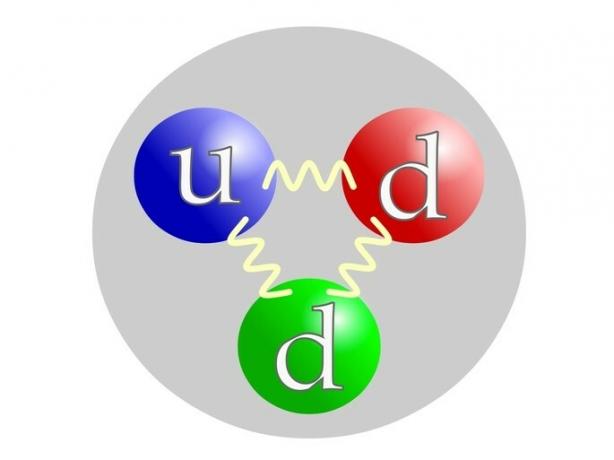
Το πρωτόνιο αποτελείται από στοιχειώδη σωματίδια που ονομάζονται κουάρκ ή κουάρκ: 2 κουάρκ u (ανά πάνω= κορυφή) και 1 quartk d (από κάτω= κάτω).

Πώς να υπολογίσετε τα πρωτόνια ενός ατόμου;
Ο αριθμός των πρωτονίων σε ένα άτομο μπορεί να προσδιοριστεί από τον ατομικό του αριθμό, ο οποίος είναι ο αριθμός θέσης στον περιοδικό πίνακα.
Για παράδειγμα, ο χρυσός Au έχει ατομικό αριθμό = 79, που σημαίνει ότι ο χρυσός έχει 79 πρωτόνια στον πυρήνα του.
Τι είναι ένα νετρόνιο;
Τα νετρόνια είναι τα σωματίδια που βρίσκονται στον πυρήνα ενός ατόμου μαζί με τα πρωτόνια. Συμβολίζονται με το γράμμα ν και χρεώνονται ουδέτερα. Το μόνο στοιχείο που δεν έχει νετρόνια είναι το υδρογόνο.
Η μάζα των νετρονίων είναι πολύ παρόμοια με αυτήν των πρωτονίων, έτσι το άθροισμα των μαζών των πρωτονίων και των νετρονίων καθορίζει την ατομική μάζα ενός στοιχείου.
Άτομα που έχουν τον ίδιο ατομικό αριθμό, αλλά διαφορετικοί αριθμοί νετρονίων ονομάζονται ισότοπα. Για παράδειγμα, το δευτέριο είναι ένα ισότοπο υδρογόνου, το οποίο έχει ένα νετρόνιο και ένα πρωτόνιο στον πυρήνα.
Ο Άγγλος φυσικός Τζέιμς Τσάντγουικ ανακάλυψε το 1931 αυτό το υποατομικό σωματίδιο, με μάζα κοντά στο πρωτόνιο, αλλά με ουδέτερο ηλεκτρικό φορτίο, γι 'αυτό ονομάστηκε νετρόνιο.
Το νετρόνιο συντίθεται όπως το πρωτόνιο από κουάρκ: 1 κουάρκ u (από πάνω= κορυφή) και 2 quartk d (από κάτω= κάτω).
Πώς να υπολογίσετε τα νετρόνια ενός ατόμου;
Μπορούμε να υπολογίσουμε τον αριθμό των νετρονίων σε ένα άτομο αν γνωρίζουμε την ατομική του μάζα και τον ατομικό του αριθμό Ζ. Γνωρίζουμε ήδη ότι ο ατομικός αριθμός Ζ είναι ο αριθμός των πρωτονίων και η ατομική μάζα είναι το άθροισμα των πρωτονίων και των νετρονίων που έχει ένα άτομο.
Για παράδειγμα, το οξυγόνο έχει ατομική μάζα 16 και το Ζ είναι 8. Ο αριθμός των πρωτονίων στο οξυγόνο ισούται με ατομική μάζα μείον Z:
16 - 8 = 8 νετρόνια
Τι είναι ένα ηλεκτρόνιο;
Τα ηλεκτρόνια είναι τα σωματίδια του ατόμου που βρίσκονται στο νέφος που περιβάλλει τον πυρήνα. Ενώ τα πρωτόνια και τα νετρόνια συγκεντρώνονται στον πυρήνα, τα ηλεκτρόνια κατανέμονται σε στρώματα στο εξωτερικό.
Τα ηλεκτρόνια στο εξώτατο κέλυφος ενός ατόμου μπορούν να μεταπηδήσουν από το ένα άτομο στο άλλο. Αυτό δίνει στο άτομο ένα διαφορετικό ηλεκτρικό φορτίο. Για παράδειγμα, εάν ένα άτομο κερδίσει ένα ηλεκτρόνιο, το φορτίο του θα είναι αρνητικό, ενώ εάν χάσει ένα ηλεκτρόνιο, το φορτίο θα είναι θετικό.
Αυτό συμβαίνει στα ιόντα, δηλαδή σε ένα άτομο που κερδίζει ή χάνει ένα ή περισσότερα ηλεκτρόνια. Για παράδειγμα, το χλώριο έχει 17 ηλεκτρόνια, αλλά μπορεί να κερδίσει ένα ηλεκτρόνιο για να γίνει ένα χλωριούχο ανιόν.-, με 18 ηλεκτρόνια και αρνητικό φορτίο.
Το ηλεκτρόνιο ανακαλύφθηκε το 1897 από τον J.J. Thomson, το ίδιο με το ατομικό μοντέλο της "πουτίγκα σταφίδας".
Το ηλεκτρόνιο αποτελείται από ένα στοιχειώδες σωματίδιο που είναι το λεπτόνιο.
Η μάζα ενός ηλεκτρονίου είναι σχεδόν 2000 φορές μικρότερη από αυτήν του πρωτονίου και του νετρονίου. Ας υποθέσουμε ότι ένα πρωτόνιο ή νετρόνιο ήταν το μέγεθος μιας μπάλας μπόουλινγκ 10 λιβρών, τότε το ηλεκτρόνιο θα ήταν το μέγεθος ενός μικρού μαρμάρου.
Επομένως, η μάζα των ηλεκτρονίων σε ένα άτομο είναι αμελητέα κατά τον υπολογισμό της ατομικής μάζας.
Πώς να υπολογίσετε τα ηλεκτρόνια ενός ατόμου;
Ο αριθμός των ηλεκτρονίων σε ένα ουδέτερο άτομο είναι ίσος με τον αριθμό των πρωτονίων σε αυτό το άτομο. Για παράδειγμα, το Au gold έχει 79 πρωτόνια, επομένως θα έχει 79 ηλεκτρόνια.
Μπορεί επίσης να σας ενδιαφέρει να δείτε:
- Κατιόντα και ανιόντα
- Άτομα και μόρια.
βιβλιογραφικές αναφορές
Myers, R.L. (2005) Τα βασικά της Φυσικής. Γκρίνγουντ.
Peake, Β.Μ. (1989) Η ανακάλυψη του ηλεκτρονίου, του πρωτονίου και του νετρονίου. J. Chemical Education 66: 738. DOI: 10.1021 / ed066p738


