Neutronid, prootonid ja elektronid: lihtne MÄÄRATLUS

Pilt: Preparaniños.com
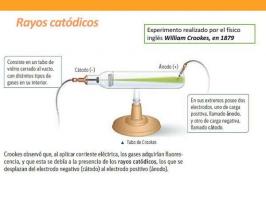
The aatomid on klassikalise keemia järgi aine struktuuriüksus. See tähendab, et kõik, mis on meie ümber ja mida võime tajuda ükskõik millise meele kaudu, koosneb aatomitest. Kogu 19. sajandi vältel uskusid teadlased, et aatomist pole midagi väiksemat. 20. sajandi esimestel kümnenditel avastasid selle sellised teadlased nagu Thomson, Stoney või Einstein Aatomid, isegi kui nad olid väga väikesed, võiks jagada teisteks osakesteks, neutroniteks, prootoniteks ja elektronid.
Kõigi nende osakeste komplekti nimetatakse subatoomseteks osakesteks. Selles õpetajatunnis vaatame üle neutronite, prootonite ja elektronide lihtne määratlus ning nende erinevused ja sarnasused.
Indeks
- Mis on prooton: lihtne määratlus
- Neutroni määratlus
- Elektroni määratlus
Mis on prooton: lihtne määratlus.
The prooton on üks subatoomilised osakesed mis on igaühe keskel aatom(tuum). Sama aatomirühma prootonid ja neutronid moodustavad koos tuum aatomitest, nii et neid kahte osakest nimetatakse ka
nukleonid. Erinevalt teistest aatomi osadest on prootoni positiivne laeng 1,6 × 10-19 C ja öeldakse, et see on väga stabiilne kuna prootoni poolväärtusaeg võib ulatuda rohkem kui 10-ni35 aastat.Lisaks sellele, et prooton on väga stabiilne osake, on see ka uskumatult raske teie suuruse jaoks: 1,672621898 × 10−27 kg, seega on see 1836 korda raskem kui elektron, kuid samal ajal on see sada tuhat korda väiksem kui terve aatom.
Nagu me varem nägime, ei ole aatomid jagamatud, aga ka subatoomilised osakesed. 1970. aastatel avastati, et prootonid on koosneb kolmest kvarkist. Neid kolme kvarki ühendab liimid, seega leitakse, et prootonid klassifitseeritakse subatomiliste osakeste rühma barüonid (osakesed, mis koosnevad kolmest kvarkist). Lisaks nende kvarkide arvule klassifitseeritakse subatoomsed osakesed vastavalt nende pöörlemisele, see tähendab nende pöörlemisele; selles klassifikatsioonis on prootonid fermionid kuna neil on 1/2 ħ pöörlemine (poole täisarvuga pöörlemisosakesed).
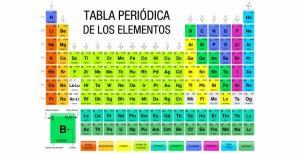
Prooton on oluline osake erinevate keemiliste elementide aatomite kõige olulisemate omaduste määramisel. The prootonite arv aatomis määrab sama aatomnumber ja koos sellega keemiline element, kuhu see kuulub. Näiteks on kõigi aatomite, mille tuumas on 20 prootonit, aatomnumber 20 ja need on kaltsiumi (Ca) aatomid.
Pilt: võrdlevad tabelid
Neutroni määratlus.
Nagu me varem nägime, leitakse neutroneid moodustades aatomite tuuma koos prootonitega. Kõigil aatomitel on tuumas prootonid, välja arvatud protio, mis on aatom, mis koosneb ainult ühest prootonist ja ühest elektronist ning mille tuumas pole neutronit.
The neutronid ja prootonid jaga mõnda Funktsioonid nagu teie kaal. Nende kahe osakese mass on enam-vähem sarnane ja palju suurem kui elektronil. Neutronid, nagu prootonid, koosnevad kolmest kvarkist, mistõttu need ka kuuluvad barüonid ja neil on 1/2 ħ pöörlemine, nii et neid arvestatakse fermionid (pool-täisarv spinni osakesed).
Midagi, mis eristab prootoneid ja neutroneid, on nende poolestusaeg: kui prooton oli väga stabiilne, on neutron osake väga ebastabiilne ja selle poolestusaeg on ainult umbes 14,7 minutit.

Elektroni määratlus.
Elektronidel on mõned omadused, mis muudavad nad väga erinevaks ülejäänud tuuma osakesest. Esiteks on elektronid ainsad subatoomilised osakesed, mida võib leida kahes vormis: vaba või moodustavad aatomi osa.
Teine erinevus on aatomi kohas, kus nad asuvad: elektronid ei ole tuuma osa aatomi, nad ei ole keskmes, kuid on perifeerias, ümbritsevad selle ja moodustavad nn Ajukoor aatomi. Öeldakse elektronid orbiidil ümber tuuma, nagu päikesesüsteemi planeedid ümber Päikese. Nende pöörlemise järgi võetakse arvesse elektrone fermionid kuna nende spinn on ± 1/2 ħ, (pool tervet tsentriosakest).
Elektron on osake a-ga prootonilaadne laeng (1,6 × 10−19 C), kuid vastupidise märgiga, see tähendab, et prootonitel ja elektronidel on jõud, mis on enam-vähem sama intensiivsusega, kuid neil on vastupidine meel. Ka elektronid on üsna stabiilne: poolväärtusaeg on umbes 4,6 × 1026 aastat.
Midagi, mis eristab elektrone teistest subatoomsetest osakestest, mida oleme näinud eespool on see, et nad on ainsad, mis pole seni tõestatud, et koosnevad ühikutest väiksem. Elektronid tegelikult oleksid leptonid, osakesed, mida praegu arvatakse olevat tõelised elementaarosakesed ja mis ei koosne muudest väiksematest elementidest. Elektronid oleksid elementaarosakesed, prootonid ja neutronid on aga aatomi alamatomid (väiksemad kui aatom), kuid mitte elementaarsed.

Pilt: slaidijaotus
Kui soovite lugeda rohkem artikleid, mis on sarnased Neutronid, prootonid ja elektronid: lihtne määratlus, soovitame sisestada meie kategooria Aatom.
Bibliograafia
- Belmonte, A. (25. juuni 2019) Subatoomilised osakesed: määratlus ja omadusedMaría del Mar (2. oktoober 2018) Aatom - mis see on, struktuur ja koostis.
- Prepara Niños (s.f) Mis on aatom: selgitus lastele.