Atomirakenne ja ominaisuudet

Kuva: SlidePlayer
Atomit ovat osa maailmaa. Kaikki aine on valmistettu atomeista, joten on tärkeää ymmärtää paremmin, mistä ne koostuvat ja mitkä ovat niiden toiminnot. Tässä OPETTAJAN oppitunnissa kerromme sinulle mitä atomin rakenne ja ominaisuudet. Jos haluat tietää enemmän aineen muodostavista hiukkasista, jatka tämän artikkelin lukemista.
Indeksi
- Mitä atomit ovat?
- Atomin rakenne
- Atomin pääominaisuudet
- Mitä ovat isotoopit?
- Kuinka atomit löytyvät luonnosta?
Mitä atomit ovat?
atomi se on pienin yksikkö, johon aine voidaan jakaa menettämättä kemiallisia ominaisuuksiaan eli kemiallisten alkuaineiden ominaisuuksia. Atomi on kaiken, mitä voi nähdä tai koskettaa, alkuperä tähdistä aamupalaan.
Jos jätämme sivuun sen kemiallisten ominaisuuksien menetyksen, voimme sanoa, että atomi koostuu erilaisista hiukkasista, joita kutsutaan subatomisiksi hiukkasiksi. Subatomisia hiukkasia on kolme tyyppiä -protonit, neutronit ja elektronit- joilla on erilaiset ominaisuudet.
Nämä hiukkaset on ryhmitelty eri numeroiksi kemiallisten alkuaineiden (happi, hiili jne.) Muodostamiseksi, mutta ne jakautuvat aina kiinteän rakenteen mukaisesti.

Kuva: Google-sivustot
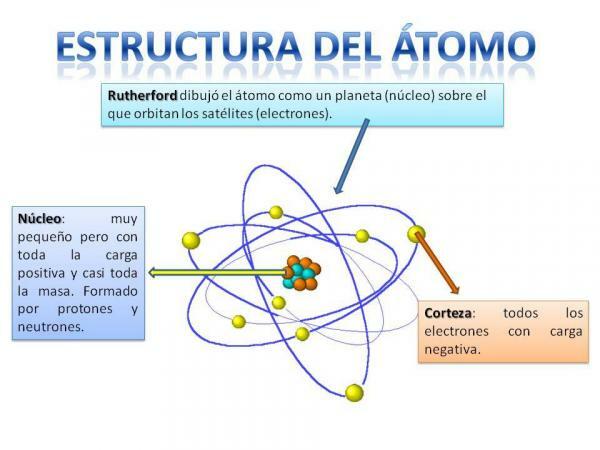
Atomin rakenne.
Atomin rakenne on kiinteäeli meillä voi olla erityyppisiä atomeja (vetyatomi, happiatomi jne.), mutta niiden subatomiset hiukkaset on järjestetty aina samalla tavalla kuin planeettajärjestelmä.
Muistat varmasti, kuinka aurinkokunta on järjestetty: aurinko on keskellä ja ympäri tästä lähtien planeetat pyörivät kuvaamalla eri kiertoratoja, jotkut lähempänä ja toiset kauempana Aurinko. Atomien tapauksessa keskellä on ydin, jonka muoto on karhunvatukan kaltainen ja koostuu neutronit ja protonit.
Ytimen ympärillä on Aivokuori mikä on alue, jonka läpi elektronit. Aikaisemmin ajateltiin, että elektronit kuvasivat tiettyjä kiertoratoja, samalla tavalla kuin planeetat tekevät, vaikka nyt se onkin tietää, että nämä kiertoradat eivät ole niin tarkasti määriteltyjä ja ovat pikemminkin alueita, joille olemme todennäköisemmin löytäneet itsemme elektronit.
Kuva: REA - Plan Ceibal
Atomin pääominaisuudet.
Tämän atomin rakennetta ja ominaisuuksia koskevan oppitunnin jatkamiseksi on tärkeää keskittyä elementteihin, jotka tekevät atomin sellaiseksi.
Ja tätä varten meidän on vastattava tähän kysymykseen: Miksi kaikki atomit päättävät järjestää itsensä tällä tietyllä tavalla? Vastaus on yksinkertainen: se johtuu sähköisen vetovoiman voimat. Atomin ydin koostuu neutronista, jolla ei ole sähkövarausta, ja protoneista, joilla on positiivinen sähkövaraus. ja elektroneilla on negatiivinen sähkövaraus, joten ytimen ja elektronien välillä on samanlainen houkutteleva voima syntyy magneetin kahden napan välissä, mutta ei ole riittävän vahva elektronien "putoamiseen" ydin.
Tämä ymmärretään paremmin, jos otamme huomioon ytimen koko: jos atomilla olisi esimerkiksi jalkapallostadionin ulottuvuus, ytimen pallomitta olisi keskellä kentältä Kuinka paljon houkuttelevaa voimaa jalkapallon pitäisi saada aikaan, että stadionin valkaisuainteet putoavat siihen!
Neutronien toiminta
Nyt saatat miettiä, ja mikä rooli neutroneilla on? Huolimatta siitä, ettei niillä ole sähkövarausta, neutroneilla on suuri rooli atomissa: ne tuottavat 99% massasta. Jos se auttaa sinua muistamaan, voimme sanoa, että atomi on kuin kolmen ystävän jengi: raskas neutroni, positiivinen protoni ja negatiivinen elektroni, joka kiertää neutronia ja elektroni.
Elektronien liike
Haluan tässä vaiheessa palata johonkin, jonka olimme jättäneet mustepesään: kiertoradat, joita elektronit kuvaavat ytimen ympärillä. Olimme sanoneet sen elektronit pyörivät ytimen ympäri Kuten planeetat tekevät ympäri Auringon, jotkut lähempänä kuin toiset, miksi he tekevät sen? Elektronit pyörivät yhdessä tai toisessa kuoressa sen energian mukaan, jonka heidän on siirryttävä pois ytimestä, toisin sanoen niillä elektronilla, jotka ovat lähempänä ydintä, ei ole riittävä voima siirtyä pois ytimestä, kun taas kuoren uloimmilla kerroksilla (orbitaaleilla) olevilla on enemmän energiaa ja ne ovat voineet siirtyä kauemmas ytimestä. ydin. Lisäksi jokaisella kiertoradalla on enintään 8 elektronin kapasiteetti (oktetin sääntö).
Atomin hiukkaset
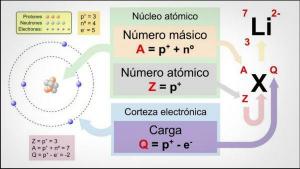
Aiomme palata toiseen lähestymistapaan, jonka olemme tehneet aiemmin, mutta emme ole selittäneet: atomit koostuvat neutronit, protonit ja elektronit, jotka yhdistävät aina saman ytimen ja kuoren rakenteen, mutta tekevät ne eri määrinä muodostaen eri kemialliset alkuaineet. Kuinka voimme saada niin monta elementtiä, joissa yhdistyvät vain 3 tyyppisiä hiukkasia? Kemiallisille alkuaineille, joita olet koskaan nähnyt edustavan jaksollisessa taulukossa, on ominaista tietty atomiluku.
atominumero (Z) Se kertoo meille protonien lukumäärän tämäntyyppisten atomien ytimessä, joka on yhtä suuri kuin elektronien lukumäärä normaaleissa olosuhteissa. Siten esimerkiksi kaikki atomit, joissa on 6 protonia (Z = 6), ovat hiiliatomeja, ja niillä on samat kemialliset ominaisuudet; atomit, joissa on 5 protonia (Z = 5), ovat booriatomeja, joilla on samat kemialliset ominaisuudet kuin toisiinsa ja jotka eroavat hiiliatomien atomista. Sinun ei tarvitse sekoittaa atomilukua atomipainoon tai massanumero (A), joka on neutronien ja protonien painon summa (elektronien paino on merkityksetön koko ytimen painoon nähden).

Kuva: SlidePlayer
Mitä ovat isotoopit?
Luonnossa voimme löytää erilaisia "alatyyppejä" elementtejä, isotoopit. Olen varma, että jossain vaiheessa olet kuullut hiilestä 14, hiilen radioaktiivisesta isotoopista, jota käytetään muun muassa fossiilien iän määrittämiseen. Isotoopit ovat kaksi atomia samalla protonimäärällä (sama atomiluku), mutta eri määrä neutroneja (eri atomimassa). Saman elementin isotoopit nimetään yleensä elementin nimen ja sen atomimassan kanssa.
Esimerkissämme molemmat isotoopit ovat hiiltä, joten niiden atomiluku on 6 (Z = 6) mutta hiili 12 ("normaali" hiili) on atomipaino 12 verrattuna hiilen 14 atomipainoon 14. Saman alkuaineen isotoopeilla on hyvin samanlaiset kemialliset ja fysikaaliset ominaisuudet. Hiilen 14 tapauksessa, toisin kuin hiili 12, se on radioaktiivinen isotooppi, jota on kaikissa hiiltä sisältävissä alkuaineissa, mukaan lukien elävät olennot.
Ja tällä päätämme tämän oppitunnin atomin rakenteesta ja ominaisuuksista. Toivomme, että siitä on ollut apua sinulle.

Kuva: Tehtäväsi
Kuinka atomit löytyvät luonnosta?
Atomeja löytyy erillään, mutta tavallisin asia on löytää ne yhdistetään ryhmiin olla nimeltään molekyylejä.
Molekyylit voivat koostua saman elementin atomeista (kuten happimolekyyli, joka koostuu kahdesta happi) tai ryhmillä, joissa on eri alkuaineiden (kaksi vetyatomia ja yksi hapen atomeja) molekyylin Vesi). Näitä elementtiryhmiä kutsutaan molekyyleiksi, jotka puolestaan voidaan yhdistää keskenään ja muodostamalla erilaisia yhä monimutkaisempia ryhmiä niiden reaktiivisuuden ja kemiallisen affiniteetin mukaan lähde kemialliset linkit.
Jos haluat lukea lisää artikkeleita, jotka ovat samanlaisia kuin Atomirakenne ja ominaisuudet, suosittelemme, että kirjoitat luokan Atomi.