Les 10 types d'éléments chimiques (expliqués et classés)
Combien d'éléments chimiques doivent exister dans l'univers? Cette question a encore un long chemin à parcourir, car les scientifiques créent de temps en temps leurs propres éléments chimiques artificiels.
Cependant, ce à quoi nous pouvons répondre est combien de types d'éléments chimiques doivent exister, quelque chose que nous découvrirons ensuite.
- Article associé: "Les 11 types de réactions chimiques"
Les types d'éléments chimiques
Dans la nature, nous pouvons trouver toutes sortes de substances. Ces substances ne se trouvent généralement pas à l'état pur, mais résultent de la combinaison de différents éléments ou matériaux qui, à travers différentes réactions, processus et périodes de temps, ont donné lieu à toutes sortes de la matière. Il n'y a rien dans l'univers qui ne soit le résultat de la combinaison d'atomes appartenant à différents types d'éléments chimiques, que nous verrons en profondeur.
Cependant, avant d'examiner les types d'éléments chimiques, passons en revue les sciences du secondaire et rappelons-nous ce que sont les éléments chimiques.
Nous appelons "élément chimique" une matière composée du même type d'atome, c'est-à-dire une substance atomiquement pure. Les éléments chimiques ne peuvent pas être décomposés en éléments plus simples et sont classés dans le tableau périodique des éléments en tant que matériaux purs de l'univers.
Mais méfiez-vous! Il ne faut pas confondre les éléments avec les substances simples, car dans certains cas deux ou plusieurs atomes d'un même élément peuvent composer molécules regroupées de différentes manières qui font varier certaines des propriétés physiques de l'élément en question, ces cas étant les isotopes. Par exemple, le diamant et le carbone sont des substances fabriquées à partir de l'élément chimique carbone (C). mais cela est organisé de différentes manières et aboutit à deux matériaux complètement différents.
Carl Sagan Il a dit que nous sommes de la poussière d'étoiles réfléchissant sur les étoiles. Cette belle phrase n'est pas une simple métaphore, mais un fait scientifique. Les éléments chimiques sont formés, pour autant que nous le sachions, à l'intérieur des étoiles étant le résultat de complexes processus de fusion et de fission atomique qui génèrent des éléments de plus en plus lourds, résultat d'un processus appelé nucléosynthèse.
La plupart des éléments connus peuvent être obtenus de la nature, trouvés spontanément ou formant des composés avec d'autres éléments tels que l'uranium (U), le carbone (C), le silicium (Si), l'argent (Ag) ou l'or (Au). D'autres, en revanche, ont été fabriqués en laboratoire comme l'américium (Am), le berkelium (Bk) ou le curium (Cm). Quel que soit son mode d'obtention ou s'il est présent dans la nature, selon ses propriétés, l'élément chimique en question aura des usages ou d'autres.
À l'heure actuelle, quelque 118 éléments chimiques sont connus, bien que compte tenu du fait que les humains ont été capables de fabriquer de nouveaux éléments, ce n'est qu'une question de temps avant que le tableau périodique ne s'étende.
- Vous etes peut etre intéressé: "Les 2 types d'électricité (expliqués)"
Les principaux types d'éléments chimiques
Les principaux types d'éléments chimiques sont représentés dans le tableau périodique, un système de classification créée par le chimiste russe Dmitri Mendeleev (1834-1907) qui en a posé les bases en 1869. Les éléments chimiques sont classés visuellement en fonction de leurs propriétés et caractéristiques.
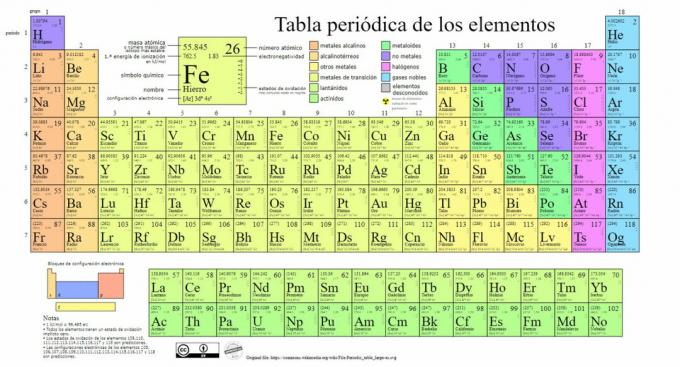
Au fil du temps et au fur et à mesure que la chimie a fait d'importantes découvertes scientifiques, ce tableau serait élargi consécutivement, atteignant la forme qu'elle a aujourd'hui avec les 118 éléments connus à ce jour.
À l'heure actuelle, dans ce tableau, nous pouvons trouver les types d'éléments chimiques suivants:
1. Métaux
Les métaux sont éléments chimiques qui contiennent généralement entre un et trois électrons dans la dernière orbite de leur atome, électrons qui peuvent être facilement transférés ce qui en fait des conducteurs de chaleur et d'électricité.
Les métaux sont généralement malléables et ductiles, avec un éclat caractéristique dont l'intensité dépend du mouvement des électrons qui composent leurs atomes. La plupart du temps, les métaux sont solides à température ambiante, à l'exception du mercure.
Parmi les métaux on retrouve l'or (Au), l'argent (Ag), le cuivre (Cu) et l'aluminium (Al) dont les caractéristiques physiques en font de magnifiques conducteurs d'électricité, bien que leur présence dans la nature soit très variée, reflétée par la différence entre leurs poids.
On pense que 75 % des éléments chimiques existant dans la nature sont des métaux, tandis que les 25 % restants seraient constitués de gaz rares, de métalloïdes et d'autres types.
Il existe des classifications dans cette catégorie, trouvant des actinides, des lanthanides, des métaux de transition, des métaux alcalins, des métaux alcalino-terreux et d'autres métaux.
- Article associé: "10 aliments riches en zinc"
1.1. Lanthanides
Les éléments lanthanides se trouvent dans des gisements composés de nombreux minéraux. Ce sont des métaux blancs qui s'oxydent facilement au contact de l'air. Parmi eux, on trouve le Lanthane (La), le Prométhium (Pm), l'Europium (Eu) et l'Ytterbium (Yb).

- Vous etes peut etre intéressé: "Les 5 types de liaisons chimiques: c'est ainsi que se compose la matière"
1.2. Actinides
Tous les isotopes des actinides sont radioactifs. Parmi eux, on trouve l'actinium (Ac), l'uranium (U), le plutonium (Pu) et l'einsteinium (Es).
1.3. Métaux de transition
Les métaux de transition sont situés dans la partie centrale du système périodique. Sa principale caractéristique est que avoir une configuration électronique de l'orbitale "d" partiellement remplie d'électrons.
Dans ce groupe il y a des substances de toutes sortes et, selon sa classification la plus large, il correspondrait aux éléments chimiques de 21 à 30, de 39 à 48, de 71 à 80 et de 103 à 112, soit un total de quarante et parmi eux on trouverait le vanadium (V), le ruthénium (Ru), l'argent (Ag), le tantale (Ta) et le lawrencio (G / D).

1.4. Métaux alcalins
Les métaux alcalins sont un groupe de six éléments composé de lithium (Li), sodium (Na), potassium (K), rubidium (Rb), césium (Cs) et francium (Fr). Ce sont des métaux brillants et mous, très réactifs à température et pression normales et perdent facilement leur électron externe, situé dans leur orbitale "s".
1.5. Terres alcalines
Les métaux alcalino-terreux sont un groupe d'éléments dans lequel on retrouve le béryllium (Be), le magnésium (Mg), le calcium (Ca), le strontium (Sr), le baryum (Ba) et le radium (Ra). Son nom vient du nom donné à ses oxydes, les "terres", qui ont des propriétés basiques ou alcalines.
Les alcalino-terreux ils sont plus durs que les alcalins, brillants et sont de bons conducteurs électriques. Ils sont moins réactifs que les alcalins et agissent comme de bons agents réducteurs. Ils ont la capacité de former des composés ioniques et ils ont tous deux électrons dans leur enveloppe la plus externe.

1.6. Autres métaux
La catégorie "autres métaux" est un type de substances que l'on trouve ici car on ne sait pas trop où les mettre.
Ce sont des éléments métalliques situés dans le tableau périodique avec les métalloïdes, dans le bloc p. Ils ont tendance à être mous avec des points de fusion bas. Parmi eux figurent l'aluminium (Al), l'indium (In), l'étain (Sn) et le bismuth (Bi) entre autres.

2. Pas de métaux
Les non-métaux possèdent généralement entre cinq et sept électrons dans leur dernière orbite, une propriété qui rend qu'ils gagnent des électrons au lieu de les abandonner et, ainsi, ils parviennent à avoir huit électrons qui les stabilisent ainsi comme atomes.
Ces éléments ce sont de très mauvais conducteurs de chaleur et d'électricité. De plus, ils n'ont pas de brillance caractéristique, sont peu malléables, peu ductiles et sont très fragiles à l'état solide. Ils ne peuvent pas être roulés ou étirés, contrairement aux métaux.
Ils sont surtout essentiels pour les systèmes biologiques, car ils sont présents dans composés organiques, tels que le soufre (S), le carbone (C), l'oxygène (O), l'hydrogène (H) et l'iode (I).

- Article associé: "Les 20 types de pierres précieuses (décrits et illustrés)"
3. Métalloïdes
Comme leur nom l'indique, les métalloïdes sont une classification intermédiaire entre les métaux et les non-métaux qui ont des propriétés des deux groupes. Cela est dû au fait qu'ils ont quatre atomes dans leur dernière orbite, une quantité intermédiaire à laquelle les métaux et les non-métaux ont.
Ces éléments chimiques ne conduisent l'électricité que dans une direction, ne permettant pas qu'elle se fasse dans la direction opposée comme c'est le cas dans les métaux. On en trouve un exemple dans le silicium (Si), un métalloïde utilisé dans la fabrication d'éléments semi-conducteurs pour l'industrie électronique grâce à cette propriété.
Les autres métalloïdes sont: le bore (B), l'arsenic (As), l'antimoine (Sb) et le polonium (Po).

4. Halogènes
Les halogènes sont un groupe de six éléments qui ils ont tendance à former des molécules composées de deux atomes (diatomique) qui sont très actifs chimiquement en raison de leur électronégativité.
Ces substances se présentent généralement sous forme d'ions, c'est-à-dire de molécules chargées électriquement, qui dans ce cas sont mononégatives, fortement oxydantes. Cela signifie que les halogènes sont des substances caustiques et corrosives.
Les halogènes sont: le fluor (F), le chlore (Cl), le brome (Br), l'iode (I), l'astate (At) et le tenese (Ts).

5. gaz nobles
Les gaz rares sont un groupe de sept dont l'état naturel est gazeux. Ils se présentent généralement sous forme de molécules diatomiques de très faible réactivité, c'est-à-dire qu'ils ne réagissent pas avec d'autres éléments composant d'autres substances et, pour cette même raison, ils sont appelés gaz inertes. En effet, dans sa dernière orbite, il y a le nombre maximum d'électrons possibles pour ce niveau, huit au total.
Ce groupe restreint d'éléments est composé d'hélium (He), de néon (Ne), d'argon (Ar), de krypton (Kr), de xénon (Xe), de radon (Rn) et d'oganeson (Og), anciennement connu sous le nom d'ununoctium.
