DEFINICIJA pozitivnih ili negativnih IONA

Kao što već znamo, atoma tvore ih subatomske čestice. Od tri vrste subatomskih čestica, samo neutroni nemaju električni naboj. Umjesto toga, protoni imaju pozitivan električni naboj, dok elektroni imaju negativan naboj. Samo se elektroni koji zauzimaju periferiju atoma mogu prenijeti s jednog atoma na drugi, dok protoni u jezgri održavaju svoj broj stabilnim. U ovoj ćemo lekciji UČITELJA vidjeti što se događa kada atomi ili molekule dobiju ili izgube elektrone. Odnosno, vidjet ćemo definicija i primjeri pozitivnih ili negativnih iona.
Indeks
- Što su ioni? Jednostavna definicija
- Stvaranje jona: elektroafinitet i elektronegativnost
- Što su negativni ioni? Uz primjere
- Što su pozitivni ioni? Uz primjere
Što su ioni? Jednostavna definicija.
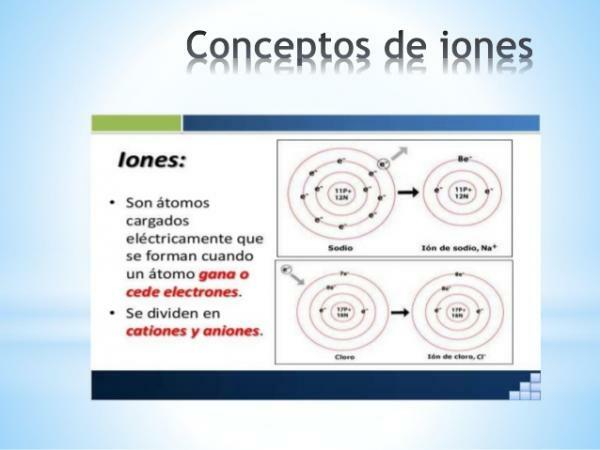
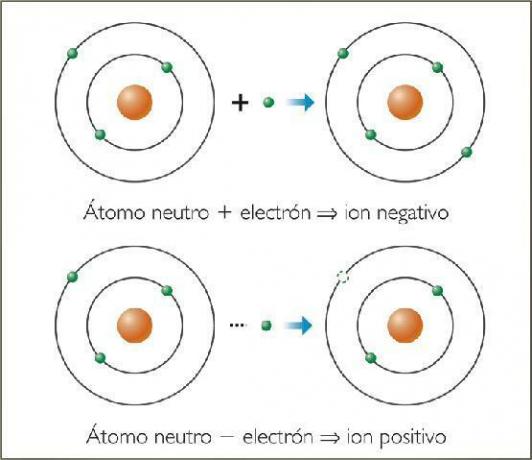
A ion je bilo koji atom ili molekula s neto električnim nabojem. Odnosno, radi se o atomu ili skupu atoma povezanih, čiji su električni naboji nisu nadoknađeni. Ta se dekompenzacija naboja događa kada se jedan ili više elektrona pridruže ili napuste atom ili skup atoma.
Ioni su tako nabijeni atomi ili molekule, zbog dobitka ili gubitka elektrona (subatomske čestice s negativnim nabojem i zanemarivom masom).
Vrste jona: monatomske i polatomne
Uzmemo li u obzir sastav iona, razlikuju se dvije vrste: monatomski i polatomni ioni.
- Kao što i samo ime govori, monatomski ioni one koje tvore a jedan atom.
- Jonski spojevi o polikatni ioni su oni u kojima su atomi kovalentno povezani (dijeleći jedan ili više parova elektrona u vezi) koji predstavljaju niz neutronima u molekuli različitoj od ukupnog broja elektrona.
- The polikatni ioni obično sadrže kisik a obično imaju strukturu sa središnjim atomom oko koje su raspoređeni preostali elementi koji čine molekulu.
- The naboj monatomskih iona reprezentativnih elemenata (obitelji 1 i 2 tablice i obitelji 13 do 17 periodnog sustava) mogu se lako utvrditi ako je poznato njihovo mjesto u periodnom sustavu. U tim slučajevima atomi dobivaju ili gube elektrone da bi u svojoj valentnoj ljusci postigli konfiguraciju plemenitog plina svog razdoblja (s2str6), ili što je isto, ispunite pravilo okteta.
Slika: Dijaprojekcija
Stvaranje iona: elektroafinitet i elektronegativnost.
Sposobnost atoma ili molekula da tvore ione određuje se s dva periodična svojstva: elektroafinitet i elektronegativnost. Oba svojstva povećavaju vrijednost tijekom razdoblja i smanjuju se kako se spuštamo kroz skupinu ili obitelj periodnog sustava.
The elektroafinitet, koji se naziva i afinitet prema elektronu, atomsko je svojstvo koje se definira kao sposobnost atoma da privlači elektrone. U slučaju spojeva, slično svojstvo tzv elektronegativnost koja se definira kao sposobnost atoma da privlači elektrone kada tvori vezu s drugim atomom. Oba svojstva tako definiraju tendenciju elementa da hvata ili gubi elektrone.
Jonske veze
U svom čvrstom obliku ioni tvore spojeve ili ionski kristali (soli), nastale kombinacijom iona različitog predznaka spojenih pomoću ionske veze. Najpoznatiji primjer ove vrste spojeva je obična sol (natrijev klorid: NaCl).
Jonska veza sastoji se od spojeva iona različitog predznaka pomoću elektrostatičkih privlačnih sila (privlačenje između naboja suprotnog predznaka). Elementi čija se elektronegativnost ili elektroafinitet vrlo razlikuju (metalni i nemetalni elementi) interveniraju u ovoj vrsti veza. U većini slučajeva ti su jonski spojevi topljiv u vodi i druga polarna otapala.
U vodenim otopinama ionski spojevi razdvajaju se na slobodne ione, koji su tzv elektroliti, budući da se zbog svoje prisutnosti u otopini voda ponaša kao električni vodič.
Što su negativni ioni? Uz primjere.
The negativni ioni Zovu se anioni. U svim su slučajevima atomi nemetalnih elemenata ili molekule koji sadrže nemetalne elemente. Ovi elementi karakterizirani su vrlo visokim elektroafinitetom i elektronegativnošću. Odnosno, oni su ioni nastali od elemenata sa velika tendencija hvatanja elektrona.
Monatomski anioni: definicija i primjeri
Oni su anioni nastali od atoma nemetalnih elemenata (skupine 13 do 17 periodnog sustava), koji su stekli jedan ili više elektrona. Tim anionima je zajednička elektronička struktura plemenitog plina (s2str6) u svojoj najudaljenijoj elektronskoj ovojnici (valentnoj ljusci).
Primjeri:
- Kloridni ion: Cl-
- Fluoridni ion: F-
- Jodidni ion: I-
- Sulfidni ion: S-2
- Nitridni ion: N-3
Poliatomski anioni: definicija i primjeri
Oni su negativno nabijeni ioni nastali od dva ili više atoma nemetalnih elemenata povezanih kovalentnim vezama. Oni su najčešći polikatni ioni. Najčešći polatomski anioni su oksoanioni koji se sastoje od središnjeg nemetalnog atoma i sadrže kisik.
Općenito se smatraju kemijskim spojevima dobivenim kada kiseli spoj izgubi jedan ili više protona (H+). Ti polihatomski anioni mogu zadržati nešto vodika u svojoj strukturi, što im daje određeni kiseli karakter (sposobnost odustajanja od protona).
Primjeri:
- Nitratni ion: NO3-
- Permanganatni ion: MnO4-
- Fosfatni ion: PO4-3
- Vodikov karbonat ili bikarbonatni ion: HCO3-
- Sulfitni ion: SO3-2
Slika: Naturopatija
Što su pozitivni ioni? Uz primjere.
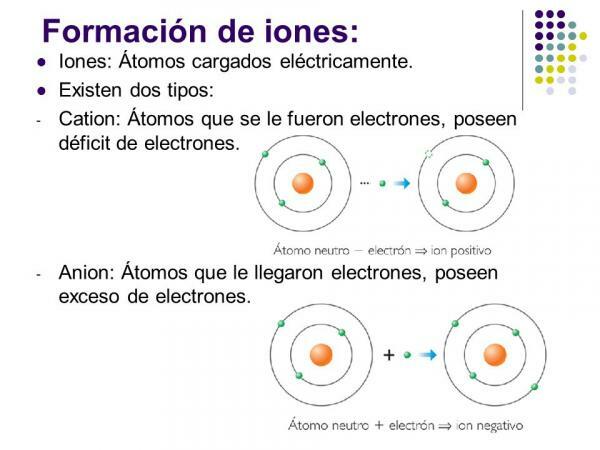
Pozitivni ioni se nazivaju cacije. U gotovo svim su slučajevima atomi metalnih elemenata ili molekule koji sadrže metalne elemente. Ovi elementi karakterizirani su vrlo niskim elektroafinitetom i elektronegativnošću, zbog čega pokazuju jasnu tendenciju gubitka elektrona.
Monatomski kationi: definicija i primjeri
Oni su ioni s pozitivnim nabojem (zbog gubitka elektrona) nastali jednim atomom metalnog elementa. U ovom slučaju, kation nastaje gubitkom elektrona koji omogućuju elementu da isprazni svoj najudaljeniji elektronički sloj i stekne konfiguraciju plemenitog plina (s)2str6) s donje razine. Oni su najčešći tip kationa.
Primjeri:
- Vodik ili hidronski kation (također se naziva i proton): H+
- Natrijev kation: Na+
- Kation željeza (III) ili željezni kation: Fe+3
- Kation kalcija: Ca+2
- Kation bakra (II) ili bakra: Cu+2
Poliatomski kationi: definicija i primjeri
Poliatomski kationi su oni koji nastaju od dva ili više atoma. Rijetki su, najzastupljeniji su takozvani homopolatomski kationi koji sadrže više od jednog atoma istog elementa, u slučaju trihidrogen iona, to je jedna od najzastupljenijih molekula u svemir. Poliatomski kationi nastali atomima različitih elemenata nisu česti, ali ih karakterizira prisutnost vodika i smatra se da potječe kada osnovni spoj uhvati proton (H+).
Primjeri:
- Amonijev kation: NH4+
- Kation oksonija: HO3+
- Kation fosfonija: PH3+
- Kation trihidrogena ili protonirani molekularni vodik: H3+
- Kation dimerkura: Hg2+2
Slika: Planeti
Ako želite pročitati više članaka sličnih Negativni i pozitivni ioni: definicija i primjeri, preporučujemo da uđete u našu kategoriju Atom.
Bibliografija
Alejandrina Gallego Picó, Rosa Mª Garcinuño Martínez, Mª José Morcillo Ortega, Miguel Ángel Vázquez Segura. (2018) Osnovna kemija. Madrid: Uned