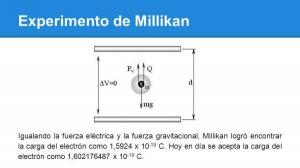
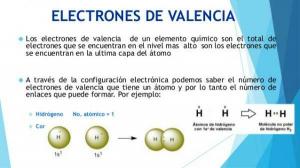
Saznajte koji je ATOMSKI BROJ
Materija se sastoji od atoma različitih kemijskih elemenata. Kemijski elementi imaju različita svojstva i karakteristike zbog kojih se međusobno razlikuju, a nedvojbeno je jedan od najvažnijih atomski broj. Atomski broj, koji je obično predstavljen s slovo "Z", predstavlja broj protona koji ima određeni atom. Atomi istog elementa imaju isti atomski broj, dok atomi različitih elemenata uvijek imaju različite atomske brojeve.
Ako ste se ikad zapitali koliki je atomski brojPozivamo vas da nastavite čitati ovu lekciju od PROFESORA kako biste znali njezinu definiciju, ali i kakve implikacije to ima na atome.
Indeks
- Atomski broj: jednostavna definicija
- Atomski broj i elementi
- Povezanost periodnog sustava i atomskog broja
- Atomski broj i neutralnost elemenata
Atomski broj: jednostavna definicija.
Ako želite znati koji je atomski broj, obratite pažnju na naše objašnjenje! Atomski broj je broj protona koji čine broj atoma određenog elementa. Obično ga predstavlja slovo "Z" (uvijek velikim slovima), koje dolazi od njemačke riječi zahl, što znači broj.
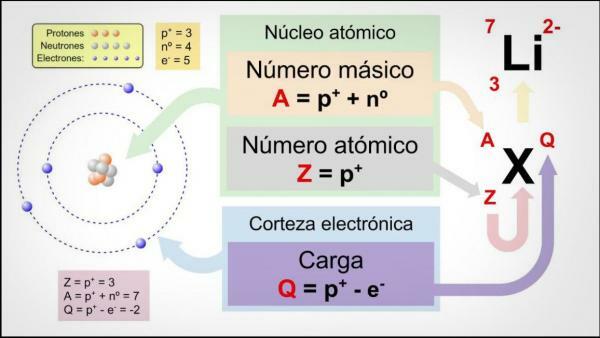
Sjetimo se da unutar atoma postoje klasično tri vrste čestica: protoni, neutroni i elektroni. U jezgri su protoni i neutroni, koji imaju najveću količinu mase u atomu. Stoga zbroj atomskog broja Z i broja neutrona N daje maseni broj A atoma.
Ponekad u prirodi možemo pronaći atome s istim atomskim brojem (Z), ali različitim brojem neutrona (N), a time i različitim atomskim masama. Ti su atomi poznati kao izotopi. Ako želite znati više o Karakteristike izotopa možete pogledati našu lekciju o toj temi.
Atomski broj ima mnogo primjena u fizici i kemiji. U sljedećim odjeljcima vidjet ćemo, uz njegovu glavnu korisnost, za što su fizičari i kemičari koristili atomski broj.
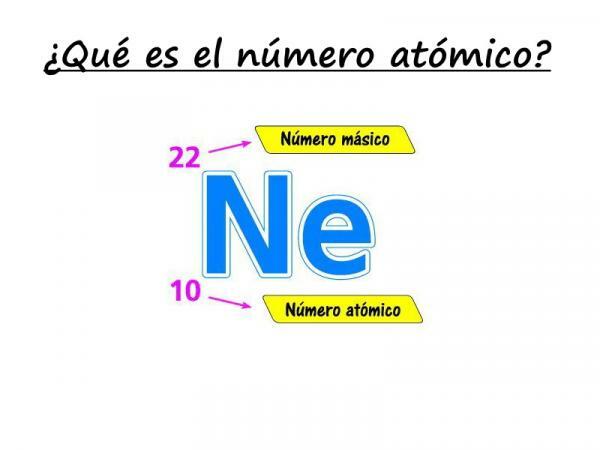
Slika: Definicija
Atomski broj i elementi.
Sad kad znamo koji je atomski broj, pogledajmo njegovu upotrebu. The glavna korisnost atomskog broja u fizici i kemiji je definirati atome istog elementa. Toliko je važno da se potraga za novim elementima obično vrši pomoću atomskih brojeva.
Atom može imati isti broj elektrona kao i drugi, a ne biti atomi istog elementa. S druge strane, ako je atomski broj dvaju atoma jednak, nužno oba atoma pripadaju atomima istog elementa.
Atomi, u svom čistom prirodnom stanju kao kemijski elementi, oni su u ovoj neutralnoj. Stoga će, prema načelima kvantne mehanike, to biti broj protona u jezgri atom koji određuje broj elektrona koje može držati u svojim orbitalama, koje okružuju jezgra. Broj elektrona, osobito najudaljenija valentna ljuska, primarni je čimbenik u određivanju njihovog kemijskog ponašanja.
Stoga je atomski broj činjenica da se određuje kemijska svojstva elementa. Iz tog se razloga element može definirati kao konzistentan ako imamo smjesu atoma s danim atomskim brojem.

Slika: 100Cia.site
Povezanost periodnog sustava i atomskog broja.
Kao što smo ranije vidjeli, atomski broj ili broj protona u jezgri je ono što stvarno određuje broj elektrona koji određeni atom može imati. Zbog toga, neizravno, atomski broj određuje redoslijed elementi u periodnom sustavu.
Ako ste se ikad morali suočiti s proučavanjem periodnog sustava elemenata, možda ste se zapitali koji su kriteriji slijedili prilikom naručivanja tih elemenata? Jesu li slučajno poredani? Možda prema njihovom redoslijedu otkrića? Pa ne, oni su raspoređeni prema redoslijedu punjenja elektroničke orbitale.
Kao što smo već vidjeli, atomski broj u konačnici određuje broj elektrona koji atom može imati. Stoga atomski broj definira elektronska konfiguracija atoma. Zbog toga neizravno atomski broj omogućuje poredak različitih kemijskih elemenata u tablici periodična, koja započinje vodikom (Z = 1), a nastavlja se helijem (Z = 2), litijem (Z = 3), berilijem (Z = 4), borom (Z = 5), ugljikom (Z = 6) itd.

Slika: Pinterest
Atomski broj i neutralnost elemenata.
Normalno, redovno, kemijski elementi obično se izražavaju kao neutralni atomi ili molekule ali ne moraju uvijek biti. Ponekad neki atomi ili molekule imaju više ili manje elektrona nego što bi trebali. U slučaju da atom ili molekula imaju dužne elektrone i nemaju električni naboj, (električno neutralni), atomski broj bit će jednak broju elektrona u atomu koji se mogu naći oko Korteks.
U drugim slučajevima, atomi mogu imati veći broj elektrona nego što im odgovara njihov atomski broj, a toliko ih je negativno nabijenih. To su tzv anioni. Inače, broj elektrona u atomu ili molekuli manji je od atomskog broja i oni će biti pozitivno nabijeni. Suočili bismo se s kationom.
Ti elektroni uglavnom određuju kemijsko ponašanje atoma i oni će biti vrlo važni u određivanju međusobnog odnosa različitih atoma ili molekula.
Ako želite pročitati više članaka sličnih Koji je atomski broj, preporučujemo da uđete u našu kategoriju Atom.
Bibliografija
- Nuklearna energija (20. svibnja 2019.) Atomski broj. Oporavljen od https://energia-nuclear.net/que-es-la-energia-nuclear/atomo/numero-atomico
- Recio Miñarro, J. (s.f) Atomski broj i maseni broj. Oporavljen od http://newton.cnice.mec.es/materiales_didacticos/el_atomo/zya.htm? 4&0
- Wikipedia (25. siječnja 2020.) Atomski broj. Oporavljen od https://es.wikipedia.org/wiki/N%C3%BAmero_at%C3%B3mico