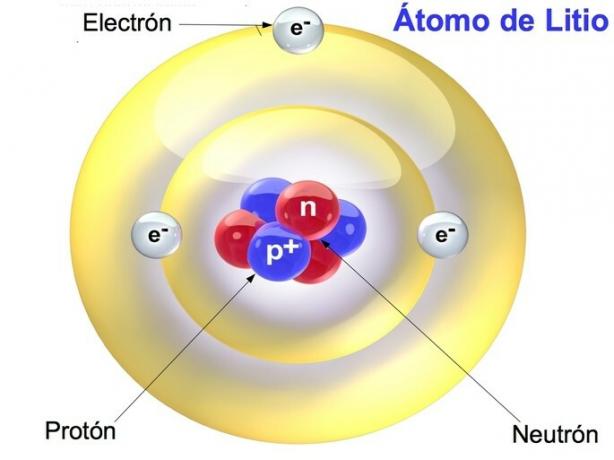
Protoni, neutroni i elektroni
Protoni, neutroni i elektroni su čestice koje čine atom, što je najmanji dio elementa. Te čestice određuju karakteristike i svojstva kemijskih elemenata.
Protoni i neutroni koncentrirani su u atomskoj jezgri, dok su elektroni raspoređeni u kori ili na periferiji atoma. Atom ima jednak broj elektrona i protona, dok je broj neutrona promjenjiv.
Dalje, predstavljamo usporednu tablicu između protona, neutrona i elektrona.
| Proton | Neutron | Elektron | |
|---|---|---|---|
| Definicija | Subatomska čestica pozitivnog naboja | Subatomska čestica neutralnog naboja | Negativno nabijena subatomska čestica |
| Opterećenje | Pozitivan +1 |
Neutralno 0 |
Negativan -1 |
| Simbol | str+ | n0 | i- |
| Mjesto u atomu | Jezgra | Jezgra | Periferne orbitale |
| Masa (kg) | 1.673 x 10--27kg | 1.675 x 10--27kg | 9.109 x 10--31kg |
| Masa u usporedbi s protonom (amu) | 1 | 1 | 0,0005 |
| Elementarna čestica | 3 kvarka: 2 u i 1 d | 3 kvarka: 2 d i 1 u | 1 lepton |
| Otkrivač (godina) | I. Rutherford (1911) | J. Chadwick (1931) | J.J. Thomson (1897) |
Što je proton?
Protoni su pozitivno nabijene čestice koje se nalaze u jezgri atoma. Svaki atom elementa ima fiksni broj protona, što određuje njegov atomski broj, odnosno Z. Dakle, vodik ima proton, a Z jednako 1.
Masa protona je 1,673 x 10-27 kg, što predstavlja 1 jedinicu atomske mase ili amu (za kraticu na engleskom jedinica atomske mase).
Godine 1911. Ernest Rutherford otkrio je da je jezgra atoma sićušna i pozitivno nabijena, otuda i koncept protona.
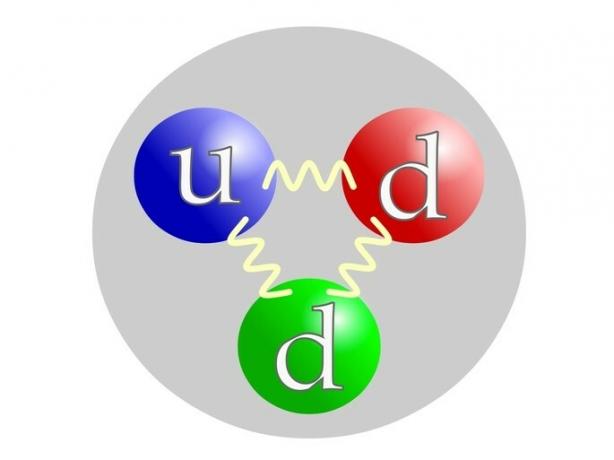
Proton se sastoji od elementarnih čestica koje se nazivaju kvarkovi ili kvarkovi: 2 kvarka u (po gore= vrh) i 1 kvart d (po dolje= dolje).

Kako izračunati protone atoma?
Broj protona u atomu može se odrediti iz njegovog atomskog broja, koji je broj položaja na periodnom sustavu.
Na primjer, zlato Au ima atomski broj = 79, što znači da zlato u svojoj jezgri ima 79 protona.
Što je neutron?
Neutroni su čestice koje se nalaze u jezgri atoma zajedno s protonima. Označeni su slovom n a oni su neutralno nabijeni. Jedini element koji nema neutrone je vodik.
Masa neutrona vrlo je slična masi protona, pa zbroj masa protona i neutrona određuje atomsku masu elementa.
Atomi koji imaju jednak atomski broj, ali različit broj neutrona nazivaju se izotopima. Primjerice, deuterij je izotop vodika koji u jezgri ima neutron i proton.
Engleski fizičar James Chadwick otkrio je tu subatomsku česticu 1931. godine, s masom bliskom protonu, ali s neutralnim električnim nabojem, zbog čega je nazvana neutronom.
Neutron su poput protona sastavljeni od kvarkova: 1 kvar u (po gore= vrh) i 2 kvarta d (po dolje= dolje).
Kako izračunati neutrone atoma?
Broj neutrona u atomu možemo izračunati ako znamo njegovu atomsku masu i njegov atomski broj Z. Već znamo da je atomski broj Z broj protona, a atomska masa zbroj protona i neutrona koje ima atom.
Na primjer, kisik ima atomsku masu 16, a Z 8. Broj protona u kisiku jednak je atomskoj masi minus Z:
16 - 8 = 8 neutrona
Što je elektron?
Elektroni su čestice atoma koje se nalaze u oblaku koji okružuje jezgru. Dok su protoni i neutroni koncentrirani u jezgri, elektroni se izvana raspoređuju u slojevima.
Elektroni u najudaljenijoj ljusci atoma mogu skakati s jednog atoma na drugi. To daje atomu drugačiji električni naboj; na primjer, ako atom dobije elektron, naboj će mu biti negativan, dok ako izgubi elektron, naboj će biti pozitivan.
To se događa u ionima, odnosno atomu koji dobiva ili gubi jedan ili više elektrona. Na primjer, klor ima 17 elektrona, ali može dobiti jedan elektron da postane Cl kloridni anion.-, sa 18 elektrona i negativnim nabojem.
Elektron je 1897. otkrio J.J. Thomson, isti čovjek iz atomskog modela "pudinga od grožđica".
Elektron se sastoji od elementarne čestice koja je lepton.
Masa elektrona gotovo je 2000 puta manja od mase protona i neutrona. Pretpostavimo da su proton ili neutron bili veličine kugle za kuglanje od 10 kilograma, tada bi elektron bio veličine malog mramora.
Stoga je masa elektrona u atomu zanemariva pri izračunavanju atomske mase.
Kako izračunati elektrone atoma?
Broj elektrona u neutralnom atomu jednak je broju protona u tom atomu. Na primjer, Au zlato ima 79 protona, stoga će imati 79 elektrona.
Možda će vas zanimati i sljedeće:
- Kationi i anioni
- Atomi i molekule.
Reference
Myers, R.L. (2005.) Osnove fizike. Greenwood.
Peake, B.M. (1989) Otkriće elektrona, protona i neutrona. J. Kemijsko obrazovanje 66: 738. DOI: 10.1021 / ed066p738