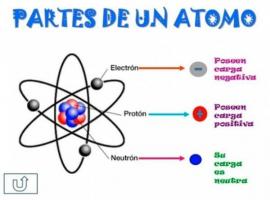
Bagian-bagian atom dan ciri-cirinya
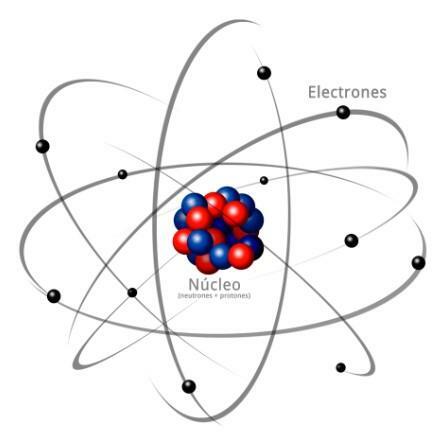
Gambar: Answers.tips
Atom adalah unsur dasar yang materi bentuk, hadir di semua keadaan materi. Mereka adalah elemen yang sangat kecil, tidak mungkin untuk dilihat melalui mata manusia tetapi mereka sangat penting bagi alam semesta kita. Untuk lebih memahami bagaimana atom dan cara kerjanya, dalam pelajaran dari GURU ini kita akan berbicara bagian-bagian atom dan ciri-cirinya.
Semua atom terdiri dari inti dan kerak. Nukleus, seperti namanya, adalah bagian tengah atom, di mana partikel-partikel yang bermuatan positif dan disebut proton, dan partikel yang muatannya netral, yaitu tidak bermuatan listrik, diberi nama neutron. Massa kedua partikel, baik proton maupun neutron, serupa. Semua atom dari unsur kimia yang sama memiliki jumlah proton yang sama, angka ini disebut nomor atom dan huruf Z digunakan untuk mewakilinya.
Di sisi lain ada korteks Apakah yang bagian luar atom. Di kulit kayu kita menemukan elektron, yang merupakan partikel bermuatan negatif. Elektron berputar dengan kecepatan tinggi di sekitar nukleus pada tingkat yang berbeda, menjadi partikel yang jauh lebih kecil daripada yang terletak di nukleus.
Menjadi neutron netral, proton positif dan elektron negatif, atom memiliki muatan listrik netral, karena mereka memiliki jumlah proton yang sama dengan elektron. Meskipun ada kasus di mana jumlah elektron lebih sedikit atau lebih besar dari proton, menyebabkan muatan atom itu negatif atau positif, dalam hal ini ia menerima nama ion, anion jika negatif atau kation jika positif.
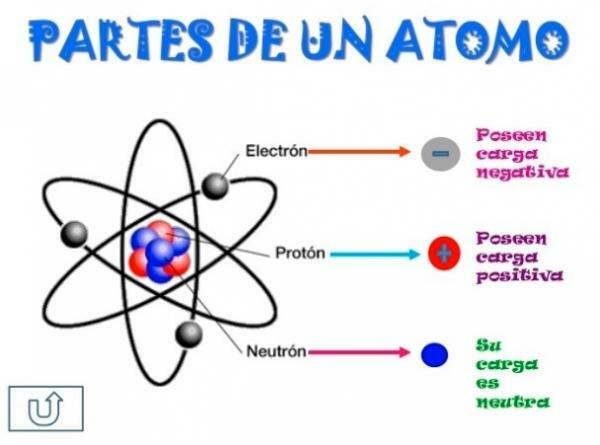
Gambar: Brainly
Untuk melanjutkan pelajaran ini tentang bagian-bagian atom dan karakteristiknya, kita harus berbicara tentang evolusi yang dimiliki bagian-bagian atom, sejak model atom telah berubah dari waktu ke waktu berkat penelitian para ilmuwan. Perlu dicatat bahwa beberapa model yang akan kami jelaskan sudah usang, tidak digunakan saat ini, tetapi mereka diperlukan untuk memahami evolusi komunitas ilmiah tentang hal ini.
Evolusi historis model atom ditandai dengan: ilmuwan berikut:
- Model Dalton: Model atom pertama adalah karya John Dalton pada tahun 1803. Ini adalah model yang sangat primitif yang kehilangan banyak elemen seperti keberadaan elektron dan proton.
- Model Thomson: John Thomson berhasil membuat model atom yang lebih lengkap daripada model Dalton, dengan menambahkan beberapa elemen kunci. Thomson menemukan keberadaan elektron dan muatan positif dan negatif.
- Model Nagaoka: Fisikawan Jepang Nagaoka tidak setuju dengan model Thomson, ia berpikir bahwa atom harus memiliki inti bermuatan positif yang besar di mana elektron bermuatan negatif berputar. Teorinya disebut Saturnus, karena ia membandingkan elektron dengan cincin Saturnus. Banyak kali model ini tidak disebutkan namanya, tetapi penting untuk memahami langkah besar yang diambil saat ini.
- Model Rutherford: Model Rutherford didasarkan pada keberadaan inti bermuatan positif di mana elektron bermuatan negatif berputar. Model ini sangat mirip dengan Nagaoka, menjadi tahun yang sangat dekat, meskipun model Jepang lebih awal.
- Model Bohr: Bohr berpikir bahwa elektron harus berjauhan dari inti berlapis dan jumlah partikel orbital ini harus sama dengan nomor atom. Modelnya juga memahami bahwa jumlah elektron bervariasi di setiap kulit, dengan lebih sedikit elektron di kulit pertama daripada di kulit terakhir.
- Model Schrodinger: Schrodinger mematahkan keyakinan bahwa elektron adalah partikel kecil yang berputar di sekitar nukleus. Ilmuwan Austria berpendapat bahwa elektron bergerak melalui fungsi gelombang, yaitu dengan, bentuk orbit.
- Model Dirac: Dirac memodifikasi ide Schrodinger untuk modelnya, menggunakan "persamaan Dirac" untuk memberikan pandangan yang lebih tepat tentang bentuk orbital elektron.