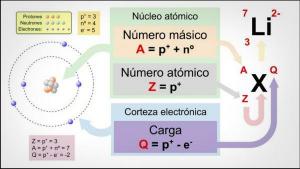
Bagaimana cara mendapatkan NOMOR MASSA?

Atom adalah bagian dari semua materi yang membentuk alam semesta. Materi sangat bervariasi karena terdiri dari berbagai jenis atom, dengan karakteristik dan sifat yang berbeda. Karakteristik atom yang berbeda diberikan oleh partikel yang membentuknya: proton, elektron, dan neutron. Proporsi yang berbeda antara satu dan yang lain didefinisikan dalam kimia dengan nama yang berbeda (nomor massa, nomor atom, dll.). Nomor massa memberi kita jumlah akhir atau jumlah total partikel dalam nukleus, atau yang sama, itu adalah membuat jumlah antara proton dan neutron, dan digunakan dalam kimia untuk membedakan isotop suatu unsur bahan kimia.
Dalam pelajaran ini dari seorang GURU kita akan melihat nomor massa, cara mendapatkannya, apa sebenarnya itu dan untuk apa digunakan.
Indeks
- Berapa nomor massanya?
- Nomor massa dan isotop
- Bagaimana cara menghitung nomor massa? - Rumus
Berapa nomor massanya?
Itu nomor massa itu tidak lebih dari jumlah proton dan neutron, yaitu, semua partikel yang ada di dalam nukleus (ingat bahwa elektron mengorbit di sekitar nukleus, membentuk kerak).
Nomor massa ditulis dengan huruf a dan itu ditunjukkan dalam situasi superscript, selalu di sebelah kiri simbol yang menunjukkan elemen yang kita hadapi, itu adalah yaitu, kita akan menemukannya sebagai angka kecil yang ditempatkan di sebelah kiri simbol elemen, di atas ini. Ini mewakili massa atom yang diukur dalam u.m.a (satuan massa atom) karena massa elektron sangat kecil, sangat kecil sehingga dapat diabaikan atau diabaikan.
Jumlah massa atom biasanya digunakan untuk membedakan isotop dari suatu unsur kimia.

Gambar: Berbagi slide
Nomor massa dan isotop.
Isotop adalah varian dari unsur kimia yang sama yang memiliki jumlah neutron yang berbeda sehingga beda nomor massa. Isotop dapat terjadi secara normal di alam (isotop alami) atau seluruhnya buatan manusia (isotop buatan). Contoh isotop di alam adalah isotop karbon:
Karbon terjadi sebagai campuran dari tiga isotop dengan nomor massa 12, 13, dan 14: 12C, 13C dan 14C.
Isotop memiliki banyak aplikasi: mereka digunakan untuk perawatan kanker, menentukan munculnya racun dalam jaringan seperti arsenik, penanda reaksi kimia, dll.
Setiap isotop suatu unsur kimia dapat memiliki karakteristik yang berbeda. Salah satu karakteristik yang paling dikenal dan paling banyak digunakan adalah waktu paruh konstan atau waktu paruh konstan setengah hidup. Waktu paruh suatu isotop adalah waktu yang diperlukan oleh setengah inti dalam sampel awal radioisotop untuk hancur. Dalam praktiknya, isotop cenderung hancur, berubah dari bentuk yang kurang stabil ke bentuk yang lebih stabil. stabil, jadi ini juga dapat dipahami sebagai waktu yang diperlukan untuk mentransmutasikan atau mengubah setengah dari atom radioaktif dari sampel. Waktu paruh karbon-14, yang menjadi karbon-12, sangat panjang dan digunakan untuk menentukan umur sisa-sisa organik purba seperti fosil. Sebaliknya, waktu paruh isotop lain seperti oksigen-15 hanya beberapa detik (122 detik, tepatnya).
Dalam kasus hidrogen, isotop alami Mereka memiliki karakteristik dan sifat yang sangat berbeda, itulah sebabnya mereka memiliki tiga nama berbeda: hidrogen konvensional atau protium 1H, deuterium 2H (D) dan tritium 3H(T). Hidrogen memiliki yang lain isotop buatan (hidrogen-4, hidrogen-5, dll.).

Gambar: Berbagi slide
Bagaimana cara menghitung nomor massa? - Formula.
Untuk menghitung nomor massa atom atau ion kita harus menambahkan nomor atom (jumlah proton dalam atom atau ion, biasanya direpresentasikan sebagai "Z") dan jumlah elektron.
Nomor massa (A) = nomor atom (Z) + jumlah neutron (N)
UNTUK = Z + N
Nomor atom dapat ditemukan dalam tabel periodik unsur, di kiri atas setiap unsur. Juga, nomor massa atau massa atom akan muncul di bawah elemen dalam tabel periodik.
Oleh karena itu, dengan mengurangkan nomor atom dari nomor massa, kita juga dapat mengetahui jumlah proton.
Jumlah neutron (N) = nomor massa (A) - nomor atom (Z)
tidak = A - Z
Misalnya, jika Anda melihat tabel periodik, Anda akan melihat bahwa besi memiliki nomor massa 55,84, yaitu, A = 56 dibulatkan ke satuan terdekat; Nomor atomnya (Z) adalah 26, jadi jumlah neutronnya adalah:
N = A - Z = 56-26 = 30
Jika Anda ingin membaca lebih banyak artikel serupa dengan Bagaimana cara mendapatkan nomor massa?, kami sarankan Anda memasukkan kategori kami atom.