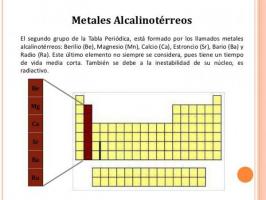
PERIODINĖS LENTELĖS evoliucija: nuo jos sukūrimo iki šiandienos
Periodinė lentelė yra viena iš žymiausios piktogramos mokslo. Nors 2019-ieji buvo 150-osios sukūrimo metinės, tai anaiptol nėra baigtas dokumentas. Šioje Dėstytojo pamokoje pamatysime, kas yra periodinės lentelės raida nuo jos sukūrimo iki šių dienų ir kokie pažangos pažinant atomus ir jų savybes leido tai padaryti.
Indeksas
- Kas yra periodinė lentelė?
- Pirmoji periodinė lentelė: kilmė
- Periodinės lentelės ir evoliucijos istorija
Kas yra periodinė lentelė?
The Periodinė elementų lentelė Periodinė elementų sistema yra mokslinis dokumentas, sutelkiantis daugiau informacijos mažiau erdvėje ir sudarantis vieną iš galingiausių mokslo ikonų. Jame yra nemaža dalis žinių apie chemiją. Panašaus dokumento nėra jokioje kitoje mokslo disciplinoje.
Periodinė elementų lentelė yra a cheminių elementų klasifikavimo sistema Tai prasidėjo daugiau nei prieš 200 metų. Ši klasifikavimo sistema laikui bėgant augo ir keitėsi, nes mokslas progresavo ir atrado naujų.
cheminiai elementai. Tačiau įvairios modifikacijos buvo įtrauktos, nepažeidžiant pagrindinės jo struktūros.Periodinė lentelė taip pavadinta todėl išreiškia grafiškai kaip jie kartojasi reguliariais intervalais cheminės savybės. Tai yra dviejų matmenų reprezentacijos tipas arba, šiuolaikiškiau vaizduojant, trimatis.
Viduje konors klasikinė periodinė lentelė (dvimatis) cheminiai elementai yra išdėstyti grupės ar šeimos ir yra pateikti dabartinėje periodinėje lentelėje vertikaliuose stulpeliuose. Išdėstytas šių grupių išdėstymas stulpeliuose sukelia eilučių seriją, vadinamą periodais, kur elementai yra išdėstyti pagal jų atominį svorį. Periodinę lentelę sudaro septyni periodai, kurie skiriasi ilgiu.

Pirmoji periodinė lentelė: kilmė.
Prieš Mendelejevą kiti mokslininkai sukūrė cheminių elementų klasifikavimo sistemas. Tačiau, skirtingai nuo periodinės elementų lentelės, jie buvo tik žinomų elementų sąrašai; o periodinė lentelė turi ypatumą, kad tai yra klasifikavimo sistema dviem aspektais (eilutėmis ir stulpeliai) arba trys dimensijos, moderniausiose versijose, kur cheminiai elementai yra išdėstyti vienas po kito sluoksniai.
Dėl šios priežasties istorikai pateikia šiuolaikinės periodinės lentelės gimimą 1869 m. Vasario 17 d., kada Dimitrijus Ivanovičius Mendelejevas baigti pirmoji periodinė lentelė iš daugelio, kuriuos jis sukūrė. Šią lentelę sudarė 63 elementai, išdėstyti šeimose, ir palikta tuščių vietų elementams, kurių dar nėra atrado, bet iš kurio jis išskaičiavo jų atominį svorį (kaip Gallio, Germanio ir Scandium)
Pagrindiniai periodinės lentelės radimo duomenys buvo ankstesnės informacijos apie atominė masė kiekvieno elemento.
Kas yra atominė masė ir atominis skaičius?
Šis skaičius reprezentavo atomo svorį ir tai buvo vienintelė pamatuojama vertė atomai. Bet tai nebuvo tiesioginiai matavimai (nėra matavimo prietaisų, leidžiančių pasverti izoliuotus atomus), bet tai buvo sistema, kuri standartas, pagal kurį vandenilio atomui buvo suteikta savavališkai reikšmė 1, o pagal tai buvo apskaičiuota likusių elementų atominės masės vertė. Raštas.
Pirmieji atominis skaičius elementų atliko anglų chemikas Jonas Daltonasir sukėlė didžiulę mokslinę diskusiją XIX a. pirmojoje pusėje. Tačiau XIX amžiaus antroje pusėje jau buvo pasiektas puikus sutarimas dėl elementų atominių masių skaičiavimo sistemos. Atominis svoris nuo Mendelejevo tapo svarbiausiu kriterijumi teisingam periodinės lentelės elementų išdėstymui.
Kai Mendelejevas užsakė žinomus elementus pagal juos didėjantis atominis svoris, pastebėjo pasikartojančių savybių atsiradimą, leidusį elementus sugrupuoti į panašių vienas į kitą grupes ar elementų šeimas. Tačiau kai kuriais atvejais elementų išdėstymas pagal jų atominę masę neatsakė į pastebėtų elementų panašumus ir pasikeitė Mendelejevas 17 elementų padėtis periodinės lentelės išdėstyme, nepaisant jų atominės masės, kad būtų galima juos sugrupuoti su tais elementais, su kuriais jie pateikė analogijas.
Šie pakeitimai leido suprasti, kad kai kurie priimti atominiai svoriai nebuvo teisingi ir buvo perskaičiuoti. Nepaisant atominių svorių pataisymų, vis tiek buvo elementų, kuriuos reikėjo pastatyti į kitas nei jų atomo svoriais nurodytas pozicijas.

Vaizdas: BBC.com
Periodinės lentelės ir evoliucijos istorija.
Nepaisant neabejotino Mendelejevo indėlio, periodinė elementų lentelė nėra vieno tyrėjo darbo rezultatas. Be Mendelejevo, XIX a. Antroje pusėje ir per visą XX a. Daugelį Chemikai toliau tyrinėjo geriausią būdą organizuoti informaciją apie cheminius elementus žinomas. Dar labiau atsižvelgiant į tai, kad per šį laiką atradimas naujų cheminių elementų ar paprastų medžiagų, dėka spektrometrijos (kuri tiria atomų ir elektromagnetinės spinduliuotės sąveiką).
The elementų klasifikacija periodinėje lentelėje iš pradžių buvo remiamasi pradiniais skaičiavimais atominiai svoriai elementų ir atskleidė analogijas, kurios leido elementus sugrupuoti į analogiškas šeimas. Nepaisant to, šių periodinių savybių atsiradimo priežasties nebuvo galima paaiškinti. Visą XX a., Atradus elektroninę struktūrą, buvo suprasta šio periodiškumo elementų savybėse priežastis.
Atomo skaičius kaip rūšiavimo tvarka
20 amžiaus pradžioje Gloveris ir Rutherfordas, pastebėjo, kad įelektrintos branduolio dalelės sudarė apie pusę atominės masės. Ši vertė atitinka atominis skaičius kuris apibrėžiamas kaip protonų skaičius atomo branduolyje ir kuris sutampa su elektronų skaičiumi neutraliame atome. Ši nauja vertė pateisino tam tikrų elementų padėties pokyčius, kurie buvo atlikti iki tol. Pavyzdžiui, padėties tarp Tellurium ir jodo pasikeitimas.
1913 m. Henry Moseley rentgeno spektrometrija patvirtino lentelės išdėstymą pagal atominio skaičiaus funkciją. Rikiavimas pagal atominį skaičių galioja ir šiandien.
Tuo pačiu metu 20-ajame amžiuje kvantinės mechanikos ir vystymosi metodų dėka toliau buvo atrasti nauji cheminiai elementai. atomų bombardavimas dalelėmis, nuo antrosios amžiaus pusės. Naudojant šią naują techniką buvo galima sukurti dirbtiniai elementai kurių nėra gamtoje.
Nors pažanga padaryta teisingai išdėstant periodinės lentelės elementus, vis tiek pasikartojančio tam tikrų savybių (savybių) atsiradimo priežastis periodiškai). Programos plėtra Kvantinė mechanika (fizikos šaka, tirianti šviesos ir atomų elgesį mikroskopiniu mastu) nuo 1920 m. buvo lemiamas paaiškinant šių savybių priežastis.
Elektroninė konfigūracija kaip periodinių savybių paaiškinimas
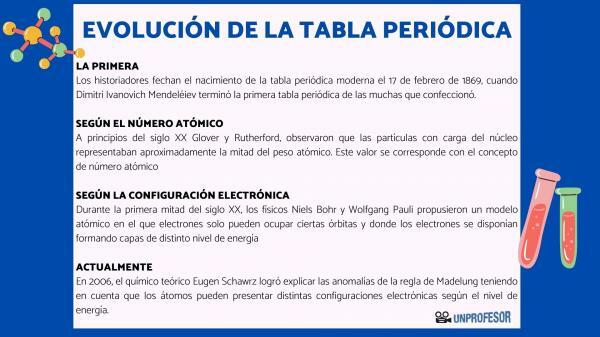
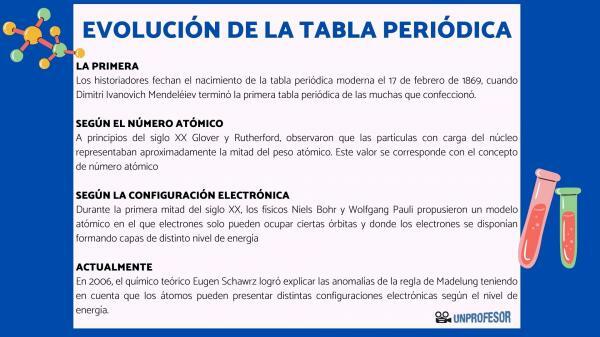
Pirmojoje 20 amžiaus pusėje fizikai Nielsas Bohras Y Wolfgangas Pauli jie pasiūlė atominį modelį, kuriame elektronai gali užimti tik tam tikras orbitas ir kur elektronai išsidėstę, sudarydami skirtingų energijos lygių sluoksnius. Elektronų pasiskirstymo orbitalėse skirtinguose apvalkaluose ar energijos lygiuose būdas yra žinomas kaip elektroninė konfigūracija.
Elektronų išsidėstymo elektronų konfigūracijose atradimas buvo pagrindinis norint suprasti savybių periodiškumą. periodiškas, nes buvo pastebėta, kad šios savybės buvo glaudžiai susijusios su atomų tolimiausia elektronine konfigūracija Valensija).
Tvarką, kuria elektronai užpildo atomines orbitales, 1930 m. Nustatė fizikas Erwinas Madelungas, kuris nustatė skaitinę užpildymo tvarkos taisyklę. Ši taisyklė yra žinoma kaip Madelungo valdžia ir tai yra empirinė taisyklė, kurios nebuvo galima paaiškinti kvantine mechanika.
Pirmų trijų periodinės lentelės eilučių pildymo seka yra paprasta, tačiau ketvirta eilutė, kurioje yra perėjimo elementai, užpildymo tvarka atliekama eilė pakeitimai. Iš viso yra 20 nenormalių elementų, kurie nesilaiko šios taisyklės.
Lentelės evoliucija tęsiasi ir šiandien
2006 m. - teorinis chemikas Eugenas Schawrzas Jam pavyko paaiškinti Madelungo taisyklės anomalijas, atsižvelgiant į tai, kad atomai gali turėti skirtingas elektronines konfigūracijas, priklausomai nuo energijos lygio. Skaičiuojant vidurkius, daugumos elementų elektronų konfigūracijos atitinka Madelungo taisyklę.
Periodinė lentelė išlieka diskusijų dalykas XXI amžiuje, nors jų išdėstymas ar elektroninė konfigūracija elementus, vis dar galioja paaiškinant šią tvarką ir elektroninėse konfigūracijose pastebėtas anomalijas naudojant a teorija.
Jei norite perskaityti daugiau panašių į Periodinės lentelės raida - santrauka, rekomenduojame įvesti mūsų kategoriją Atomas.
Bibliografija
Įvairūs autoriai. (2019)Specialus: periodinė lentelė. Tyrimai ir mokslas. Barselona: Scientific Press S.A.