Atomo dalys ir jų charakteristikos
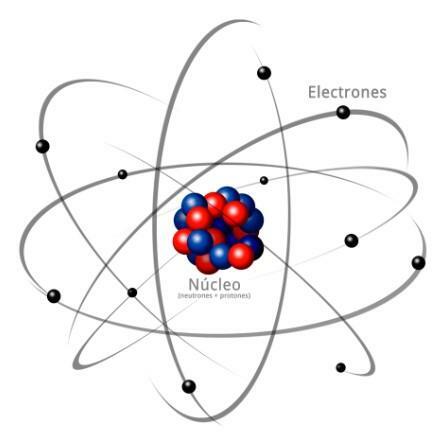
Vaizdas: Answers.tips
Atomai yra pagrindiniai elementai formos materija, būdamas visose materijos būsenose. Jie yra labai maži elementai, kurių neįmanoma pamatyti žmogaus akimis, tačiau jie tikrai svarbūs mūsų visatai. Norėdami geriau suprasti, kaip yra atomai ir kaip jie veikia, šioje mokytojo pamokoje mes kalbėsime atomo dalys ir jų charakteristikos.
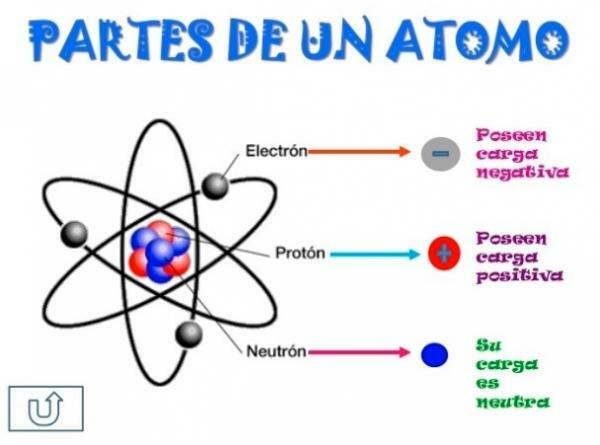
Visus atomus sudaro a šerdis ir pluta. Branduolys, kaip rodo jo pavadinimas, yra centrinė atomo dalis, kurioje dalelės, kurių krūvis yra teigiamas ir kurios vadinamos protonaiir dalelės, kurių krūvis yra neutralus, tai yra, jos neturi elektrinio krūvio, gaudamos pavadinimą neutronai. Abiejų dalelių, tiek protonų, tiek neutronų, masė yra panaši. Visi to paties cheminio elemento atomai turi vienodą protonų skaičių, šis skaičius vadinamas atominiu skaičiumi, o jam žymėti naudojama raidė Z.
Kita vertus, yra Žievė Kas yra išorinė atomo dalis. Žievėje randame elektronai, kurios yra neigiamai įkrautos dalelės. Elektronai dideliu greičiu sukasi aplink branduolį skirtingais lygiais, dalelės yra daug mažesnės nei tos, kurios yra branduolyje.
Būdami neutralūs neutronai, teigiami protonai ir neigiami elektronai, atomas turi neutralų elektros krūvį, nes jie turi tą patį protonų skaičių kaip ir elektronai. Nors yra atvejų, kai elektronų yra mažiau ar daugiau nei protonų, dėl to atsiranda krūvis atomas yra neigiamas arba teigiamas, šiuo atveju jis gauna pavadinimą jonas, anijonas, jei jis yra neigiamas, arba katijonas, jei jis yra teigiamas.
Vaizdas: Brainly
Norėdami pratęsti šią pamoką apie atomo dalis ir jų charakteristikas, turime kalbėti apie evoliuciją, kurią nuo to laiko turėjo atomo dalys. atominis modelis laikui bėgant keitėsi mokslininkų tyrimų dėka. Reikia atsižvelgti į tai, kad keli modeliai, kuriuos mes paaiškinsime, yra pasenę ir nėra naudojami šiuo metu, tačiau jie yra būtini norint suprasti mokslo bendruomenės raidą šia tema.
Istorinei atominio modelio evoliucijai būdinga sekant mokslininkus:
- „Dalton“ modelis: Pirmasis atominis modelis buvo Johno Daltono darbas 1803 m. Tai labai primityvus modelis, kuriam trūksta daugybės elementų, tokių kaip elektronų ir protonų buvimas.
- „Thomson“ modelis: Johnui Thomsonui pavyko sukurti išsamesnį nei Daltono atominį modelį, pridedant keletą pagrindinių elementų. Tomsonas atrado elektronų egzistavimą ir teigiamus bei neigiamus krūvius.
- „Nagaoka“ modelis: Japonų fizikas Nagaoka nesutiko su Thomsono modeliu, jis manė, kad atomas turi turėti didelį teigiamai įkrautą branduolį, ant kurio sukasi neigiamai įkrauti elektronai. Jo teorija vadinama Saturno, nes jis palygino elektronus su Saturno žiedais. Daug kartų šis modelis nėra įvardijamas, tačiau būtina suprasti, koks didelis žingsnis žengtas šiuo metu.
- „Rutherford“ modelis: Rutherfordo modelis buvo pagrįstas teigiamai įkrauto branduolio, kuriame sukosi neigiamai įkrauti elektronai, egzistavimu. Šis modelis yra labai panašus į Nagaoka, būdami labai artimų metų, nors japonų modelis yra ankstesnis.
- Bohr modelis: Bohras manė, kad elektronai turėtų būti toli nuo sluoksniuoto branduolio, o šių orbitinių dalelių skaičius turėtų būti lygus atominiam skaičiui. Jo modelis taip pat supranta, kad kiekvienoje apvalkale elektronų skaičius skiriasi, o pirmajame apvalkale yra mažiau elektronų nei paskutiniame.
- „Schrodinger“ modelis: Schrodingeris sulaužė įsitikinimą, kad elektronai yra mažytės dalelės, kurios sukasi aplink branduolį. Austrijos mokslininkas teigė, kad elektronai juda naudojant bangų funkciją, ty orbitos forma.
- „Dirac“ modelis: Diracas modifikavo Schrodingerio savo modelio idėjas, naudodamas „Dirac lygtį“, kad teisingiau matytųsi apie orbitos elektronų formą.