Evolutie van de PERIODIEKE TABEL: van de oprichting tot vandaag
Het periodiek systeem is een van de meest iconische iconen van de wetenschap. Hoewel 2019 de 150e verjaardag was van zijn oprichting, is het zeker geen voltooid document. In deze les van een LERAAR zullen we zien wat de evolutie van het periodiek systeem vanaf de creatie tot op de dag van vandaag en welke vorderingen in de kennis van atomen en hun eigenschappen dit mogelijk hebben gemaakt.
Inhoudsopgave
- Wat is het periodiek systeem?
- Eerste periodiek systeem: de oorsprong
- Geschiedenis van het periodiek systeem en evolutie
Wat is het periodiek systeem?
De periodiek systeem Het periodiek systeem van elementen is het wetenschappelijke document dat meer informatie in minder ruimte concentreert en een van de krachtigste iconen van de wetenschap vormt. Het bevat een groot deel van de kennis die we hebben over chemie. Er is geen vergelijkbaar document in een andere wetenschappelijke discipline.
Het periodiek systeem der elementen is a
classificatiesysteem van chemische elementen Het begon meer dan 200 jaar geleden. Dit classificatiesysteem is in de loop van de tijd gegroeid en veranderd, naarmate de wetenschap vorderde en nieuwe werden ontdekt. chemische elementen. De verschillende modificaties zijn echter aangebracht waarbij de fundamentele structuur intact is gebleven.Het periodiek systeem is zo genoemd omdat: drukt grafisch uit de manier waarop ze met regelmatige tussenpozen herhalen zeker chemische eigenschappen. Het is een soort tweedimensionale weergave of, in zijn modernere voorstellingen, driedimensionaal.
In de klassiek periodiek systeem (tweedimensionaal) de chemische elementen zijn gerangschikt in groepen of families en worden in het huidige periodiek systeem weergegeven in verticale kolommen. De geordende rangschikking van deze groepen in kolommen geeft aanleiding tot een reeks rijen, die perioden worden genoemd, waarin de elementen zijn gerangschikt op basis van hun atoomgewicht. Het periodiek systeem bestaat uit zeven perioden die in lengte variëren.

Eerste periodiek systeem: de oorsprong.
Vóór Mendelejev hadden andere wetenschappers classificatiesystemen voor chemische elementen ontwikkeld. Maar, in tegenstelling tot het periodiek systeem der elementen, waren ze: louter lijsten van de bekende elementen; terwijl het periodiek systeem de bijzonderheid heeft dat het een classificatiesysteem is in twee dimensies (rijen en kolommen) of drie dimensies, in de modernste versies, waar de chemische elementen opeenvolgend zijn gerangschikt arranged lagen.
Om deze reden dateren historici de geboorte van het moderne periodiek systeem 17 februari 1869, wanneer Dimitri Ivanovitsj Mendelejev beëindig de eerste periodiek systeem van de vele die hij maakte. Deze tabel bestond uit 63 elementen gerangschikt in families en liet lege ruimtes over voor elementen die nog niet waren ontdekt, maar waaruit hij hun atoomgewicht had afgeleid (zoals in het geval van Gallium, Germanium en Scandium)
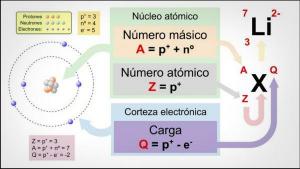
De belangrijkste gegevens voor de ontdekking van het periodiek systeem waren de voorkennis van de atoomgewicht van elk element.
Wat is atoomgewicht en atoomnummer?
Dit nummer vertegenwoordigde het gewicht van het atoom en het was de enige meetbare waarde van de atomen. Maar het waren in ieder geval geen directe metingen (er zijn geen meettoestellen die het mogelijk maken om geïsoleerde atomen te wegen) maar het was eerder een systeem dat een standaard waarin een willekeurige waarde van 1 aan het waterstofatoom werd gegeven en de waarde van het atoomgewicht van de overige elementen werd berekend in relatie tot deze Patroon.
De eerste berekeningen van de atoomnummer van de elementen werden uitgevoerd door de Engelse chemicus John Dalton, en zorgde in de eerste helft van de 19e eeuw voor een groot wetenschappelijk debat. In de tweede helft van de 19e eeuw was er echter al een opmerkelijke consensus over het systeem voor het berekenen van de atoomgewichten van de elementen. Het atoomgewicht werd vanaf Mendelejev een belangrijk criterium voor de juiste volgorde van de elementen in het periodiek systeem.
Toen Mendelejev de bekende elementen bestelde volgens hun toenemend atoomgewicht, zag het verschijnen van terugkerende eigenschappen waardoor de elementen konden worden gegroepeerd in groepen of families van elementen die op elkaar leken. In sommige gevallen reageerde de volgorde van de elementen op basis van hun atoomgewicht echter niet op de overeenkomsten tussen de waargenomen elementen en veranderde Mendelejev de positie van 17 elementen in de rangschikking van het periodiek systeem ondanks hun atoomgewicht, om ze te kunnen groeperen met die elementen waarmee ze analogieën presenteerden.
Deze veranderingen toonden aan dat sommige van de geaccepteerde atoomgewichten niet correct waren en opnieuw werden berekend. Ondanks de correcties in de atoomgewichten waren er toch elementen die op andere posities moesten worden geplaatst dan aangegeven door hun atoomgewicht.

Afbeelding: BBC.com
Geschiedenis van het periodiek systeem en evolutie.
Ondanks de onmiskenbare bijdrage van Mendelejev, is het periodiek systeem der elementen niet het resultaat van het werk van een enkele onderzoeker. Naast Mendelejev hebben in de tweede helft van de negentiende eeuw en gedurende de twintigste eeuw vele Chemici gingen door met het onderzoeken van de beste manier om informatie over chemische elementen te ordenen bekend. Zeker gezien het feit dat gedurende deze tijd de ontdekking van nieuwe chemische elementen of eenvoudige stoffen, dankzij spectrometrie (die de interacties tussen atomen en elektromagnetische straling bestudeert).
De classificatie van elementen in het periodiek systeem was aanvankelijk gebaseerd op de beginnende berekeningen van de atoomgewichten van de elementen en onthulde analogieën waardoor de elementen in analoge families konden worden gegroepeerd. Toch kon de reden voor het verschijnen van deze periodieke eigenschappen niet worden verklaard. Het was gedurende de 20e eeuw, met de ontdekking van elektronische structuur, toen de reden voor deze periodiciteit in de eigenschappen van de elementen werd begrepen.
Het atoomnummer als sorteervolgorde
Aan het begin van de 20e eeuw Glover en Rutherford, merkte op dat de geladen deeltjes in de kern ongeveer de helft van het atoomgewicht uitmaakten. Deze waarde komt overeen met het concept van atoomnummer die wordt gedefinieerd als het aantal protonen in de atoomkern en dat samenvalt met het aantal elektronen in een neutraal atoom. Deze nieuwe waarde rechtvaardigde de tot dan toe doorgevoerde positiewijzigingen van bepaalde elementen. Bijvoorbeeld de verandering van positie tussen Tellurium en Jodium.
1913, Henry Moseley bevestigde de volgorde van de tabel als een functie van het atoomnummer door röntgenspectrometrie. De volgorde volgens het atoomnummer is nog steeds van kracht.
Tegelijkertijd werden er in de 20e eeuw steeds nieuwe chemische elementen ontdekt dankzij de kwantummechanica en de ontwikkeling van de techniek van bombardement van atomen door deeltjes, uit de tweede helft van de eeuw. Met deze nieuwe techniek was het mogelijk om te creëren kunstmatige elementen die niet in de natuur voorkomen.
Hoewel er vooruitgang was geboekt in de juiste rangschikking van de elementen binnen het periodiek systeem, is nog steeds de reden voor het herhaaldelijk voorkomen van bepaalde eigenschappen (de eigenschappen periodiek). De ontwikkeling van de kwantummechanica (tak van de natuurkunde die het gedrag van licht en atomen op microscopische schaal bestudeert) uit 1920 was doorslaggevend om de reden voor deze eigenschappen te verklaren.
Elektronische configuratie als uitleg van periodieke eigenschappen
In de eerste helft van de 20e eeuw hebben natuurkundigen Niels Bohr Y Wolfgang Pauli ze stelden een atomair model voor waarin elektronen alleen bepaalde banen kunnen innemen en waarbij de elektronen zijn gerangschikt en lagen met verschillende energieniveaus vormen. De manier waarop de elektronen zijn verdeeld in de orbitalen in de verschillende schillen of energieniveaus staat bekend als elektronische configuratie.
De ontdekking van de rangschikking van elektronen in elektronenconfiguraties was van fundamenteel belang voor het begrip van de periodiciteit van de eigenschappen periodiek, aangezien werd waargenomen dat deze eigenschappen nauw verband hielden met de buitenste elektronische configuratie van de atomen (laag van Valencia).
De volgorde waarin elektronen atomaire orbitalen vullen, werd in 1930 vastgesteld door natuurkundige Erwin Madelung die een numerieke regel vaststelde voor de volgorde van vullen. Deze regel staat bekend als: Madelung regel en het is een empirische regel die niet kon worden verklaard door middel van kwantummechanica.
De vulvolgorde is eenvoudig voor de eerste drie rijen van het periodiek systeem, maar in de vierde rij, waar de overgangselementen zich bevinden, ondergaat de volgorde van vullen een reeks van wijzigingen. Er zijn in totaal 20 afwijkende items die deze regel niet volgen.
Evolutie van de tafel gaat vandaag verder
In 2006, de theoretische chemicus Eugen Schawrz Hij slaagde erin de anomalieën van de regel van Madelung uit te leggen, rekening houdend met het feit dat atomen verschillende elektronische configuraties kunnen hebben, afhankelijk van het energieniveau. Bij het berekenen van de gemiddelden voldoen de elektronenconfiguraties van de meeste elementen aan de regel van Madelung.
Het periodiek systeem blijft een kwestie van debat in de 21e eeuw, hoewel de opstelling of elektronische configuratie van de elementen, is het nog steeds geldig om deze volgorde en de anomalieën waargenomen in de elektronische configuraties te verklaren door middel van a theorie.
Als u meer artikelen wilt lezen die vergelijkbaar zijn met Evolutie van het periodiek systeem - samenvatting, raden we u aan om onze categorie in te voeren van: het atoom.
Bibliografie
Diverse auteurs. (2019)Speciaal: het periodiek systeem. Onderzoek en wetenschap. Barcelona: Scientific Press S.A.