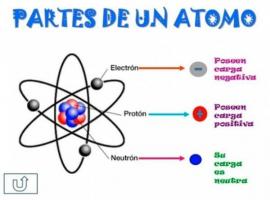
Atoomstructuur en kenmerken

Afbeelding: SlidePlayer
Atomen maken deel uit van onze wereld. Alle materie is gemaakt van atomen, dus het is belangrijk om beter te begrijpen waaruit ze bestaan en wat hun functies zijn. In deze les van een LERAAR gaan we je vertellen wat de structuur van een atoom en kenmerken. Als je meer wilt weten over de deeltjes waaruit alle materie bestaat, blijf dan dit artikel lezen.
Inhoudsopgave
- Wat zijn atomen?
- Structuur van het atoom
- Belangrijkste kenmerken van het atoom
- Wat zijn isotopen?
- Hoe komen de atomen in de natuur voor?
Wat zijn atomen?
De atoom het is de kleinste eenheid waarin materie kan worden verdeeld zonder zijn chemische eigenschappen te verliezen, dat wil zeggen zijn eigenschappen als chemisch element. Het atoom is de oorsprong van alles wat je kunt zien of aanraken, van de sterren tot je ontbijt vanmorgen.
Als we het verlies van zijn chemische eigenschappen buiten beschouwing laten, kunnen we zeggen dat het atoom bestaat uit verschillende deeltjes, subatomaire deeltjes genaamd. Er zijn drie soorten subatomaire deeltjes:
-protonen, neutronen en elektronen- met verschillende kenmerken.Deze deeltjes zijn in verschillende aantallen gegroepeerd om de chemische elementen te vormen (zuurstof, koolstof, enz.), maar ze zullen altijd volgens een vaste structuur worden verdeeld.

Afbeelding: Google Sites
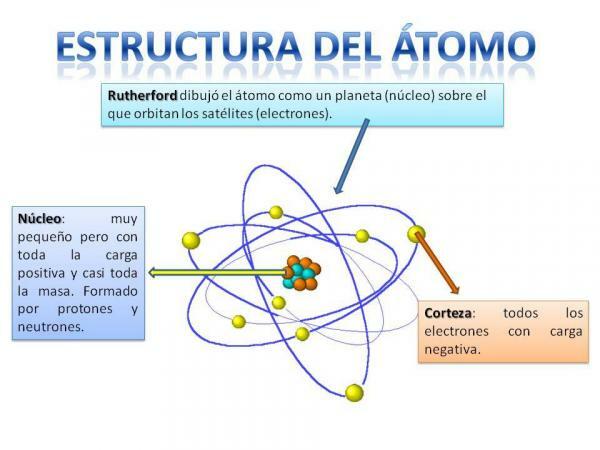
Structuur van het atoom.
De structuur van het atoom ligt vast, dat wil zeggen, we kunnen verschillende soorten atomen hebben (het waterstofatoom, het zuurstofatoom, enz.), maar hun subatomaire deeltjes zijn altijd op dezelfde manier georganiseerd als een planetair systeem.
Je zult je zeker herinneren hoe het zonnestelsel is georganiseerd: de zon staat in het centrum en eromheen hiervandaan draaien de planeten en beschrijven ze verschillende banen, sommige dichterbij en andere verder weg van de Zon. In het geval van atomen, in het centrum is de kern, met een vorm die lijkt op een braam en is samengesteld uit de neutronen en de protonen.
Rond de kern is de Cortex wat is het gebied waardoor de elektronen. Vroeger dacht men dat elektronen bepaalde banen beschreven, vergelijkbaar met planeten, maar nu is dat zo weet dat deze banen niet zo goed gedefinieerd zijn en meer lijken op gebieden waarin we ons eerder zullen bevinden elektronen.
Afbeelding: REA - Plan Ceibal
Belangrijkste kenmerken van het atoom.
Om door te gaan met deze les over de structuur van het atoom en de kenmerken, is het belangrijk om te focussen op de elementen die ervoor zorgen dat een atoom als zodanig wordt beschouwd.
En daarvoor moeten we deze vraag beantwoorden: waarom besluiten alle atomen om zichzelf op die bepaalde manier te ordenen? Het antwoord is simpel: het komt door: elektrische aantrekkingskrachten. De kern van het atoom bestaat uit neutronen, die geen elektrische lading hebben, en protonen, die een positieve elektrische lading hebben. en de elektronen hebben een negatieve elektrische lading, dus er is een vergelijkbare aantrekkingskracht tussen de kern en de elektronen geproduceerd tussen de twee polen van een magneet, maar is niet sterk genoeg voor elektronen om naar de te "vallen" kern.
Dit wordt beter begrepen als we rekening houden met de kerngrootte:: als het atoom bijvoorbeeld de afmeting van een voetbalstadion had, zou de kern de afmeting hebben van de bal in het midden van het veld Hoeveel aantrekkingskracht zou de voetbal moeten hebben om de tribunes van het stadion erop te laten vallen!
De functie van neutronen
Nu vraag je je misschien af, en welke rol spelen neutronen? Ondanks dat ze geen elektrische lading hebben, spelen neutronen een grote rol binnen het atoom: ze dragen 99% van de massa bij. Als het je helpt herinneren, kunnen we zeggen dat een atoom is als een bende van drie vrienden: de zware neutron, het positieve proton en het negatieve elektron, dat rond en rond het neutron gaat en elektron.
De beweging van elektronen
Op dit punt wil ik dat we teruggaan naar iets dat we in de inktpot hadden achtergelaten: de banen die de elektronen rond de kern beschrijven. Dat hadden we gezegd elektronen draaien om de kern zoals de planeten rond de zon doen, sommige dichterbij dan andere, waarom doen ze het? Elektronen roteren in de ene of andere schil volgens de energie die ze hebben om van de kern weg te bewegen, dat wil zeggen dat de elektronen die zich dichter bij de kern bevinden niet de voldoende kracht om van de kern weg te bewegen, terwijl die in de buitenste schillen (orbitalen) van de korst meer energie hebben en in staat zijn geweest om verder van de kern af te bewegen. kern. Verder is er in elk van de orbitalen een maximale capaciteit van 8 elektronen (octetregel).
De deeltjes van een atoom
We gaan terug naar een andere benadering die we eerder hebben gedaan maar niet hebben uitgelegd: atomen zijn opgebouwd uit neutronen, protonen en elektronen, die altijd dezelfde structuur van kern en korst volgen, maar ze doen dat in verschillende aantallen om de verschillende chemische elementen te vormen. Hoe kunnen we zoveel elementen krijgen die slechts 3 soorten deeltjes combineren? De chemische elementen, die je ooit in het periodiek systeem hebt gezien, worden gekenmerkt door een bepaald atoomnummer.
De atoomnummer (Z) Het vertelt ons het aantal protonen in de kern van dit type atomen, dat onder normale omstandigheden gelijk is aan het aantal elektronen. Zo zullen bijvoorbeeld alle atomen met 6 protonen (Z = 6) koolstofatomen zijn, en ze zullen dezelfde chemische eigenschappen hebben; de atomen met 5 protonen (Z = 5) zullen booratomen zijn, met dezelfde chemische eigenschappen als elkaar en verschillend van die van koolstofatomen. Je hoeft atoomnummer niet te verwarren met atoomgewicht of massagetal (A), wat de som is van het gewicht van neutronen en protonen (het gewicht van de elektronen is verwaarloosbaar ten opzichte van het gewicht van de totale kern).

Afbeelding: SlidePlayer
Wat zijn isotopen?
In de natuur kunnen we verschillende "subtypes" van elementen vinden, de isotopen. Ik weet zeker dat je ooit hebt gehoord van koolstof 14, een radioactieve isotoop van koolstof die wordt gebruikt om onder andere de ouderdom van fossielen te bepalen. Isotopen zijn twee atomen met hetzelfde aantal protonen (zelfde atoomnummer), maar verschillend aantal neutronen (verschillende atoommassa). De isotopen van hetzelfde element worden meestal genoemd met de naam van het element, gevolgd door zijn atomaire massa.
In ons voorbeeld zijn beide isotopen koolstof, dus ze hebben een atoomnummer van 6 (Z = 6) maar koolstof 12 ("normale" koolstof) heeft een atoomgewicht van 12 versus het atoomgewicht van koolstof 14 14. De isotopen van hetzelfde element hebben zeer vergelijkbare chemische en fysische eigenschappen. In het geval van koolstof 14 is het, in tegenstelling tot koolstof 12, een radioactieve isotoop die aanwezig is in alle elementen die koolstof bevatten, inclusief levende wezens.
En hiermee eindigen we deze les over de structuur van het atoom en kenmerken. We hopen dat het u heeft geholpen.

Afbeelding: uw taken
Hoe komen de atomen in de natuur voor?
Atomen kunnen geïsoleerd worden gevonden, maar de normaalste zaak is om ze te vinden gecombineerd in groepen genaamd moleculen.
Moleculen kunnen bestaan uit atomen van hetzelfde element (zoals het zuurstofmolecuul, bestaande uit twee atomen van zuurstof) of door groepen met atomen van verschillende elementen (twee atomen waterstof en één zuurstof vormen het molecuul van Water). Deze groepen elementen worden moleculen genoemd, die op hun beurt met elkaar kunnen worden gecombineerd en vormen verschillende, steeds complexere groepen op basis van hun reactiviteit en hun chemische affiniteit voor bron van chemische verbindingen.
Als u meer artikelen wilt lezen die vergelijkbaar zijn met Structuur van het atoom en kenmerken, raden we u aan om onze categorie van het atoom.