Waar zijn ISOTOPEN voor?
Isotopen zijn atomen van hetzelfde element met hetzelfde aantal protonen in de kern, maar met een verschillend aantal neutronen. Dit verschil dat, a priori, het lijkt u misschien vrij onbeduidend, het maakt de isotopen van hetzelfde element hetzelfde of verschillend in veel kenmerken en eigenschappen, fysisch en chemisch. De mens heeft van al deze dingen kunnen profiteren in ons voordeel. De toepassingen van isotopen zijn gevarieerd en beïnvloeden zeer verschillende velden: ze helpen ons onze voedsel, om ziekten te diagnosticeren en te genezen of om de ouderdom te achterhalen van fossiele overblijfselen die miljoenen geleden zijn begraven van jaren. In deze les van een LERAAR zullen we zien waar zijn isotopen voor? en hoe ze ons helpen op tien verschillende gebieden van ons leven.
Inhoudsopgave
- Wat zijn isotopen?
- Isotopen en het verkrijgen van energie
- Isotopen in de geneeskunde
- Isotopen in kunst en archeologie
- Isotopen in voedsel en landbouw
- Andere toepassingen van isotopen
Wat zijn isotopen?
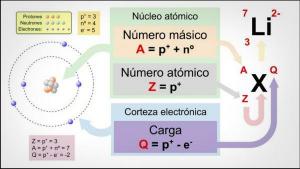
de atomen Ze bestaan, op een klassieke manier, uit drie soorten deeltjes: neutronen, protonen en elektronen. De neutronen en protonen vormen de kern, terwijl de elektronen rond de kern draaien en een "elektronenwolk" vormen.
De atomen van een chemisch element worden gekenmerkt door een bepaald aantal protonen. Het aantal protonen van een element in de chemie heet atoomnummer (Z). Atomen zijn elektrisch neutraal, dat wil zeggen, ze hebben hetzelfde totale aantal positieve deeltjes (protonen) als negatieve (elektronen). Een ander ding dat atomen kenmerkt, is hun massagetal (A) dat is de som van alle protonen en neutronen waaruit de atoomkern bestaat en die hem het grootste deel van zijn gewicht of massa geven. Je kunt er meer over leren in deze andere les van een LERAAR op Hoe het massagetal te krijgen?
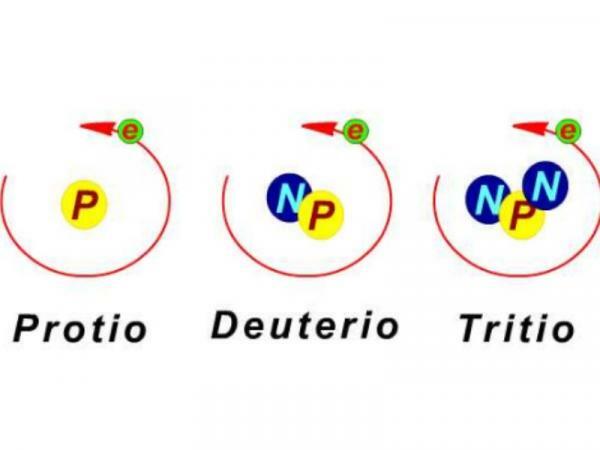
Echter, twee atomen van hetzelfde scheikundige element (met hetzelfde atoomnummer) kunnen een verschillend aantal neutronen in hun kern hebben, en dus een ander atoomgewicht. Deze twee atomen, met hetzelfde atoomnummer maar verschillend atoomgewicht, worden isotopen genoemd. isotopen van hetzelfde chemische element kan kenmerken of eigenschappen hebben die ze zeer interessant en nuttig maken voor mensen. Als je meer wilt weten over het onderwerp kun je onze les bezoeken Kenmerken van isotopen.
Nu je weet wat ze zijn, als je je ooit hebt afgevraagd waar zijn isotopen voor?, blijf lezen!
Isotopen en het verkrijgen van energie.
Zoals je weet, is een van de belangrijkste energiebronnen op aarde: de kernenergie. De naam kernenergie komt van het feit dat energie letterlijk wordt verkregen uit de kern van atomen. Zoals we eerder zagen, bestaat de kern van atomen uit protonen en neutronen, die door een grote kracht met elkaar verbonden zijn. Deze energie kan door twee processen door de mens worden vrijgegeven en gebruikt: kernfusie (de combinatie van twee kernen, die samenkomen om een grotere en energiekere te vormen) en de kernsplijting (het uiteenvallen of scheiden van een kern in meerdere kleinere).
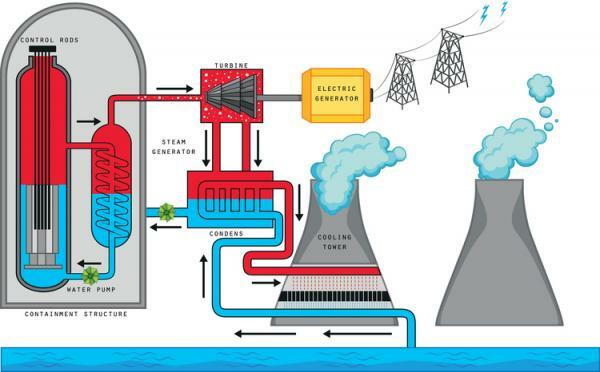
Momenteel wordt het grootste deel van de productie van kernenergie gedaan door kernsplijting. Hiervoor is de Plutoniumisotoop «Pu-239» en uraniumisotoop «U-235» omdat ze erg onstabiel en zwaar zijn en de deling van de kern een vrij hoge energieproductie met zich meebrengt. Wanneer de kernen van deze isotopen scheuren, wordt een grote hoeveelheid gegenereerd in de vorm van warmte; Deze warmte wordt in kernreactoren gebruikt om water te verwarmen, dat van vloeibare toestand naar gas gaat. Deze waterdamp wordt naar een turbine getransporteerd, die in beweging komt. Die turbine is op zijn beurt verbonden met een Elektrische generator wiens missie het is om de draaiende energie van de turbine om te zetten in elektrische energie, die kan worden opgeslagen, vervoerd en gebruikt in onze huizen.
Isotopen in de geneeskunde.
Een van de gebieden waarop de toepassing van isotopen het grootst is, is de geneeskunde. We kunnen tijdens de ziekte twee fasen onderscheiden waarin isotopen worden gebruikt: de diagnose en behandeling van de ziekte.
Voor de diagnose van ziekten en pathologieën, technieken zoals: röntgenstralen of scintigrafie; de scant zijn gebaseerd op een detectiemethode radiofarmaca, die niets meer zijn dan mengsels van stoffen waartussen zich kleine hoeveelheden van een radio-isotoop bevinden. Ze kunnen ook worden gebruikt om kleine hoeveelheden enzymen of eiwitten te bepalen die in sommige biologische processen worden gegenereerd.
Isotopen kunnen worden gebruikt om ziekten te behandelen. Isotopen worden gebruikt tijdens bestralingstherapiebehandelingen om cellen te vernietigen die kwaadaardige weefsels en tumoren vormen; In dit proces bereikt de ioniserende straling van medische apparatuur de tumorcellen en tast hun DNA aan, waardoor er zoveel breuken en mutaties ontstaan dat ze de dood veroorzaken. Bovendien kunnen isotopen, alvorens radiotherapiebehandelingen toe te passen, artsen helpen de kenmerken van tumorcellen, hun locatie, enz. te bestuderen. en op deze manier een actieplan opstellen om de dosis, frequentie en aantal bestralingssessies die nodig zijn voor aanvang van de behandeling aan te passen.
Een andere toepassing van isotopen in de geneeskunde is de toepassing van radio-isotopen voor de sterilisatie van materiaal, apparatuur en faciliteiten zoals operatiekamers. Er zijn verschillende soorten stralingssterilisatie, afhankelijk van het element dat we gebruiken, hoewel de meest gebruikte ultraviolette (UV) straling is.
Isotopen in kunst en archeologie.
Als je je ooit hebt afgevraagd waar isotopen voor zijn in de wereld van kunst en archeologie, ben je misschien een van hun toepassingen tegengekomen: datering van werken. De isotopen en de vergelijking van de halfwaardetijd hiervan maken het mogelijk om de leeftijd van monsters te dateren archeologische vindplaatsen van opgravingen maar ook van kunstwerken zoals schilderijen, muurschilderingen of zelfs sculpturen. Een andere van de meest relevante toepassingen in de kunst is de identificatie van vervalsingen of wijzigingen van werken: dankzij isotopenanalyse is het mogelijk om niet alleen de datum te weten waarop een werk is gemaakt (en mogelijke kopieën op te sporen), maar ook om te weten welke materialen gebruikt om het te maken (en vergelijk ze met die gebruikt door de auteur van het veronderstelde werk), kun je de binnenste lagen van de werken onderzoeken zonder beschadigen, enz. Micro-organismen en insecten die vastzaten in natte schilderijen kunnen zelfs worden opgespoord en hun leeftijd geanalyseerd.
Tot slot kunnen isotopen ook worden gebruikt om werken behouden en voorkomen dat ze beschadigd raken. Bepaalde werken kunnen bedekt zijn met een stof waarop vervolgens gammastraling wordt toegepast. Deze combinatie van monomeren en straling vertraagt de verslechtering van het werk omdat het het progressieve verlies van fixatie vermindert dat het werk lijdt wanneer het wordt blootgesteld aan de omgeving, het wordt gesteriliseerd en insecten, schimmels en anderen die de Toneelstukken. Deze methode wordt meestal toegepast op schilderijen, maar er zijn andere methoden die het mogelijk maken om zelfs boeken te herstellen in extreme omstandigheden van bewaring.

Isotopen in landbouw en voedsel.
Landbouw en voedsel gebruiken isotopen op alle niveaus, van voordat de plant wordt geplant tot hij onze tafel bereikt. Isotopen worden gebruikt voor de genetische verbetering van plantensoorten die erg belangrijk zijn voor menselijke consumptie, waardoor de ontwikkeling van genetische variëteiten productiever, resistenter en efficiënter. Eenmaal in de plantage laten de isotopen ons toe bewust gebruik van kunstmest omdat ze ons in staat stellen om hun overmatig gebruik te detecteren. Ten slotte worden tijdens de voorbereiding voor marketing isotopen gebruikt tijdens sterilisatie, zowel van containers als hetzelfde product zelf, waardoor het langer en in betere omstandigheden meegaat, totdat het consumptie.
Andere toepassingen van isotopen.
Er zijn veel andere toepassingen van isotopen, zoals de volgende:
- Studie van de watercyclus. Hydrologie gebruikt isotopen om de watercyclus te volgen en mogelijke verontreiniging van het water tijdens verschillende fasen van de cyclus te detecteren. Een van de belangrijkste toepassingen is het opsporen van grondwaterverontreiniging, met name door overmatig gebruik van meststoffen.
- Vervuilingsstudies. Isotopen worden niet alleen gebruikt om waterverontreiniging te bepalen, zoals we in het vorige punt hebben gezien, maar ze kunnen ook worden gebruikt om de aanwezigheid van verbindingen te bepalen zwavel- en stikstofverontreinigende stoffen in de atmosfeer of om de verontreiniging van sedimenten door aardoliederivaten te bestuderen die bijvoorbeeld kunnen ontstaan door een lekkage onwettig.
- Toepassingen van isotopen in de industrie. De studie en kennis van de eigenschappen van de verschillende isotopen hebben de industrie in staat gesteld om processen te verbeteren en te ontwikkelen maar ook om te verifiëren dat verschillende instrumenten, onderdelen of objecten in perfecte staat verkeren (controle van kwaliteit).
- In mijnbouw en kosmologie. Isotopen worden gebruikt om kernsondes te maken, die de samenstelling van de verschillende lagen van onze planeet bestuderen. Aan de andere kant, de studie van de isotopen die meteorieten stelt ons in staat om de ouderdom van het heelal, de mogelijke oorsprong van deze meteorieten en de kenmerken ervan te onderzoeken.
- Isotopen en de studie van de ruimte. Isotopen worden gebruikt om kerncellen te maken; Deze apparaten worden gebruikt als energieopslag die de apparatuur en instrumenten van satellieten en ruimtesondes van stroom voorziet.
Als u meer artikelen wilt lezen die vergelijkbaar zijn met Waar zijn isotopen voor?, raden we u aan om onze categorie van het atoom.
Bibliografie
- Guerrero, R., & Berlanga, M. (2000). Stabiele isotopen: grondgedachte en toepassingen. Huidige Spaanse Vereniging voor Microbiologie (29).
- Enresa-UCO-leerstoel (s.f) Gebruik van radioactiviteit.