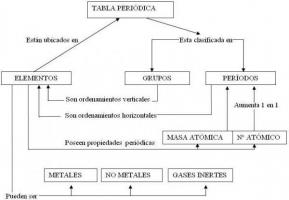
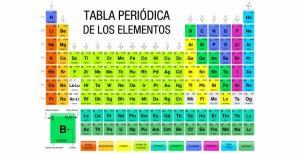
Finn ut hvor elektronene er i et ATOM

Elektroner er subatomære partikler som kretser rundt atomkjernen i en elektronsky som kalles elektronisk cortex. I denne leksjonen fra en LÆRER vil vi se hvor er elektronene innenfor atomstrukturen, samt oppførselen til elektroner i de forskjellige tilstandene til atomene (bakken og opphisselsestilstand), når atomer dannes monatomiske ioner og når elektronene ikke er bundet til noe bestemt atom.
Indeks
- Hva er elektroner og hvor finnes de?
- Hvordan vite hva er valenselektronene?
- Elektroner av et atom: jordtilstand og i tilstand av eksitasjon
- Elektron gevinst eller tap: Monatomisk iondannelse
- Elektroner i bevegelse: elektrisk strøm
Hva er elektroner og hvor finnes de?
De elektroner Jeg vet finn inni av atomersom er de minste enhetene som utgjør saken. Atomer er udelbare og strukturen og sammensetningen avgjør materialets egenskaper.
Atomer består av tre typer subatomære partikler:
- Protoner: er partikler med masse og positiv ladning
- Nøytroner: er partikler med masse og uten elektrisk ladning
- Elektroner: De er masseløse og negativt ladede partikler.
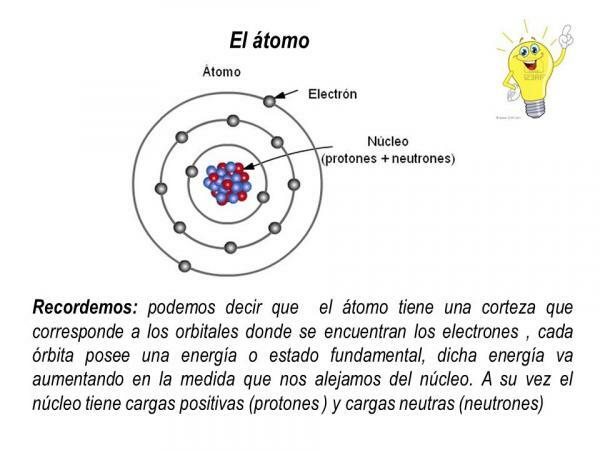
Protoner og nøytroner er en del av atomkjernen, slik at atomkjernen den konsentrerer hele massen og den positive ladningen til atomet.
Elektronene, derimot, kretser rundt kjernen i definerte baner og danner en elektronsky som kalles elektronisk cortex. Atommets elektroniske skall konsentrerer hele den negative ladningen og har ingen masse.
Elektronbaner
Banene som elektronene beskriver rundt atomkjernen er visse forhåndsdefinerte baner. Det vil si at banene til elektronene rundt atomkjernen ikke er tilfeldige. Innenfor det elektroniske skallet er det bare noen få mulige baner for elektroner; mens andre baner er forbudt. er definert som atombane det området rundt kjernen der sannsynligheten for å finne et elektron er større enn 90%.
I hver av disse mulige orbitalene får elektronet som sirkulerer gjennom det en viss energi som øker ettersom orbitalene er lenger fra kjernen. Orbitalene er gruppert i forskjellige energinivåer (n) eller lag, det er totalt 7 energinivåer, hvor n = 1 er det laveste energinivået og nærmest atomkjernen. I hvert av energinivåene eller laget er det forskjellige typer orbitaler (s, p, d og f orbitaler)
Arrangementet der elektroner fordeles i de forskjellige energinivåene og orbitalene i et atom er kjent som elektronisk konfigurasjon.
Bilde: Lysbildespiller
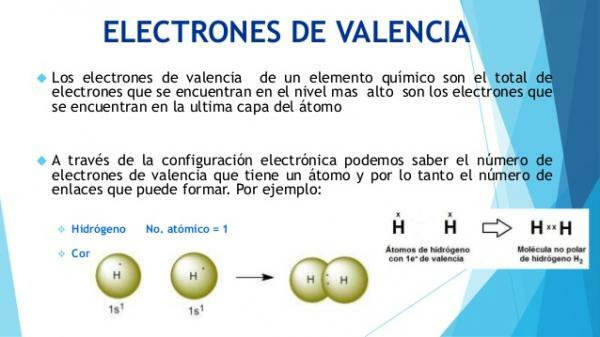
Hvordan vite hva er valenselektronene?
De fysiske og kjemiske egenskapene til atomer er definert av deres sammensetning og, spesielt, av deres elektroniske konfigurasjon ytterste lag (valenslag).
Kjemiske elementer er de forskjellige typer atomer som eksisterer og er definert av deres atomnummer (Z) og deres massetall (A).
- Atomnummer (Z): antall protoner av et atomelement, som er lik antall elektroner hvis atomet er nøytralt.
- Massetall (A): antall partikler med masse av et atomelement, det vil si summen av partiklene i atomkjernen (protoner pluss nøytroner).
Hvert element tildeles a kjemisk symbol som representerer det, og settet av dem alle sendes i det vitenskapelige dokumentet som ordner etter deres atomnummer og grupperer dem i henhold til deres egenskaper i familier og grupper av affine: den Periodiske tabell.
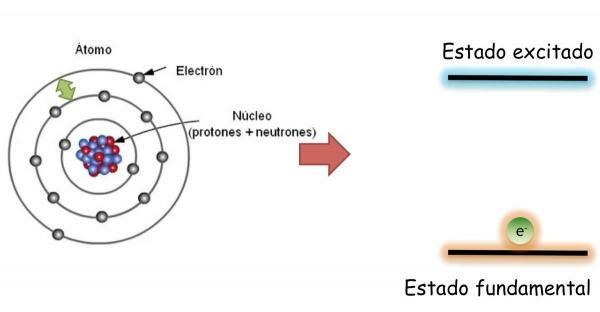
Elektroner av et atom: jordtilstand og i eksitasjonstilstand.
I grunnleggende tilstand, som er definert som tilstanden med minimum energi og maksimal stabilitet av et atom; elektronene fordeles ikke tilfeldig i de forskjellige atomorbitalene, men okkuperer de forskjellige orbitalene på en ordnet måte, og fyller alltid ut i utgangspunktet, lavere energifrie orbitaler.
I denne tilstanden har atomet samme antall elektroner som protoner, og de positive og negative ladningene kompenserer hverandre, derfor er atomet som helhet nøytralt (det har ingen nettolading).
Imidlertid elektronene kan hoppe fra en bane til en annen avgir eller absorberer energi. Når elektronene til et atom ikke fyller orbitalene på en ordnet måte, sies det at atomet er i spent tilstand. I den opphissede tilstanden opptar en eller flere elektroner orbitaler med høyere energi og etterlater tomme med lavere energi. I begeistret tilstand er atomene svært ustabile og har en tendens til raskt å gå tilbake til bakken.
Når du bytter omløp elektronet avgir eller absorberer energi. Hvis elektronet hopper fra en bane med lavere energi til en høyere energi, vil atomet absorbere energi; mens hvis hoppet blir gjort i motsatt retning (fra en bane med høyere energi til en med lavere energi), vil atom frigjøre energi.
Tap eller gevinst av elektroner: dannelse av monatomiske ioner.
Elektronene i det ytterste skallet av den elektroniske cortexen (kalt valensskall) er elektroner som de kan forlate atomet eller de kan innlemmes for denne. På denne måten kan et atom få eller miste elektroner.
I en nøytralt atom antall protoner som er tilstede i kjernen er lik det elektronene som utgjør dets elektroniske skall. Det vil si at antallet positive ladninger er lik antallet negative ladninger. Når det er gevinst eller tap av elektroner, dannes atomene monatomiske ioner.
Typer monatomiske ioner
I henhold til ladningen til ionet skilles det mellom to typer:
- Monatomiske kationer: atomer som har mistet en eller flere elektroner, slik at en del av den positive ladningen til kjernen ikke blir kompensert. Derfor får atomet en netto positiv ladning.
- Monatomiske anioner: atomer som har fått en eller flere elektroner slik at antall elektroner er større enn antall protoner i kjernen slik at atomet får en netto negativ ladning.

Elektroner i bevegelse: elektrisk strøm.
Når elektroner de er ikke bundet til noe atom spesielt beveger de seg gjennom det frie rommet mellom atomer. Denne uavhengige bevegelsen av elektroner danner en strøm av elektrisk ladning som kan bevege seg gjennom visse materialer (ledende og halvledermaterialer).
Dette er for eksempel det som skjer i tilfelle elektrisk strøm som leverer strøm til bygninger, kjøretøy osv.
Hvis du vil lese flere artikler som ligner på Hvor finnes elektronene?, anbefaler vi at du skriver inn vår kategori av Atomet.
Bibliografi
Alejandrina Gallego Picó, Rosa Mª Garcinuño Martínez, Mª José Morcillo Ortega, Miguel Ángel Vázquez Segura. (2018) Grunnleggende kjemi. Madrid: Uned