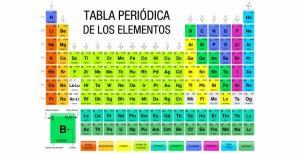
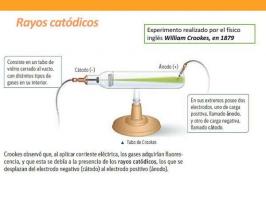
Struktura i charakterystyka atomu

Obraz: SlidePlayer
Atomy są częścią naszego świata. Cała materia składa się z atomów, dlatego ważne jest, aby lepiej zrozumieć, z czego się składają i jakie są ich funkcje. W tej lekcji od NAUCZYCIELA powiemy Ci, co budowa atomu i charakterystyka. Jeśli chcesz dowiedzieć się więcej o cząsteczkach, z których składa się cała materia, czytaj dalej ten artykuł.
Indeks
- Czym są atomy?
- Struktura atomu
- Główne cechy atomu
- Czym są izotopy?
- Jak atomy znajdują się w przyrodzie?
Czym są atomy?
atom to jest najmniejsza jednostka, na którą można podzielić materię bez utraty swoich właściwości chemicznych, czyli swoich właściwości jako pierwiastka chemicznego. Atom jest źródłem wszystkiego, co można zobaczyć lub dotknąć, od gwiazd po poranne śniadanie.
Jeśli odłożymy na bok utratę jego właściwości chemicznych, możemy powiedzieć, że atom składa się z różnych cząstek, zwanych cząstkami subatomowymi. Istnieją trzy rodzaje cząstek subatomowych -protony, neutrony i elektrony- o różnych cechach.
Cząstki te są pogrupowane w różne liczby, tworząc pierwiastki chemiczne (tlen, węgiel itp.), ale zawsze będą rozmieszczone zgodnie ze stałą strukturą.

Obraz: Witryny Google
Budowa atomu.
Struktura atomu jest ustalona, to znaczy możemy mieć różne typy atomów (atom wodoru, atom tlenu itp.), ale ich cząsteczki subatomowe są zawsze zorganizowane w podobny sposób jak układ planetarny.
Na pewno zapamiętasz, jak zorganizowany jest Układ Słoneczny: Słońce jest w centrum i dookoła od tego planety obracają się, opisując różne orbity, jedne bliższe, a inne bardziej odległe od Słońce. W przypadku atomów w centrum znajduje się rdzeń, o kształcie zbliżonym do jeżyny i składa się z neutrony i protony.
Wokół rdzenia znajduje się Kora który jest obszarem, przez który elektrony. Dawniej sądzono, że elektrony opisują pewne orbity, podobnie jak planety, chociaż teraz tak jest wie, że te orbity nie są tak dobrze zdefiniowane i bardziej przypominają obszary, w których jesteśmy bardziej skłonni się znaleźć elektrony.
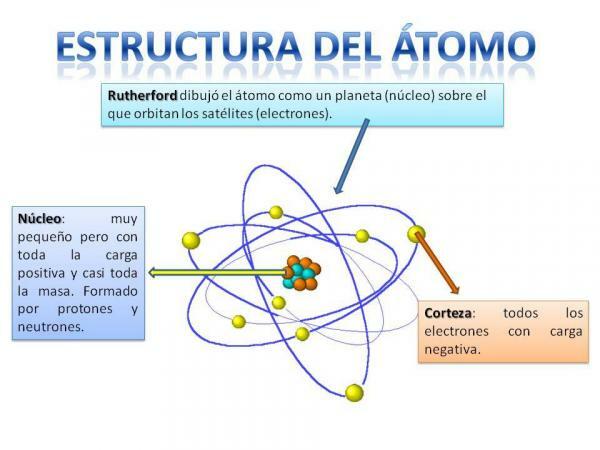
Zdjęcie: REA - Plan Ceibal
Główne cechy atomu.
Kontynuując tę lekcję na temat struktury i cech atomu, ważne jest, aby skupić się na elementach, które sprawiają, że atom jest uważany za taki.
I w tym celu musimy odpowiedzieć na to pytanie: Dlaczego wszystkie atomy decydują się na taki porządek? Odpowiedź jest prosta: to zasługa elektryczne siły przyciągania. Jądro atomu składa się z neutronów, które nie mają ładunku elektrycznego, oraz protonów, które mają dodatni ładunek elektryczny. a elektrony mają ujemny ładunek elektryczny, więc między jądrem a elektronami istnieje podobna siła przyciągania wytwarzany między dwoma biegunami magnesu, ale nie jest wystarczająco silny, aby elektrony „spadły” do rdzeń.
Lepiej to zrozumieć, jeśli weźmiemy pod uwagę rozmiar rdzenia: gdyby atom miał np. wymiar stadionu piłkarskiego, jądro miałoby wymiar piłki w środku z boiska Ile siły przyciągającej musiałaby wywołać piłka, aby spadły na nią trybuny stadionowe!
Funkcja neutronów
Teraz możesz się zastanawiać, jaką rolę odgrywają neutrony? Mimo że nie mają ładunku elektrycznego, neutrony odgrywają wielką rolę w atomie: stanowią 99% masy. Jeśli to pomoże Ci zapamiętać, możemy powiedzieć, że atom jest jak banda trzech przyjaciół: ciężka neutron, dodatni proton i ujemny elektron, który krąży wokół neutronu i elektron.
Ruch elektronów
W tym momencie chcę, żebyśmy wrócili do czegoś, co zostawiliśmy w kałamarzu: orbit, które elektrony opisują wokół jądra. Powiedzieliśmy, że elektrony krążą wokół jądra tak jak planety wokół Słońca, niektóre bliżej niż inne, dlaczego to robią? Elektrony obracają się w jednej lub drugiej powłoce w zależności od energii, którą muszą oddalić od jądra, to znaczy elektrony, które są bliżej jądra, nie mają wystarczającą siłę, aby oddalić się od jądra, podczas gdy te w najbardziej zewnętrznych warstwach (orbitalach) skorupy mają więcej energii i były w stanie oddalić się dalej od jądra. rdzeń. Ponadto na każdym z orbitali znajduje się maksymalna pojemność 8 elektronów (reguła oktetu).
Cząstki atomu
Wrócimy do innego podejścia, które zrobiliśmy wcześniej, ale którego nie wyjaśniliśmy: atomy składają się z neutrony, protony i elektrony, które zawsze łączą się zgodnie z tą samą strukturą jądra i skorupy, ale robią to w różnej liczbie, tworząc różne pierwiastki chemiczne. Jak możemy uzyskać tak wiele pierwiastków łączących tylko 3 rodzaje cząstek? Pierwiastki chemiczne, które kiedykolwiek widziałeś w układzie okresowym, charakteryzują się pewną liczbą atomową.
liczba atomowa (Z) Mówi nam o liczbie protonów w jądrze tego typu atomu, która jest równa liczbie elektronów w normalnych warunkach. Na przykład wszystkie atomy, które mają 6 protonów (Z = 6) będą atomami węgla i będą miały te same właściwości chemiczne; atomy z 5 protonami (Z = 5) będą atomami boru o tych samych właściwościach chemicznych i różniących się od atomów węgla. Nie musisz mylić liczby atomowej z masą atomową lub liczba masowa (A), czyli suma mas neutronów i protonów (masa elektronów jest znikoma w stosunku do masy całego jądra).

Obraz: SlidePlayer
Czym są izotopy?
W naturze możemy znaleźć różne „podtypy” pierwiastków, izotopy. Jestem pewien, że w pewnym momencie słyszałeś o węglu 14, radioaktywnym izotopie węgla używanym między innymi do określania wieku skamieniałości. Izotopy są dwa atomy o tej samej liczbie protonów (ta sama liczba atomowa), ale inna liczba neutronów (inna masa atomowa). Izotopy tego samego pierwiastka są zwykle nazywane nazwą pierwiastka, po której następuje jego masa atomowa.
W naszym przykładzie oba izotopy są węglem, więc mają liczbę atomową 6 (Z = 6) ale węgiel 12 („normalny” węgiel) ma masę atomową 12 w porównaniu do masy atomowej węgla 14 14. Izotopy tego samego pierwiastka mają bardzo podobne właściwości chemiczne i fizyczne. W przypadku węgla 14, w przeciwieństwie do węgla 12, jest to radioaktywny izotop, który występuje we wszystkich pierwiastkach zawierających węgiel, w tym w organizmach żywych.
I na tym kończymy lekcję o budowie atomu i cechach. Mamy nadzieję, że to ci pomogło.

Obraz: Twoje zadania
Jak atomy znajdują się w przyrodzie?
Atomy można znaleźć w izolacji, ale najzwyklejszą rzeczą jest ich odnalezienie połączone w grupy nazywa molekuły.
Cząsteczki mogą składać się z atomów tego samego pierwiastka (takich jak cząsteczka tlenu, składająca się z dwóch atomów tlenu) lub grupami z atomami różnych pierwiastków (dwa atomy wodoru i jeden tlenu tworzą cząsteczkę Woda). Te grupy pierwiastków nazywane są cząsteczkami, które z kolei można łączyć ze sobą i tworzenie różnych, coraz bardziej złożonych ugrupowań zgodnie z ich reaktywnością i powinowactwem chemicznym do źródło związki chemiczne chemical.
Jeśli chcesz przeczytać więcej artykułów podobnych do Struktura i charakterystyka atomu, zalecamy wpisanie naszej kategorii Atom.