TODAS as propriedades do ATOM

Imagem: SlideShare
Embora não possamos vê-los a olho nu, átomos são parte de toda matéria do nosso planeta. Toda matéria é feita de átomos, que se agrupam para formar elementos químicos, moléculas, compostos, etc. O átomo é definido como o menor unidade básica de matéria que possui as propriedades de um elemento químico. Cada elemento químico é definido pelo tipo de átomo de que é feito, então a questão final é: quais propriedades o átomo tem? Nesta lição de um PROFESSOR, revisaremos o propriedades do átomo que tornam cada átomo um elemento químico característico.
Índice
- Qual é o átomo?
- Número atômico, número de massa e isótopos
- Densidade, outra das propriedades do átomo
- Raio iônico e raio de Vanderwalls
- Energia de ionização
Qual é o átomo?
Antes de entrarmos para analisar as propriedades do átomo é importante que saibamos melhor do que se trata. O átomo é uma unidade formada por três partículas subatômicas: prótons, nêutrons e elétrons. Estes são organizados em núcleo e córtex.
- O testemunho é formado por prótons Y nêutrons, que está no centro do átomo e é responsável pela maior parte do peso do átomo; os prótons são carregados positivamente, enquanto os nêutrons são neutros, então o núcleo é carregado positivamente.
- O Córtex É formado por elétrons, que são pequenas partículas carregadas negativamente que giram em torno do núcleo formando órbitas (como a dos planetas), mas sem nunca cair para o núcleo do átomo. O córtex do átomo é o encarregado de interagir com o córtex dos demais átomos, pois está localizado na parte externa dos átomos.
Os diferentes átomos são constituídos por prótons, nêutrons e elétrons, iguais em todos os elementos químicos. Então, o que faz com que haja diferentes elementos químicos? O número de prótons, nêutrons e elétrons dos quais os átomos de cada elemento são compostos é diferente e isso, por sua vez, faz com que cada elemento tenha diferentes caracteristicas ou outros.

Imagem: SlideShare
O número atômico, o número de massa e os isótopos.
As três primeiras características têm a ver diretamente com o número de partículas que constituem o átomo de cada elemento.
O número atômico (Z) indica o número de prótons que constituem o núcleo de um átomo. Assim, por exemplo, todos os átomos de ferro terão 26 prótons em seus núcleos. Além disso, se não nos disserem o contrário, os elementos químicos estão em um estado neutro, ou seja, o carga positiva (prótons) e negativa (elétrons) é a mesma, então todos eles também terão 26 elétrons.
O Número de massa ou peso atômico (A) indica o número total de prótons e nêutrons que constituem o núcleo de um átomo. Como já indicamos antes, o peso dos elétrons é praticamente desprezível em comparação com o dos elétrons. prótons e nêutrons, então o número de massa indica indiretamente o peso do átomo em questão. Continuando com o exemplo do ferro, se você consultar a tabela periódica dos elementos verá que o peso atômico deste elemento é 55,85, o que significa que todos os átomos desse elemento terão aquele peso.
finalmente, o isótopos de um elemento químico são variantes do mesmo átomo (ou seja, têm o mesmo número atômico), mas um número de massa diferente, ou seja, um número diferente de nêutrons. A maioria dos elementos químicos tem mais de um isótopo natural, sendo o elemento com a maior quantidade de isótopos estáveis o estanho (Sn), que possui 10 isótopos naturais diferentes.
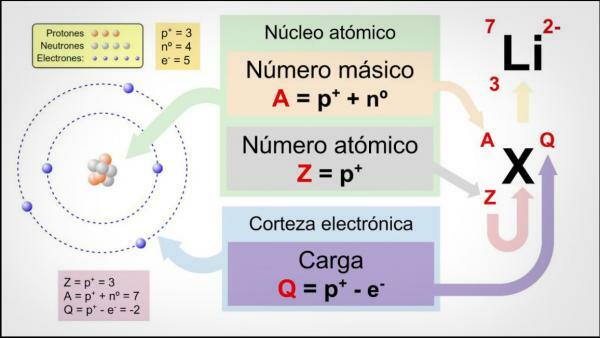
Imagem: ConceptDefinition.de
Densidade, outra propriedade do átomo.
O densidade de um átomo é o número de unidades de massa (u.m.a) do elemento que estão presentes em um determinado volume do espaço. A densidade de qualquer substância é simbolizada pela letra grega "Ro" (escrito r) e suas unidades de acordo com o sistema internacional de unidades (SI) são quilogramas por metro cúbico (kg / m3). No caso dos elementos químicos, por serem tão pequenos, o grama por centímetro cúbico (g / cm3).
A fim de calcular a densidade de um átomo (densidade atômica), teríamos que levar em consideração a massa do átomo e seu volume. Enquanto a maior parte da massa do átomo está no núcleo do mesmo, o volume tem que fazer com o quão grande é o átomo e, portanto, o número de orbitais eletrônicos terá um papel importante. Levando em consideração essas propriedades e sua tendência no sistema periódico, podemos observar que o a densidade aumenta à medida que aumentamos em um grupo e também aumenta à medida que nos aproximamos da parte central da tabela periódica.
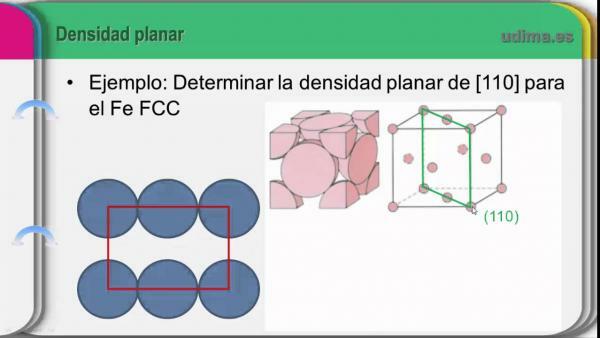
Imagem: YouTube
Raio iônico e raio de Vanderwalls.
O raio iônico é o raio que um íon de um elemento possui no estado de cristal iônico. Nesse estado, os íons estão tão próximos que os orbitais eletrônicos mais externos estão em contato uns com os outros.
Por outro lado, o raio de Vanderwalls É a distância na qual dois átomos são mantidos separados devido à repulsão de cargas negativas que existem entre os elétrons de cada um dos átomos. O raio de Vanderwalls seria o raio de uma esfera sólida imaginária usada para modelar o átomo, portanto, não é muito usado na prática diária.
Ao contrário do que acontece com a densidade ou massa, essas duas propriedades estão intimamente relacionadas com o volume do átomo, isto é, eles têm mais a ver com o número de elétrons nele do que com o testemunho.

Imagem: SlidePlayer
Energia de ionização.
Finalmente, outra das propriedades do átomo é o energia de ionização, uma propriedade que nos diz a energia de que precisamos para separar um elétron em seu estado fundamental (diferente de um ânion ou cátion) de um átomo de um elemento em estado gasoso, mas também pode ser definido como a força com a qual um elétron se liga a outro moléculas. Esta propriedade é muito interessante, pois nos permite ter uma ideia aproximada do capacidade de reagir de um átomo de um determinado elemento químico. A energia de ionização é maior à medida que removemos os elétrons, portanto, para um elemento, há uma energia de primeira ionização, uma segunda energia de ionização, e assim por diante e eles ficam cada vez maiores.
Como no caso anterior, esta propriedade também está intimamente relacionada ao número de orbitais do elemento em questão, pois quanto menos orbitais ele tiver, mais custará remover os elétrons de um átomo determinado.
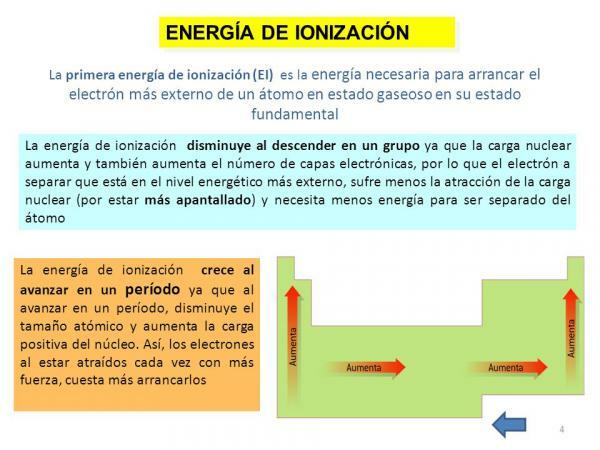
Imagem: SlidePlayer
Se você quiser ler mais artigos semelhantes a Propriedades do átomo, recomendamos que você insira nossa categoria de O átomo.