Diagrama de Moeller: o que é, como é usado em Química e exemplos
A química pode ser especialmente complicada, portanto, qualquer ferramenta que facilite o aprendizado para aqueles que são apresentados a ela é bem-vinda.
Um dos métodos mais populares de se familiarizar com a regra de Madelung e a configuração eletrônica dos átomos é o diagrama de Moeller, uma regra mnemônica gráfica que torna muito fácil ver em quais orbitais o elétrons.
A seguir vamos descobrir em que consiste o diagrama de Moeller, como se relaciona com a regra de Madelung, como é aplicada por meio de alguns exemplos resolvidos e quais elementos químicos não obedecem a esta estratégia.
- Artigo relacionado: "Os 5 tipos de ligações químicas: é assim que a matéria é composta"
Qual é o diagrama de Moeller?
O diagrama de Moeller, também conhecido como método da chuva ou regra das diagonais, é um método gráfico e mnemônico para aprender a regra de Madelung, uma técnica para conhecer e escrever a configuração eletrônica de elementos químicos.
Este diagrama é caracterizado pelo desenho de diagonais através das colunas dos orbitais, de cima para baixo, da direita para a esquerda. Por meio do diagrama de Moeller, é definida uma ordem no preenchimento dos orbitais, que será definida por três números quânticos: n, le ml.
O diagrama de Moeller funciona de acordo com o seguinte:

Cada coluna corresponde a um orbital diferente por onde circulam os elétrons de um átomo, partículas subatômicas de carga negativa. Os orbitais em questão são: s, p, d e f, cada um com um espaço específico para abrigar elétrons e, portanto, diferentes níveis de energia.
Se desenharmos as diagonais ou setas no sentido acima mencionado, temos que o primeiro orbital é 1s. A segunda flecha começa com o orbital 2s. A terceira flecha cruza 2p e 3s. A quarta diagonal é 3p e 4s. A quinta diagonal é 3d, 4p e 5s e assim por diante. O diagrama de Moeller é uma técnica introdutória para quem está começando a estudar as configurações eletrônicas dos elementos da tabela periódica em química.
- Você pode estar interessado: "Os 6 ramos principais das ciências naturais"
Regra de Madelung
Já que o diagrama de Moeller é a representação gráfica da regra de Madelung (também conhecido como regra de Klechkovsky em alguns países) devemos primeiro saber do que se trata. De acordo com esta regra, o preenchimento dos orbitais de um átomo deve obedecer às seguintes duas regras:
A primeira regra de Madelung
Os orbitais com os valores mais baixos de n + l são preenchidos primeiro, com n sendo o número quântico principal e l sendo o momento angular orbital..
Por exemplo, o orbital 3d corresponde a n = 3 e l = 2. Portanto, n + l = 3 + 2 = 5. Em vez disso, o orbital 4s corresponde a n = 4 e l = 0, portanto, n + l = 4 + 0 = 4. A partir disso é estabelecido que os elétrons preenchem o orbital 4s primeiro antes do 3d, pois 4s = 4 enquanto 3d = 5.
- Artigo relacionado: "Os 11 tipos de reações químicas"
Segunda regra de Madelung
Se dois orbitais têm o mesmo valor de n + l, os elétrons vão ocupar aquele com o menor valor de n primeiro.
Por exemplo, o orbital 3d tem um valor de n + l = 5, idêntico ao do orbital 4p (4 + 1 = 5), mas, uma vez que o orbital 3d tem o valor mais baixo para n, ele será preenchido primeiro do que o Orbital 4p.
A partir de todas essas observações e regras, a seguinte ordem pode ser alcançada no preenchimento dos orbitais atômicos: 1s 2s 2p 3s 3p 4s 3d 4p. Embora essa ordem seja fixa, memorizá-la de cor é complicado, e é por isso que existe um diagrama de Moeller que representa graficamente sua ordem.
- Você pode estar interessado: "Os 9 postulados da teoria atômica de Dalton"
Etapas a seguir ao usar o diagrama de Moeller
Como comentamos na seção anterior, a regra de Madelung usa a fórmula n + l para estabelecer o que orbitais são preenchidos antes e a partir disso determinam qual é a configuração eletrônica de um elemento determinado. No entanto, o diagrama de Moeller já representa isso de forma gráfica e fácil, então é suficiente seguir o colunas do mesmo diagrama e desenhar diagonais para descobrir em que ordem os orbitais de cada elemento.
Para descobrir a configuração eletrônica de um átomo e em quais orbitais seus elétrons estão localizados, devemos primeiro saber seu número atômico Z. O número Z corresponde ao número de elétrons em um átomo, desde que esse átomo seja neutro, ou seja, que não seja um íon, nem positivo (cátion) nem negativo (ânion).
Assim, sabendo Z para um átomo neutro, já sabemos quantos elétrons um átomo neutro daquele elemento geralmente possui. Com isso em mente, começaremos a desenhar as diagonais no diagrama de Moeller. Devemos levar em consideração que cada tipo de orbital tem uma capacidade diferente de abrigar elétrons, os quais são:
- s = 2 elétrons
- p = 6 elétrons
- d = 10 elétrons
- f = 14 elétrons
Ele para no orbital onde o último elétron dado por Z foi ocupado.
Exemplos de diagrama de Moeller
Para entender melhor como funciona o diagrama de Moeller, veremos a seguir alguns exemplos práticos de como definir a configuração eletrônica de diferentes elementos.
Berílio
Para estabelecer a configuração eletrônica de um átomo neutro de berílio (Be), o que devemos primeiro fazer é procurá-lo na tabela periódica, um alcalino-terroso que está localizado na segunda coluna e segunda linha da tabela. Seu número atômico é 4, portanto Z = 4 e também possui 4 elétrons.
Levando tudo isso em consideração, usaremos o diagrama de Moeller para ver como os 4 elétrons deste elemento estão localizados. Começamos fazendo diagonais no sentido acima mencionado, de cima para baixo e da direita para a esquerda.
Quando estamos preenchendo orbitais, Recomenda-se colocar o número de elétrons encontrados em cada um deles como um sobrescrito. Como 1s é o primeiro orbital e ocupa dois elétrons, vamos escrevê-lo:

Como ainda temos elétrons livres, continuamos a preencher os orbitais. O próximo é o orbital 2s e, como com 1s, ocupa 2 elétrons, portanto, 2s2. Como já temos todos os elétrons bem localizados nos orbitais do átomo neutro de Be, podemos dizer que a configuração eletrônica deste elemento é:

Garantimos que fizemos bem adicionando os sobrescritos: 2 + 2 = 4
- Você pode estar interessado: "Teoria cinética molecular: os 3 estados da matéria"
Corresponder
O elemento fósforo (P) é um não metal encontrado na terceira linha e coluna 16 da tabela periódica, com Z = 15, portanto tem 15 elétrons no total que devem ocupar os orbitais.
Tendo visto o exemplo anterior, podemos avançar um pouco e localizar 4 de seus elétrons nos mesmos orbitais que o berílio tem para seus 4 elétrons, faltando 9 elétrons mais.

Após o orbital 2s, a próxima diagonal entra no orbital 2p e termina no orbital 3s. O orbital 2p pode ocupar 6 elétrons e, no caso de 3s, apenas 2. Assim, teríamos:
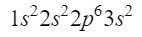
No momento temos 12 elétrons bem localizados, mas ainda temos mais 3 pela frente. Fazemos outra diagonal e desta vez entramos pelo orbital 3p de acordo com o diagrama de Moeller, um orbital que tem espaço para 6 elétrons, mas como temos apenas 3 elétrons restantes, este orbital não estará completamente ocupado, colocando 3 como um sobrescrito. Assim, para acabar com o fósforo, sua configuração eletrônica é a seguinte:

Garantimos que fizemos bem adicionando os sobrescritos: 2 + 2 + 6 + 2 + 3 = 15
Zircônio
O elemento zircônio (Zr) é um metal de transição encontrado na coluna 4 e linha 5 e tem um Z = 40. Encurtando o caminho aproveitando o exemplo anterior, podemos localizar os primeiros 18 elétrons.
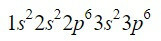
Depois do orbital 3p, os próximos a preencher, nos guiando pelo diagrama de Moeller, são os orbitais 4s, 3d, 4p e 5s, com capacidade para 2, 10, 6 e 2 elétrons respectivamente.

Completar os primeiros nove orbitais no diagrama adiciona um total de 20 elétrons, deixando os 2 elétrons restantes que estão alojados no próximo orbital, o 4d. Assim, a configuração eletrônica do elemento neutro zircônio é:
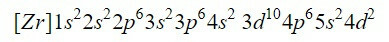
Garantimos que fizemos bem adicionando os sobrescritos: 2 + 2 + 6 + 2 + 6 + 2 + 10 + 6 + 2 + 2 = 40
Oxigênio
Aqui vemos um exemplo um pouco mais complicado que é o oxigênio (O). Este gás é encontrado na coluna 16 e linha 2 da tabela periódica, é um não metal e tem um número atômico 8.
Até agora, olhando os outros exemplos, poderíamos pensar que é Z = 8, porém não é tão simples, pois este gás é de natureza especial, quase sempre na forma de um íon com carga de -2.
Isso significa que, embora um átomo de oxigênio neutro tenha 8 elétrons, conforme indicado por seu número atômico, ele tem É verdade que na natureza ele tem mais, no seu caso 10 (8 elétrons + 2 elétrons ou, se preferir, -8 de carga elétrica -2).
Então, neste caso, o número de elétrons que temos que localizar nos orbitais não é 8, mas 10 elétrons, como se estivéssemos localizando os elétrons do elemento químico neon que tem Z = 10.
Compreendendo isso, só temos que fazer a mesma coisa que temos feito nos casos anteriores, apenas levando em consideração que estamos trabalhando com um íon (ânion):
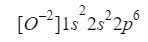
Garantimos que fizemos bem adicionando os sobrescritos: 2 + 2 + 6 = 10
Cálcio
Algo semelhante ao oxigênio acontece com o cálcio (Ca), só que neste caso estamos falando de um cátion, ou seja, um íon com carga positiva.
Este elemento é encontrado na coluna 2, linha 4 da tabela periódica, com um número atômico de 20, no entanto, no A natureza é geralmente apresentada na forma de um íon com carga positiva +2, o que significa que sua carga eletrônica é 18 (- 20 + 2 = 18; 20 elétrons - 2 elétrons = 18 elétrons).
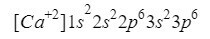
Garantimos que fizemos bem adicionando os sobrescritos: 2 + 2 + 6 + 2 + 6 = 18
Exceções ao diagrama de Moeller e à regra de Madelung
Embora o diagrama de Moeller seja muito útil para entender a regra de Madelung e saber como os elétrons dos diferentes elementos químicos estão localizados, a verdade é que ele não é infalível. Existem certas substâncias cuja composição não obedece ao que explicamos.
Suas configurações eletrônicas diferem experimentalmente daquelas previstas pela regra de Madelung por razões quânticas.. Dentre esses elementos que não seguem os padrões temos: cromo (Cr, Z = 24), cobre (Cu, Z = 29), prata (Ag, Z = 47), ródio (Rh, Z = 45), cério ( Ce, Z = 58), nióbio (Nb; Z = 41), entre outros.
Exceções são muito frequentes no preenchimento dos orbitais d e f. Por exemplo, no caso do cromo, que deve ter uma configuração de valência terminando em 4s ^ 2 3d ^ 4 de acordo com o diagrama de Moeller e a regra de Madelung, ele na verdade tem uma configuração de valência de 4s ^ 1 3d ^ 5. Outro exemplo estranho é o da prata, que em vez de ter 5s ^ 2 4d ^ 9 como o último, tem 5s ^ 1 4d ^ 10.

