Hlavné CHARAKTERISTIKY izotopov

Obrázok: Planéty
Všetka hmota, ktorá tvorí našu planétu, je tvorená atómami. Ale všetky atómy nie sú rovnaké, atómy rôznych prvkov majú rôzny počet protónov, neutrónov a elektrónov. Niekedy je ich počet subatomárne častice nie sú rovnaké, nie sú vyvážené a druhy ako izotopy. Izotopy sú atómy toho istého prvku (napríklad vodíka), ale nemajú rovnaký počet neutrónov. Táto „nerovnováha“ spôsobuje charakteristiky izotopov rovnakého prvku nie sú rovnaké. V tejto lekcii UČITEĽA sa podrobne pozrieme na všetky tieto vlastnosti. Začali sme!
Register
- Čo je to izotop?
- Atómové vlastnosti izotopov
- Zvedavá aplikácia izotopov: izotopové značenie
- Vlastnosti izotopov toho istého prvku
Čo je to izotop?
Predtým, ako začnete hovoriť o vlastnostiach izotopov, je dôležité lepšie pochopiť, o čo ide. subatomárna častica. Mohli by sme povedať, čo sú to izotopy sú „podskupiny“ atómov: Oni sú atómy rovnakého prvku, ale ktoré sa líšia v určitých veciach.
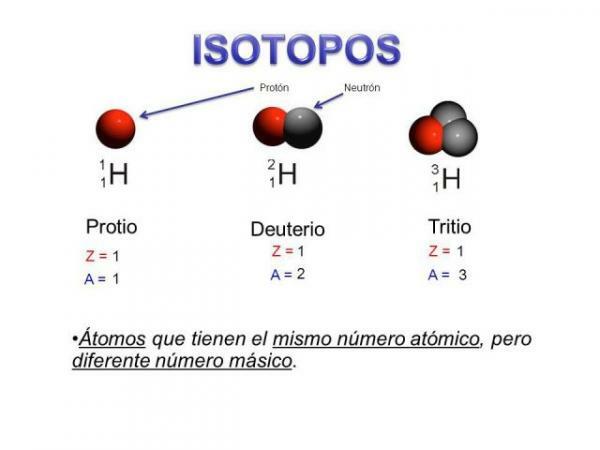
Izotopy sú dva atómy s rovnakým počtom protónov
(rovnaké atómové číslo), ale rôzny počet neutrónov (iná atómová hmotnosť). Izotopy toho istého prvku sú zvyčajne pomenované podľa názvu prvku, za ktorým nasleduje jeho atómová hmotnosť. Je všeobecne známe al štrnásť uhlíka (C14), ktorý sa používa na určenie veku fosílií, ale uhlík má ďalšie izotopy, ako napr uhlík 12 a uhlík 13, ktoré sú stabilnejšie ako iné izotopy uhlíka, ako je uhlík 8 alebo uhlík uhlík 22.V našom prípade sú všetky tieto atómy uhlíkovými atómami, takže majú atómové číslo 6 (Z = 6), ale uhlík 12 („Normálny“ uhlík) má atómovú hmotnosť 12 oproti atómovej hmotnosti 14 uhlíka 14 alebo atómovej hmotnosti 8 uhlíka C8.
Tieto rozdiely medzi rôznymi izotopmi môžu spôsobiť, že atómy majú odlišné vlastnosti, správanie sa s atómami iných prvkov, polčasy rozpadu atď.
Obrázok: Vaše úlohy
Atómové vlastnosti izotopov.
- Prvou vlastnosťou izotopov na atómovej úrovni je, že sú to všetky izotopy atómy rovnakého prvku.
- Táto hlavná charakteristika nás vedie k druhej charakteristike: všetky izotopy toho istého prvku majú rovnaké atómové číslo, teda rovnaký počet protónov.
- Všetky izotopy prvku majú rovnaký počet protónov.
- Izotopy toho istého prvku majú rôzny počet neutrónov, to znamená rôzne hmotnostné číslo alebo atómová hmotnosť.

Obrázok: EHU
Zvedavá aplikácia izotopov: izotopové značenie.
Izotopové označovanie je technika, ktorá využíva dve veľmi dôležité vlastnosti izotopov: že všetky izotopy reagujú rovnakým spôsobom chemické reakcie a ktoré niektorí majú rádioaktivita.
Počas chemickej reakcie môžu byť dve alebo viac látok, nazývané činidlá, kombinujú svoje atómy a vytvárajú ďalšie rôzne látky vznikajúce z rôznych kombinácií, takzvané produkty. The izotopové značenie je technika, pomocou ktorej môžeme do reakcie zaviesť rádioaktívny izotop činidla, aby Bude to reagovať normálnym spôsobom a my ho vďaka rádioaktivite môžeme kedykoľvek lokalizovať vydávať.
Ďalšie varianty tejto techniky nám umožňujú identifikovať rôzne izotopy činidla podľa hmotnostná spektrometria alebo infračervená spektroskopia.

Obrázok: Prehrávač obrázkov
Vlastnosti izotopov toho istého prvku.
V dôsledku atómových charakteristík videných v predchádzajúcej časti môžu mať izotopy toho istého prvku ďalšie typy charakteristík, ktoré popíšeme nižšie.
- Izotopy toho istého prvku majú iná hmota. Fyzikálne vlastnosti ako napr hustota, ktoré budú odlišné pre rôzne izotopy toho istého prvku.
- Istý chemické vlastnosti závisia od typu prvku, ktorý je, a preto sa nebudú líšiť pre rôzne izotopy prvku. Príkladom je rozpustnosť, čo to bude konštantný pre všetky izotopy prvku.
- S ich rovnosťou v chemických vlastnostiach úzko súvisí nasledujúca charakteristika izotopov: izotopy toho istého prvku reagujú rovnakým spôsobom pri chemických reakciách. To znamená, že ak atóm uhlíka 12 (najbežnejší alebo „normálny“ atóm) reaguje s dvoma atómami kyslíka Pri formovaní molekuly oxidu uhličitého vieme, že sú to aj izotopy ostatných uhlíkov oni budú. Toto je veľmi dôležitá vlastnosť pre mnoho praktických aplikácií izotopov a rádioizotopov.
- Izotopy prvku môžu byť prírodného alebo umelého pôvodu. Ak sa dá daný izotop nájsť v prírode, bez toho, aby do jeho vzniku zasiahla ruka človeka, čelíme izotopu prirodzené, zatiaľ čo ak bol vytvorený v jadrových reaktoroch, urýchľovačoch častíc alebo rádioizotopových generátoroch, hovoríme, že je umelý. ten istý prvok môže mať prírodné aj umelé izotopy.
- Izotopy môžu byť rádioaktívne alebo nerádioaktívne. Rádioaktívne izotopy sú tie, v ktorých je prebytok energie, ktorú atóm má tendenciu eliminovať, aby prešiel z nestabilného stavu do stabilnejšieho stavu.
- V súvislosti s predchádzajúcimi charakteristikami môžeme povedať, že izotopy rádioaktívny majú a premenlivá životnosť. Životnosť je doba, ktorá trvá, kým sa izotop rozpadne, to znamená prestane mať prebytočnú energiu, ktorá ho robí nestabilným. Existujú rádioaktívne izotopy, ktoré sú veľmi nestabilné a ich životnosť je niekoľko sekúnd, zatiaľ čo iným trvá niekoľko hodín alebo dokonca rokov, kým sa rozpadnú a stanú sa stabilnejšími izotopmi. Normálne umelo vytvorené atómy majú oveľa kratšiu životnosť alebo dobu rozpadu ako prirodzené.
Ak si chcete prečítať viac podobných článkov Vlastnosti izotopov, odporúčame vám vstúpiť do našej kategórie Atóm.
Bibliografia
- Briceño V, G. (s.f) izotopy.
- Belmonte, A. (15. mája 2019). Vlastnosti atómu.
- Wikipedia (22. októbra 2019). Izotop.
