10 vrst kemičnih vezi (pojasnjeno s primeri)
Kemične vezi so sile, ki držijo atome skupaj da tvorijo molekule. Obstajajo tri vrste vezi med atomi:
- Kovinska vez.
- Jonska vez.
- Kovalentna vez: nepolarna, polarna, preprosta, dvojna, trojna, dativna.
Po zaslugi teh vezi nastanejo vse spojine, ki obstajajo v naravi. Obstajajo tudi sile, ki držijo molekule skupaj, znane kot medmolekularne vezi, kot so:
- Vodikove vezi ali mostovi.
- Dipol-dipolne sile.
Nato razložimo vsako od teh povezav.
| Vrste kemičnih vezi | Značilno | Primeri | |
|---|---|---|---|
| Kovina | Kovinski ioni plavajo v morju gibljivih elektronov. | Kovinski elementi: natrij, barij, srebro, železo, baker. | |
| Jonski | Prenos elektronov z enega atoma na drugega. | Na natrijev klorid+Kl- | |
| Kovalentno | Nepolarna | Med dvema atomoma enakomerno delite elektrone. | Molekularni vodik H-H ali H2 |
| Polar | Neenakomerno delite elektrone med dvema atomoma. | Molekula vode H2ALI | |
| Preprosto | Delite par elektronov. | Molekula klora Cl2 Cl-Cl | |
| Dvojno | Delite dva para elektronov. | Molekula kisika O2 O = O | |
| Trojna | Delite tri pare elektronov. | Molekula dušika N≣N ali N2 | |
| Dativ | Le eden od atomov deli elektrone. | Vez med dušikom in borom v spojini amonijak-bor trifluorid. | |
| Medmolekularne sile | Vodikov most | Vodike v eni molekuli privlačijo elektronegativni atomi druge molekule. | Vodikove vezi med vodikom v eni molekuli vode in kisikom v drugi molekuli vode. |
| Dipol-dipol | Molekule z dvema električnima poloma privlačijo nasprotne polove drugih molekul. | Interakcije med molekulami metana H2C = O |
Kovinska vez
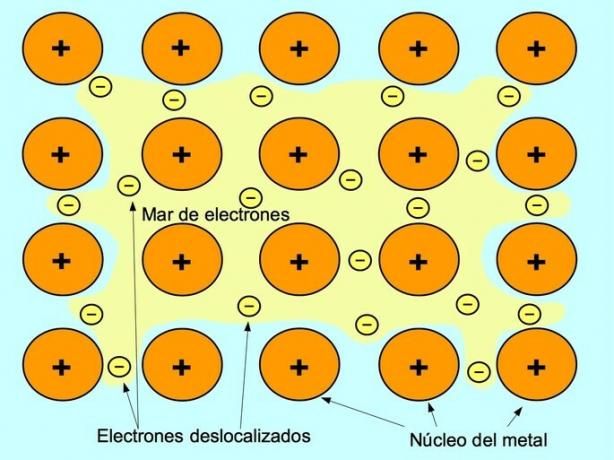
Kovinska vez je sila privlačnosti med pozitivnimi ioni kovinskih elementov in negativnimi elektroni, ki se prosto gibljejo med ioni. Kovinski atomi so tesno zapakirani, kar omogoča elektronom, da se gibljejo znotraj mrež atomov.
V kovinah se valenčni elektroni sprostijo iz prvotnega atoma in tvorijo "morje" elektronov, ki plava okoli celotne kovinske strukture. To povzroči, da se kovinski atomi pretvorijo v pozitivno nabite kovinske ione, ki se spakirajo.
Kovinska vez je vzpostavljena med kovinskimi elementi, kot so natrij Na, barij Ba, kalcij Ca, magnezij Mg, zlato Au, srebro Ag in aluminij Al.
Jonska vez
Ionska vez je sila, ki povezuje kovinski element, kot sta natrij ali magnezij, z nekovinskim elementom, kot sta klor ali žveplo. Kovina izgubi elektrone in se spremeni v pozitivni kovinski ion, imenovan kation. Ti elektroni preidejo v nekovinski element in se ta spremeni v negativno nabit ion, imenovan anion.
Kationi in anioni se združujejo in tvorijo tridimenzionalno mrežo, ki jo vzdržujejo sile elektrostatične privlačnosti med ioni z različnimi naboji. Te sile tvorijo ionske spojine.
Zemeljsko skorjo sestavljajo predvsem ionske spojine. Večina kamnin, mineralov in dragih kamnov je ionskih spojin. Na primer:
- Natrijev klorid NaCl: kovinski element je natrij, ki prenaša elektron v klor, ki je nekovinski element.
- Magnezijev klorid MgCl2: Magnezij Mg donira dva elektrona dvema atomoma klora, kot je prikazano na spodnji sliki:
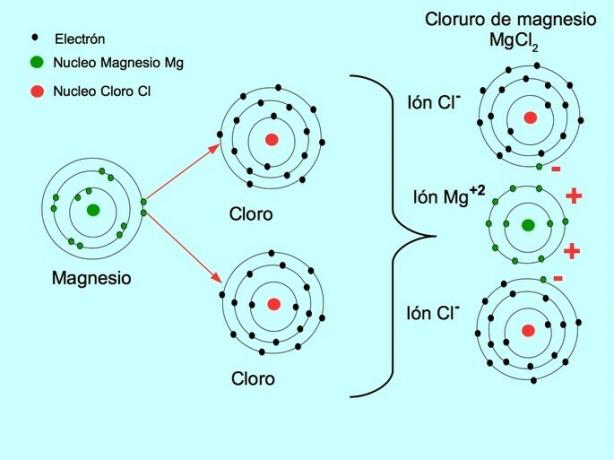
Poglej tudi Razlika med kationi in anioni.
Kovalentna vez
Kovalentna vez nastane, ko si dva nekovinska atoma delita elektrone. Ta vez je lahko več vrst, odvisno od afinitete do elektronov atomov in količine skupnih elektronov.
Nepolarna kovalentna vez
Nepolarna kovalentna vez je vez, ki nastane med dvema atomoma, pri čemer se elektroni delijo enako. Ta vez se običajno pojavi v simetričnih molekulah, to je molekulah, sestavljenih iz dveh enakih atomov, kot je molekula vodika H2 in molekulo kisika O2.

Polarna kovalentna vez
Polarna kovalentna vez nastane, ko si dva atoma delita elektrone, vendar ima eden izmed njih večjo privlačnost za elektrone. Zaradi tega ima molekula bolj negativni "pol" z več elektroni, nasprotni pol pa bolj pozitiven.
Molekule s to porazdelitvijo ali neravnovesjem elektronov so znane kot polarne. Na primer, v vodikovem fluoridu HF obstaja kovalentna vez med vodikom in fluorom, vendar ima fluor večjo elektronegativnost, zato močneje privlači elektrone v skupni rabi.
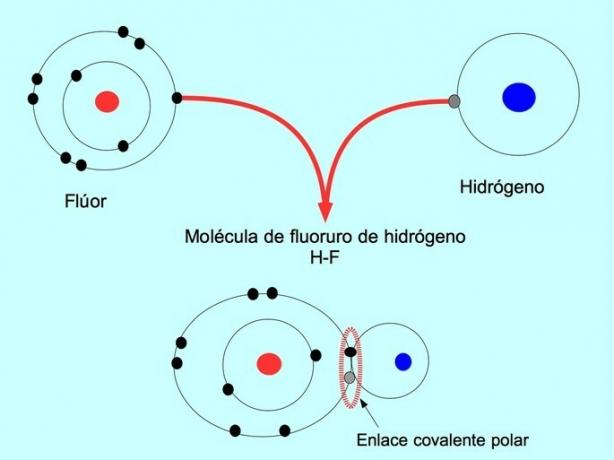
Preprosta kovalentna vez
Ko si dva atoma delita dva elektrona, po enega iz vsakega, nastala kovalentna vez imenujemo enojna kovalentna vez.
Na primer, klor je atom, ki ima v svoji zunanji lupini sedem valentnih elektronov, ki jih lahko napolnimo z osmimi elektroni. Klor se lahko kombinira z drugim klorom in tvori molekulo klora Cl2 ki je veliko bolj stabilen kot samo klor.
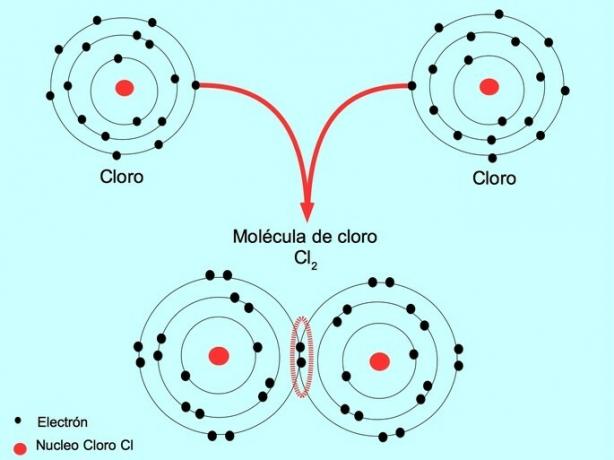
Dvojna kovalentna vez
Dvojna kovalentna vez je vez, kjer si štirje elektroni (dva para) elektronov delijo dva atoma. Na primer, kisik ima v zadnji lupini 6 elektronov. Ko se združita dva kisika, si med seboj delijo štiri elektrone, zaradi česar ima vsak v zadnji lupini 8 elektronov.
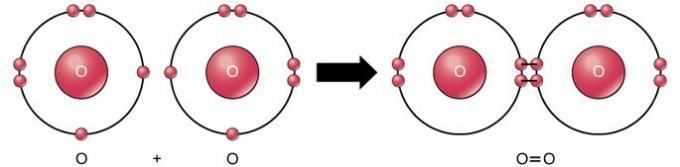
Trojna kovalentna vez
Trojna kovalentna vez nastane, ko si med dvema atomoma razdelimo 6 elektronov (ali tri pare). Na primer, v molekuli vodikovega cianida HCN nastane trojna vez med ogljikom in dušikom, kot je prikazano na spodnji sliki:
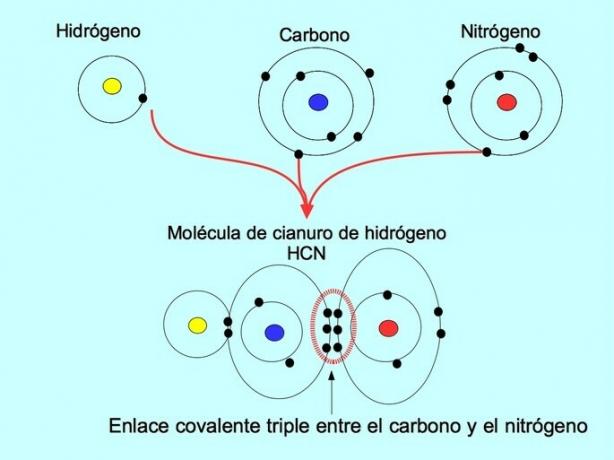
Koordinatna ali dativna kovalentna vez
Koordinirana ali dativna kovalentna vez je vez, ki nastane, ko samo eden od atomov v vezi prispeva par elektronov. Na primer, ko reagira amoniak NH3 z borovim trifluoridom BF3, Dušik se z dvema elektronoma veže neposredno na bor, ki nima elektronov, ki bi jih lahko delili. Na ta način tako dušik kot bor ostaneta v svoji valentni lupini z 8 elektroni.
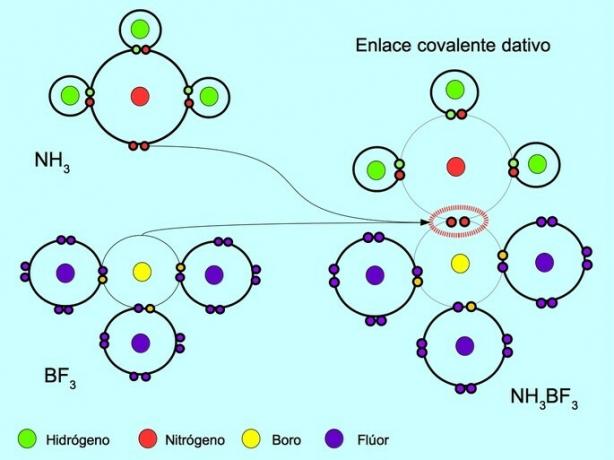
Poglej tudi Organske in anorganske spojine.
Medmolekularne povezave
Molekule se povezujejo s silami, ki omogočajo tvorbo snovi v tekočem ali trdnem stanju.
Dipol-dipolne vezi ali sile
Med polarnimi molekulami se lahko vzpostavijo šibke medmolekularne vezi, kadar negativni polovi privlačijo pozitivne polove in obratno. Na primer metanal H2C = O je polarna molekula z delnim negativnim nabojem na kisiku in delno pozitivnim nabojem na vodikih. Pozitivna stran ene metanske molekule privlači negativno stran druge metanske molekule.
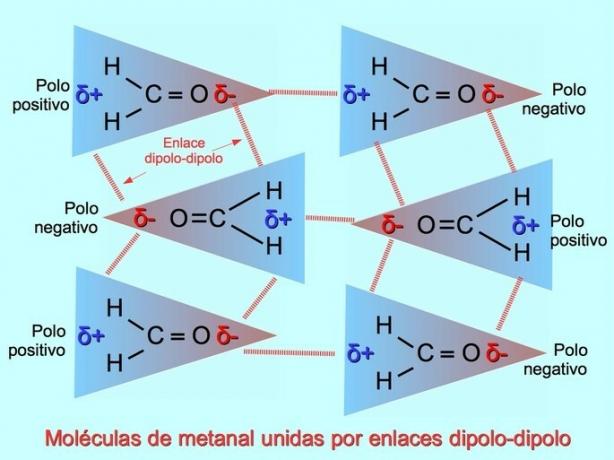
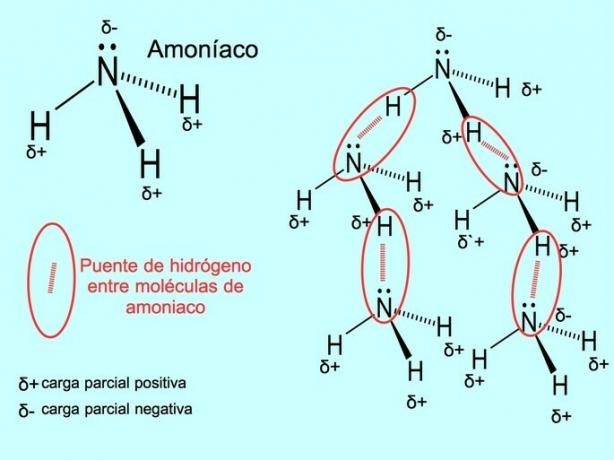
Vodikove vezi ali vezi
Vodikova vez ali vodikova vez je vez, ki se vzpostavi med molekulami. Pojavi se, kadar je vodik v molekuli kovalentno vezan na kisik, dušik ali fluor. Kisik, dušik in fluor so atomi z višjo elektronegativnostjo, zato močneje privlačijo elektrone, ko jih delijo z drugim manj elektronegativnim atomom.
Med molekulami vode H obstajajo vodikove vezi2O in amoniak NH3 kot prikazuje slika:
Morda vas zanima ogled:
- Atomi in molekule.
- Primeri organskih in anorganskih spojin.
- Kovine in nekovine
Reference
Zumdahl, S. S., Zumdahl, S. A. (2014) Kemija. Deveta izdaja. Brooks / Cole. Belmont.
Commons, C., Commons, P. (2016) Heinemannova kemija 1. 5. izdaja. Pearson Avstralija. Melbourne.


