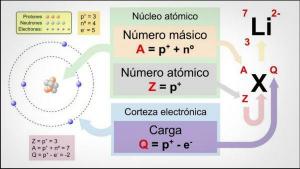
Atomstruktur och egenskaper

Bild: SlidePlayer
Atomer är en del av vår värld. All materia är gjord av atomer, så det är viktigt att bättre förstå vad de består av och vad deras funktioner är. I den här lektionen från en LÄRARE ska vi berätta för dig vad struktur av en atom och egenskaper. Om du vill veta mer om partiklarna som utgör allt, fortsätt läsa den här artikeln.
Index
- Vad är atomer?
- Atomens struktur
- Atomens viktigaste egenskaper
- Vad är isotoper?
- Hur finns atomerna i naturen?
Vad är atomer?
De atom det är den minsta enheten i vilken materia kan delas utan att förlora sina kemiska egenskaper, det vill säga dess egenskaper som ett kemiskt element. Atomen är ursprunget till allt som kan ses eller beröras, från stjärnorna till din frukost i morse.
Om vi lägger bort förlusten av dess kemiska egenskaper kan vi säga att atomen består av olika partiklar, kallade subatomära partiklar. Det finns tre typer av subatomära partiklar -protoner, neutroner och elektroner- med olika egenskaper.
Dessa partiklar är grupperade i olika antal för att bilda de kemiska elementen (syre, kol, etc.), men de kommer alltid att fördelas enligt en fast struktur.

Bild: Google Sites
Atomens struktur.
Atomstrukturen är fixerad, det vill säga vi kan ha olika typer av atomer (väteatomen, syreatomen, etc.) men deras subatomära partiklar är alltid organiserade på ett liknande sätt som ett planetsystem.
Du kommer säkert ihåg hur solsystemet är organiserat: solen är i centrum och runt från detta roterar planeterna och beskriver olika banor, några närmare och andra mer avlägsna från Sol. När det gäller atomer, i mitten är kärna, med en form som liknar en björnbär och består av neutroner och den protoner.
Runt kärnan finns Bark vilket är det område genom vilket elektroner. Tidigare trodde man att elektroner beskrev vissa banor, liknande planeter, även om det nu är vet att dessa banor inte är så väl definierade och att de liknar områden där vi är mer benägna att befinna oss elektroner.
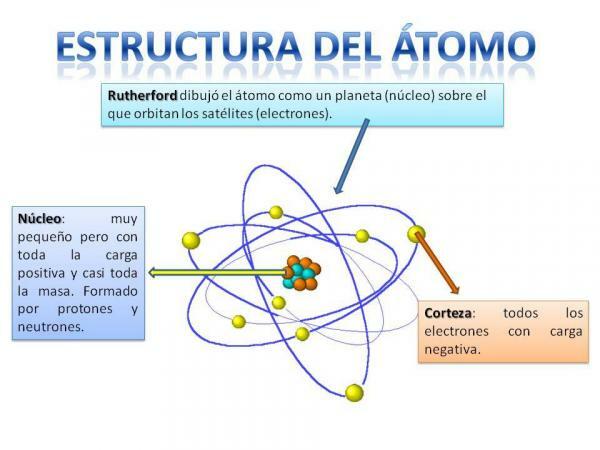
Bild: REA - Plan Ceibal
Atomens huvudsakliga egenskaper.
För att fortsätta med denna lektion om atomens struktur och egenskaper är det viktigt att fokusera på de element som gör att en atom betraktas som sådan.
Och för detta måste vi svara på den här frågan: Varför bestämmer alla atomer att beställa sig själva på ett visst sätt? Svaret är enkelt: det beror på elektriska attraktionskrafter. Atomens kärna består av neutroner som inte har någon elektrisk laddning och protoner som har en positiv elektrisk laddning. och elektronerna har en negativ elektrisk laddning, så det finns en liknande attraktionskraft mellan kärnan och elektronerna produceras mellan de två polerna på en magnet men är inte tillräckligt stark för att elektroner ska "falla" till kärna.
Detta förstås bättre om vi tar hänsyn till kärnstorlek: om atomen till exempel hade dimensionen på en fotbollsstadion, skulle kärnan ha dimensionen på bollen i mitten från fältet Hur mycket attraktiv kraft fotbollskulan skulle behöva göra för att stadionblekarna skulle kunna falla på den!
Funktionen hos neutroner
Nu kanske du undrar och vilken roll spelar neutroner? Trots att de inte har någon elektrisk laddning har neutroner en stor roll inom atomen: de bidrar med 99% av massan. Om det hjälper dig att komma ihåg kan vi säga att en atom är som ett gäng med tre vänner: den tunga neutron, den positiva protonen och den negativa elektronen, som går runt och runt neutronen och elektron.
Elektronernas rörelse
Vid den här tiden vill jag att vi ska gå tillbaka till något som vi hade kvar i bläckhuset: banorna som elektronerna beskriver runt kärnan. Vi hade sagt det elektroner kretsar kring kärnan Som planeterna gör runt solen, några närmare än andra, varför gör de det? Elektroner roterar i ett eller annat skal enligt den energi de har för att röra sig bort från kärnan, det vill säga de elektroner som är närmare kärnan har inte tillräcklig kraft för att röra sig bort från kärnan medan de i yttersta lager (orbitaler) i skorpan har mer energi och har kunnat röra sig längre bort från kärnan. kärna. Vidare finns det i var och en av orbitalerna en maximal kapacitet på 8 elektroner (oktettregel).
Partiklarna i en atom
Vi kommer att återvända till ett annat tillvägagångssätt som vi har gjort tidigare men inte har förklarat: atomer består av neutroner, protoner och elektroner, som alltid kombineras efter samma struktur av kärna och skorpa, men de gör det i olika antal för att bilda de olika kemiska elementen. Hur kan vi få så många element som bara kombinerar tre typer av partiklar? De kemiska elementen, som du någonsin sett representeras i det periodiska systemet, kännetecknas av att de har ett visst atomnummer.
De atomnummer (Z) Det berättar för oss antalet protoner i kärnan hos denna typ av atomer, vilket är lika med antalet elektroner under normala förhållanden. Således kommer till exempel alla atomer som har 6 protoner (Z = 6) att vara kolatomer, och de kommer att ha samma kemiska egenskaper; Atomerna med 5 protoner (Z = 5) kommer att vara boratomer, med samma kemiska egenskaper som varandra och skiljer sig från de hos kolatomer. Du behöver inte förväxla atomnummer med atomvikt eller massnummer (A), som är summan av vikten av neutroner och protoner (elektronernas vikt är försumbar med avseende på den totala kärnans vikt).

Bild: SlidePlayer
Vad är isotoper?
I naturen kan vi hitta olika "undertyper" av element, isotoper. Jag är säker på att du någon gång har hört talas om kol 14, en radioaktiv isotop av kol som används för att bland annat bestämma fossilåldern. Isotoper är två atomer med samma antal protoner (samma atomnummer), men olika antal neutroner, (olika atommassa). Isotoperna av samma element benämns vanligtvis med namnet på elementet följt av dess atommassa.
I vårt exempel är båda isotoperna kol, så de har ett atomnummer på 6 (Z = 6) men kol 12 ("normalt" kol) har en atomvikt på 12 mot atomvikten på kol 14 14. Isotoperna av samma element har mycket liknande kemiska och fysikaliska egenskaper. När det gäller kol 14, till skillnad från kol 12, är det en radioaktiv isotop som finns i alla element som innehåller kol, inklusive levande varelser.
Och med detta avslutar vi denna lektion om atomens struktur och egenskaper. Vi hoppas att det har varit till hjälp för dig.

Bild: Dina uppgifter
Hur finns atomerna i naturen?
Atomer kan hittas isolerat, men det mest normala är att hitta dem i grupper kallad molekyler.
Molekyler kan bestå av atomer av samma element (såsom syremolekylen, som består av två atomer av syre) eller genom grupper med atomer av olika element (två atomer av väte och en av syre bildar molekylen av Vatten). Dessa grupper av element kallas molekyler, som i sin tur kan kombineras med varandra och bildar olika mer och mer komplexa grupperingar beroende på deras reaktivitet och deras kemiska affinitet för källa till kemiska länkar.
Om du vill läsa fler artiklar som liknar Atomstruktur och egenskaperrekommenderar vi att du anger vår kategori av Atomen.