ALLA egenskaperna hos ATOM

Bild: SlideShare
Även om vi inte kan se dem med blotta ögat, atomer är en del av all materia av vår planet. All materia är gjord av atomer, som grupperar sig för att bilda kemiska element, molekyler, föreningar etc. Atomen definieras som minsta basenhet av materia som har egenskaperna hos ett kemiskt element. Varje kemiskt grundämne definieras av typen av atom den är gjord av, så den sista frågan är: vilka egenskaper har atomen? I den här lektionen från en LÄRARE kommer vi att granska egenskaperna hos atomen som gör varje atom till ett karakteristiskt kemiskt element.
Index
- Vad är atomen?
- Atomnummer, massnummer och isotoper
- Densitet, en annan av atomens egenskaper
- Jonisk radie och Vanderwalls radie
- Joniseringsenergi
Vad är atomen?
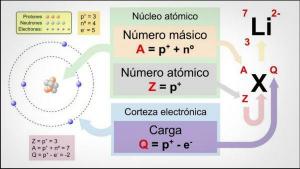
Innan vi går in för att analysera atomens egenskaper är det viktigt att vi vet bättre vad det handlar om. De atom är en enhet bildad av tre subatomära partiklar: protoner, neutroner och elektroner. Dessa är organiserade i kärnan och cortex.
- De kärna Den består protoner Y neutroner, som är i atomens centrum, och som ansvarar för större delen av atomens vikt; protoner är positivt laddade, medan neutroner är neutrala så att kärnan är positivt laddad.
- De Bark Det bildas av elektroner, som är små, negativt laddade partiklar som roterar runt kärnan och bildar banor (som planeterna) men utan att någonsin falla till atomens kärna. Atomens cortex är ansvarig för att interagera med cortex i andra atomer eftersom den ligger på utsidan av atomerna.
De olika atomerna består av protoner, neutroner och elektroner, samma i alla kemiska element. Så vad gör det olika kemiska element? Antalet protoner, neutroner och elektroner av vilka atomerna för varje element består är olika och detta i sin tur gör att varje element har olika funktioner eller andra.

Bild: SlideShare
Atomtal, massnummer och isotoper.
De tre första egenskaperna har att göra direkt med antalet partiklar som utgör varje atoms atom.
De atomnummer (Z) anger antalet protoner som utgör atomens kärna. Så till exempel kommer alla järnatomer att ha 26 protoner i sin kärna. Dessutom, om de inte säger något annat, är de kemiska elementen i neutralt tillstånd, det vill säga positiv (protoner) och negativ (elektron) laddning är densamma, så de kommer alla också att ha 26 elektroner.
De massnummer eller atomvikt (A) anger det totala antalet protoner och neutroner som utgör atomens kärna. Som vi redan har angett tidigare är vikten av elektroner praktiskt taget försumbar jämfört med den för elektroner. protoner och neutroner, så massantalet indirekt indikerar vikten av atomen i fråga. Fortsätter du med exemplet på järn, om du konsulterar det periodiska elementet ser du att vikten Atomen i detta element är 55,85, vilket betyder att alla atomer i det elementet kommer att ha det vikt.
Slutligen, isotoper av ett kemiskt element är varianter av samma atom (det vill säga de har samma atomnummer) men ett annat massnummer, det vill säga ett annat antal neutroner. De flesta kemiska element har mer än en naturlig isotop, grundämnet med den högsta mängden stabila isotoper är Tin (Sn), som har 10 olika naturliga isotoper.
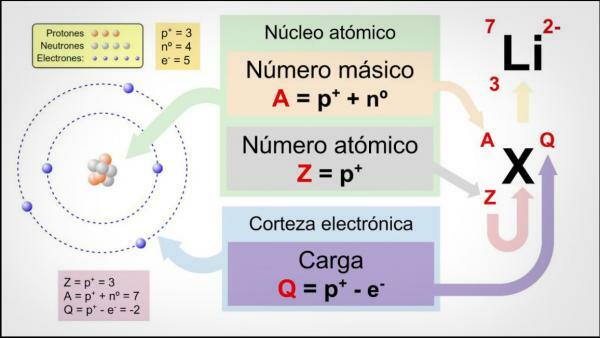
Bild: ConceptDefinition.de
Densitet, en annan av atomens egenskaper.
De densitet av en atom är antalet massaenheter (u.m.a) av elementet som finns i en viss rymdvolym. Densiteten hos alla ämnen symboliseras genom den grekiska bokstaven "Ro" (skriven r) och dess enheter enligt det internationella systemet för enheter (SI) är kilogram per kubikmeter (kg / m3). När det gäller kemiska grundämnen, som är så små, är gram per kubikcentimeter (g / cm3).
För att beräkna en atoms densitet (atomdensitet), skulle vi behöva ta hänsyn till atommassan och dess volym. Medan större delen av massan av atomen är i samma kärna, måste volymen göra med hur stor atomen är, och därför kommer antalet elektroniska orbitaler att spela en roll Viktig. Med hänsyn till dessa egenskaper och deras tendens i det periodiska systemet kan vi konstatera att densiteten ökar när vi ökar i en grupp och ökar också när vi närmar oss den centrala delen av periodiska systemet.
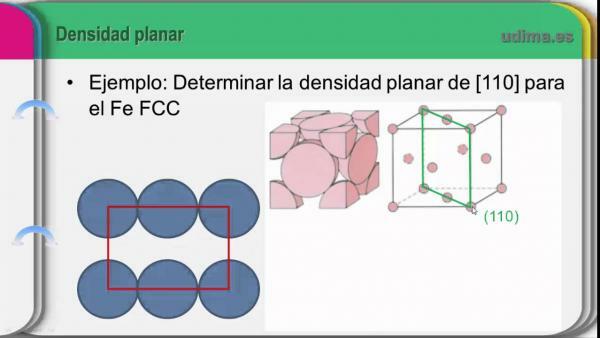
Bild: YouTube
Jonisk radie och Vanderwalls radie.
De jonisk radie är den radie som en jon av ett element har i joniskt kristalltillstånd. I det tillståndet är jonerna så nära varandra att de yttersta elektroniska orbitalerna är i kontakt med varandra.
Å andra sidan, vanderwalls radie är avståndet som två atomer hålls isär på grund av avstötningen av negativa laddningar mellan elektronerna i var och en av atomerna. Vanderwalls-radien skulle vara radien för en imaginär fast sfär som används för att modellera atomen så att den inte används mycket i den dagliga praktiken.
Till skillnad från vad som händer med densitet eller massa, är dessa två egenskaper nära besläktade med atomens volym, det vill säga, de har mer att göra med antalet elektroner i den än med kärna.

Bild: SlidePlayer
Joniseringsenergi.
Slutligen är en annan av atomens egenskaper den joniseringsenergi, en egenskap som berättar för oss vilken energi vi behöver för att separera en elektron i dess jordtillstånd (annat än en anjon eller katjon) av en atom av ett element i ett gasformigt tillstånd men det kan också definieras som den kraft med vilken en elektron binder med andra molekyler. Den här egenskapen är mycket intressant eftersom den gör det möjligt för oss att få en grov uppfattning om förmåga att reagera av en atom av ett visst kemiskt element. Joniseringsenergin är högre när vi tar bort elektroner, så för ett element finns det en energi av första jonisering, en andra joniseringsenergi, och så vidare och de blir större och större.
Som i föregående fall är denna egenskap också nära relaterad till antalet orbitaler i det berörda elementet eftersom ju färre orbitaler det har desto mer kostar det att ta bort elektronerna från en atom fast besluten.
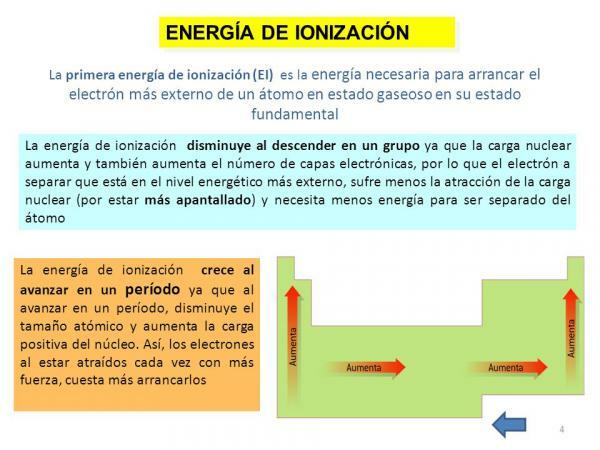
Bild: SlidePlayer
Om du vill läsa fler artiklar som liknar Atoms egenskaperrekommenderar vi att du anger vår kategori av Atomen.